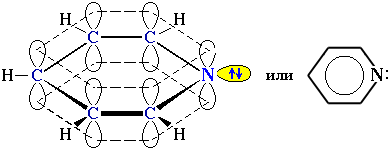
Строение
Строение пиридина полностью аналогично строению бензола, с той лишь разницей, что одна группа СН бензола заменена в пиридине на атом азота. Такая замена приводит к следующим существенным изменениям: (а) нарушается геометрия правильного гексагона, поскольку связь углерод – азот короче, чем связь углерод — углерод; (б) в молекуле пиридина вместо одного атома водорода, расположеного в плоскости цикла, присутствует неподеленная пара электронов, также расположенная в плоскости цикла, занимающая sp2-гибридную орбиталь и не принимающая участия в образовании ароматического секстета электронов (именно эта неподеленная пара электронов обусловливает основные свойства пиридина); (в) молекула пиридина представляет собой постоянный диполь вследствие большей электроотрицательности атома азота по сравнению с атомом углерода.
Электроотрицательный атом азота способствует индуктивной поляризации молекулы пиридина в результате смещения электронной плотности преимущественно по σ-связям. Кроме того, атом азота определяет стабильность поляризованных канонических структур, в которых он отрицательно заряжен — структуры 3, 4 и 5. Эти структуры вместе со структурами 1 и 2, которые полностью аналогичны формулам Кекуле бензола, вносят вклад в строение молекулы пиридина. Поляризованные канонические структуры подразумевают также постоянно присутствующую в молекуле пиридина поляризацию системы π-электронов (при рассмотрении с позиций более строгого метода молекулярных орбиталей это связано с относительным различием в орбитальных коэффициентах ВЗМО и НСМО).
Поскольку индуктивный и мезомерный эффекты имеют одну и ту же направленность, молекула пиридина поляризована со смещением электронной плотности к атому азота. Это также означает, что на атомах углерода пиридинового цикла локализуется частичный положительный заряд, особенно на α- и γ-атомах углерода. Поскольку на атомах углерода молекулы пиридина наблюдается некий дефицит электронов, пиридин и аналогичные гетероароматические соединения принято относить к электронодефицитным гетероциклическим соединениям или, как иногда говорят, π-дефицитным. Пиридин проявляет основные свойства. Он намного основнее пиррола. Основность пиридина несколько больше, чем у ароматических, но заметно меньше, чем у алифатических аминов. Избыток электронной плотности у гетероатома позволяет сделать вывод: пиридиновый атом азота – основный и нуклеофильный центр. Понятие «пиридиновый атома азота» применяется ко всем азотсодержащим гетероциклам, в которых атом азот обладает свойствами аналогичными атому азота пиридина.
|