Колоночная хроматография
Дикун Ю.С. МТМ - 11 Доклад на тему: Колоночная хроматография Колоночная хроматография – способ разделения смесей жидких или твердых веществ, основанный на различном средстве разделяемых веществ к неподвижной (сорбент) и подвижной (элюент) фазам. Как правило, чем лучше вещество сорбируется неподвижной фазой - тем медленнее вещество выходит с колонки. Область применения: 1) Разделение смесей жидких или твердых веществ, различающихся по Rf. 2) Отделение целевого вещества от не сорбирующихся примесей. Колоночная хроматография напоминает противоточную экстракцию. Она основана на распределении растворенных веществ между подвижной органической фазой и водной фазой, удерживаемой твердым носителем. Носитель должен быть инертен по отношению к разделяемым веществам, но должен хорошо удерживать неподвижную жидкую фазу. Обычно применяемые носители (силикагель, кизельгур, целлюлоза) удерживают 0,5-1 мг жидкой фазы на 1 г собственной массы. В качестве неподвижной жидкой фазы чаще всего используют воду. При разделении веществ, хорошо растворимых в органических растворителях, часто поступают наоборот: твердый носитель пропитывают органическим растворителем, а в качестве подвижной жидкой фазы используют воду. Колоночной распределительной хроматографией удобно пользоваться для препаративного выделения чистых веществ. Типичный прибор для колоночной хроматографии приведен на рису.1.
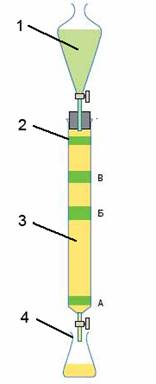
Рис. 1 - Прибор для колоночной хроматографии, где: 1 – Элюент; 2 - Хроматографическая колонка и количество сорбента; 3 – Сорбент; 4 – Приемники фракции; 5 – Лапка. Существуют следующие требования к элюенту § Выделяемые вещества не должны взаимодействовать с элюентом или разрушаться при его присутствии. § Элюент может быть или индивидуальным растворителем или смесью нескольких растворителей. Растворители должны легко удаляться после выделения веществ (поэтому диметилсульфоксид (ДМСО) или диметилформамид (ДМФА) не подходят из-за высокой температуры кипения). § Элюент подбирают таким образом, чтобы на тонкослойной хроматограмме смеси (желательно на том же сорбенте), Rf продуктов различался не менее 0.15, и пятна выходили с Rf не более 0.5-0.6 после одного прогона хроматограммы. § Если под действием растворителей различной полярности (полярных (метанол, возможно с добавлением уксусной кислоты или триэтиламина) и неполярных (гексан, пентан)) вещество не сдвигается со старта или двигается с фронтом, следует перейти к другому сорбенту. Пример: Rf = 0, так ведут себя высоко полярные вещества (ионные жидкости, амины) на силикагеле; или неполярные вещества на сорбентах с обращенной фазой. Элюент добавляется или непосредственно, или при помощи капельной (делительной) воронки. При проведении хроматографирования слой сорбента ни в коем случае не должен пересыхать, иначе может произойти его растрескивание, приводящее к снижению разделяющей способности. Хроматографическая колонка и количество сорбента - представляет собой стеклянную трубку, один из концов которой имеет пористую насадку или заткнут кусочком ваты, для того чтобы сорбент не высыпался. Длина колонки зависит от Rf разделяемых веществ. Чем меньше разница в Rf - тем длиннее колонка (слой сорбента). Пример: Для разделения 2-х веществ с разницей в Rf ~ 0.4 требуется колонка около 10 см. Ширина колонки зависит от количества (г) разделяемой смеси. Чем больше количество - тем шире колонка. Сорбент - выбирается исходя из свойств разделяемой смеси. Разделяемые вещества не должны разрушаться в присутствии сорбента. Если под действием растворителей различной полярности (полярных (метанол, возможно с добавлением уксусной кислоты или триэтиламина) и неполярных (гексан, пентан)) вещество не сдвигается со старта или двигается с фронтом, следует перейти к другому сорбенту (от полярного сорбента к неполярному и наоборот). Приемники фракций. Для сбора фракций можно использовать как обычные плоскодонные колбы, так и пробирки. Когда разделяемые вещества окрашены, видно как они выходят с колонки. Каждое вещество собирают в отдельный приемник. Если вещества выходят смесью - смесь собирают отдельно. Если разделяемые вещества не окрашены, ведут сбор фракций определенного объема, который зависит от размеров колонки и от степени разделения веществ (Rf). Пример: Обычно при делении 0.2 г исходной смеси собирают по 7-10 мл фракций, при делении 2-3 г - по 20-25 мл. Собранные фракции анализируют при помощи тонкослойной хроматографии (ТСХ). Колонку закрепляют на штативе при помощи лапки. Металлическая лапка не должна соприкасаться со стеклом, для избегания растрескивания колбы при перегонке. Для этого между колбой и лапкой помещают резиновые прокладки.
Методика проведения колоночной хроматографии. В качестве хроматографических колонок используют стеклянную бюретку 8-12 мм и длиной 25-30 см. Колонку закрепляют штативом. На дно колонки (перед сужением) кладут кусок стеклянной ваты. Оксид алюминия (для хроматографии) сеют через сито (0,25 мм). Сорбент засыпают в колонку в сухом виде или в виде суспензии в таком растворителе, в котором будет происходить хромаграфуванняю В первом случае оксид алюминия засыпают в колонку, заполненную растворителем, и все время слегка постукивают по колонке, чтобы адсорбент равномерно уплотняя. Избыток растворителя выпускают через кран. При втором способе заполнения колонки оксид алюминия сильно смачивают в растворителе и суспензию наливают небольшими порциями в колонку, слегка постукивая по ней для равномерного осаждения сорбента. В верхней части колонки помещают тампон из стеклянной ваты, закрывающий слой сорбента. Сорбент не должен быть заполнен доверху колонки. Затем сверху постепенно доливают раствор в таком количестве, чтобы над поверхностью адсорбента всегда оставался небольшой слой жидкости. Когда раствор полностью протечет через колонку, вливают чистую элюент и начинают проявки хроматограммы. Наблюдая за разделением окрашенных веществ, следят за образованием цветных зон. Если компоненты смеси необходимо выделить, то хроматограмму элюють, продолжая добавлять растворитель. Постепенно слои разделенных веществ спускаются вниз колонки. Их вымывают из колонки и собирают в отдельные приемники. Если разделению подвергать смесь бесцветных веществ, то за ходом элюирования наблюдают, отбирая константы веществ, оставшихся в каждой фракции. В случае плотного слоя сорбента раствор в колонке проходит медленно. Тогда элюент пропускают под давлением воздуха в верхнюю часть колонки или отсасывают из колонки с помощью водоструйное насоса.
Рекомендации при проведении колоночной хромотографии Современные методы колоночной хроматографии позволяют, пожалуй, разделять смеси любого состава. Для этого необходимо тщательно подобрать для каждого компонента смеси: элюент и сорбент. 1. Перед проведением колоночной хроматографии необходимо подобрать элюент и сорбент при помощи тонкослойной хроматографии Для эффективной очистки выделяемого компонента смеси должно иметь значение Rf должно быть ~0.5. Примеси должны отличаться по Rf не менее, чем на 0.15. 2. Элюент для колоночной хроматографии должен быть менее полярным, чем для тонкослойного храмотографиического анализа. 3. Для эффективного разделения смеси нескольких веществ можно использовать градиентное элюирование, т.е. (на примере хроматографии на силикагеле), начинать элюировать неполярными растворителями (пентан, гексан), далее постепенно увеличивать полярность смеси (смеси: гексан/этилацетат от 20:1 до 1:5) и, наконец, переходить к высоко полярным растворителям и смесям (метанол, смеси метанол/триэтиламин 20:1). 4. Способы заполнения колонки сорбентом: § Сухой способ. Колонка заполняется сорбентом. После чего сразу наносят вещество и приступают к элюированию. Большой минус этого способа - частое растрескивание слоя сорбента - из-за чего плохое разделение. Данный способ подходит для флеш-хроматографии, т.е. отделения целевого вещества от примесей с Rf ~0. § Элюент затем сорбент. Колонку заполняют до половины длины элюентом, затем порциями засыпают сорбент, следя, чтобы он полностью смачивался. Минус этого способа - если сорбент достаточно мелкий, он слипается комками и падает на дно колонки в виде шариков. Способ часто применяют при работе с крупнозернистым силикагелем. § Сорбент в виде суспензии в элюенте. В колонку засыпают необходимое количество сухого сорбента (чтобы определить необходимое количество), высыпают его из колонки в химический стакан. Заливают сорбент элюентом и перемешивают для равномерного смачивания. Через некоторое время суспензию взбалтывают и выливают при помощи химической воронки на колонку. Остатки сорбента смывают со стенок химического стакана элюентом. 5.Способы нанесения вещества на колонку: § Сухой способ. Вещества наносятся в индивидуальном виде - твердом (просто насыпают на колонку) или жидком (переносят пипеткой на колонку). § В растворе. Вещество растворяют в минимальном количестве элюента или менее полярном растворителе, чем элюент и наносят пипеткой. Растворитель должен быть менее полярный, чем элюент, иначе вещество вытянется с колонки вместе с этим растворителем. Чем уже слой раствора с веществом - тем лучше разделение. § В виде твердой смеси с сорбентом. Вещество смешивают с сорбентом с добавлением небольшого количества растворителя. Растворитель удаляют на роторном испарителе. Сухой сорбент с веществом насыпают на колонку. 6. Наносить вещество на колонку (жидкое или в растворе) следует по стенкам колонки, чтобы не размывать слой сорбента. Чем ровнее нанесено вещество, тем лучше его разделение. 7. После нанесения вещества верхний слой сорбента на колонке можно накрыть ваткой или фильтровальной бумагой, чтобы при добавлении элюента не происходило размывание слоя сорбента. Чем ровнее слой сорбента, тем лучше разделение веществ. 8. Элюирование под давлением. В принципе, в большинстве случаев элюирование проводят при атмосферном давлении. Так как чем быстрее скорость элюирования - тем хуже разделение. Однако, при использовании мелкозернистых сорбентов без элюирования при избыточном давлении не обойтись из-за крайне низкой скорости процесса. В этих случаях применяют колбы Бунзена, в которые помещают хроматографические колонки и подключают к вакуумному насосу (наиболее подходит при проведении флеш-хроматографии на фильтре Шотта) или нагнетают давление при помощи груши. При проведении хроматографирования слой сорбента ни в коем случае не должен пересыхать, иначе может произойти его растрескивание, приводящее к снижение разделяющей способности.
|