СПИРТЫ (ОКСИСОЕДИНЕНИЯ)
Производные углеводородов, получаемые замещением одного или нескольких атомов водорода на группу ОН (окси-группа). Физические свойства: С1-С11-при комнатной температуре жидкости,С12-твердые вещества. Среди спиртов нет газообразных веществ. Между молекулами спиртов возникают водородные связи и поэтому образуется межмолекулярные ассоциаты. у спиртов температура кипения выше чем у алканов. С1-С3-хорошо растворимы в воде. Классификация 1. По строению цепи (предельные, непредельные). 2. По атомности – одноатомные (одна группа ОН), многоатомные (2 и более групп ОН). 3. По положению группы ОН (первичные, вторичные, третичные). Предельные одноатомные спирты Общая формула СnH2n+1OH По систематической номенклатуре (IUPAC) спирты называют по углеводородам, соответствующим самой длинной цепочке углеродных атомов с добавлением окончания “ол”, 6 5 4 3 2 1 СН3-СНCH3-СН2-СН2-СНOH-СН3 5-метил-2-гексанол Нумерацию начинают с того конца, ближе к которому расположена группа ОН. Изомерия 1. Структурная – изомерия цепи изомерия положения окси-группы 2. Пространственная – оптическая, если все три группы у углерода, связанного с группой ОН, разные, например: СН3-СC3H7OH-С2Н5 3-метил-3-гексанол Получение 1. Гидролиз галоидных алкилов C2H4-Cl2+2NaOH=C2H4(OH)2+2NaCl а) первичные спирты получают действием металлорганических соединений на формальдегид: СН3-MgBr + CH2=O CH3-CH2-O-MgBr CH3-CH2OH + MgBr (OH) б) вторичные спирты получают действием металлорганических соединений на другие альдегиды: CH3-CH2-MgBr+CH3-C CH3-COH-CH2-CH3 CH3-CHOH-CH2-CH3+MgBr (OH) в) третичные спирты – действием металлорганических соединений на кетоны: CH3-CO-CH3 + H3C-MgBr CH3-CCH3OMgBr-CH3 CH3-CCH3OH-CH3 + MgBr (OH) 2.Окисление алкенов a)раствором KMnO4 на холоде 3CH2=CH2+KMnO4+4HOH= 3CH2OH-CH2OH+2MnO2+2KOH б)с последующим гидролизом. 2C2H4+O2=2C2H4O+HOH= CH2OH-CH2OH 3. Восстановление альдегидов, кетонов: CH3-CHO + H2 CH3-CO-CH3 + H2 CH3-CHOH-CH3 4.получение из синтез-газа CO+2H2=CH3OH Химические свойства Обуславливаются наличием группы ОН. Она определяет важнейшие свойства спиртов. Можно выделить 3 группы химических превращений с участием группы ОН. I.Реакции замещения водорода в окси-группе. 1) Образование алкоголятов а) действие щелочных металлов и некоторых других активных металлов (Mg, Ca, Al) C2H5OH + Na Алкоголяты нацело разлагаются водой с образованием спиртов и щелочи. C2H5ONa+HOH б) Реакция Чугаева-Церевитинова – действие магнийорганических соединений. C2H5OH + CH3MgBr Реакция применяется в анализе спиртов для определения количества “подвижного водорода”. В этих реакциях спирты проявляют очень слабые кислотные свойства. 2) Образование сложных эфиров на остаток кислоты – ацил. Реакция этерефикации – взаимодействие спиртов с карбоновыми кислотами. R1-COOH+HO-CH2-R2= R1-COO-CH2-R2+HCl 3) Образование простых эфиров Простые эфиры образуются в результате замещения водорода окси-группы на алкил (алкилирование спиртов). а) алкилирование галоидными алкилами C2H5OH + ClCH3 б) алкилирование алкилсульфатами или диалкилсульфатами C2H5OH + CH3O-SO2OH C2H5OH + CH3OSO2OCH3 в) межмолекулярная дегидратация в присутствии твердого катализатора C2H5OH + HOC2H5 II. Реакции с отрывом группы ОН. 1) Замещение группы ОН на Hal. а) действие HHal C3H5(OH)3+HBr = C3H5(OH)2Br + HOH б) действие PHаl и PНal5 R-CH2-OH+PCl5 = R-CH2-Cl + POCl3 + HCl в) действие SOCl2 и SO2Cl2 R-CH2-OH +SOCl2 = R-CH2-Cl+SO2 + HCl 2) дегидратация спиртов (внутримолекулярное отщепление воды) R-CH2-OH+H2SO4 = R-CH=CH2 + HOH Отщепление водорода идет от наименее гидрированного из 2-х соседних звеньев с гидроксилсодержащими (правило Зайцева). III. Окисление и дегидрирование спиртов Отношение спиртов к окислению связано с индукционным влиянием связи С-О. Полярная связь С-О увеличивает подвижность атомов водорода при углероде, связанном с группой ОН. CH3 1) Окисление первичных спиртов а) до альдегидов; CH3-CH2-OH + O б) до кислот CH3-CH2-OH+ O 2) Окисление вторичных спиртов идет до кетонов C2H5-CHOHCH3+O = H2O + C2H5-COCH3 3) Третичные спирты при аналогичных условиях не окисляются, т.к. не имеют подвижного атома углерода, связанного с группой ОН. Однако при действии сильных окислителей (концентрированные растворы при высокой температуре), реакция окисления идет с разрушением углеродной цепи. При этом окислению подвергаются соседние звенья (наименее гидрированные), т.к. там больше сказывается индукционное влияние гидроксильной группы. CH3-CCH3CH3OH-CH3+O2= H3C-COCH2-CH3+CHHO 4) Дегидрирование спиртов – под действием катализаторов. Также происходит с участием самых подвижных атомов водорода: водорода оксигруппы и водорода у соседнего атома углерода. CH3-CH2-OH В реакциях замещения и отщепления водорода наиболее активны спирты первичные, а в реакциях замещения и отщепления группы ОН, наоборот, наиболее легко реагируют спирты третичные.
|

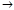
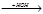


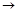
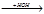
 CH3-CH2OH
CH3-CH2OH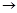
 C2H5ONa + H
C2H5ONa + H C2H5OH + NaOH
C2H5OH + NaOH C2H5OMgBr + CH4
C2H5OMgBr + CH4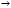 C2H5OCH3 + H2SO4
C2H5OCH3 + H2SO4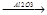 C2H5OC2H5 + H2O
C2H5OC2H5 + H2O H
H H2O + CH3-COOH
H2O + CH3-COOH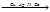 H2 + CH3-CH2-OMe
H2 + CH3-CH2-OMe


