
Головна сторінка Випадкова сторінка
КАТЕГОРІЇ:
АвтомобіліБіологіяБудівництвоВідпочинок і туризмГеографіяДім і садЕкологіяЕкономікаЕлектронікаІноземні мовиІнформатикаІншеІсторіяКультураЛітератураМатематикаМедицинаМеталлургіяМеханікаОсвітаОхорона праціПедагогікаПолітикаПравоПсихологіяРелігіяСоціологіяСпортФізикаФілософіяФінансиХімія
ЛАБОРАТОРНА РОБОТА №2
Дата добавления: 2014-10-22; просмотров: 682
|
|
| Тема: | Основні класи неорганічних сполук. Кислоти, солі. | |
| Мета: | Ознайомитись з методами одержання кислот та солей, їх хімічними властивостями. | |
| Реактиви: | Розчини: | - Натрій силікат; |
| - Сульфатна (сірчана) кислота; | ||
| - Хлоридна (соляна) кислота; | ||
| - Кальцій гідроксид; | ||
| - Кобальт (ІІ) хлорид. | ||
| Тверді речовини: | - Кальцій карбонат; | |
| - Фосфор (V) оксид; | ||
| - Сіліціум (ІV) оксид. | ||
| Індикатори: | - Метилоранж; | |
| - Лакмус; | ||
| - Фенолфталеїн. | ||
| Обладнаня: | Хімічний штатив, пробірки. |
1.1 Методичні вказівки до вивчення теоретичного матеріалу
Кислотами називають складні речовини загальної формули HXEYOZ (E – елемент). Кислоти, молекули яких не містять атомів кисню, називають безкисневими, наприклад, HCl – хлоридна (хлорводнева), H2S – сульфідна (сірководнева) та ін. Однією з основних характеристик кислот є їх основність.
Основність кислоти – це кількість атомів водню в кислоті, здатних заміщуватись у хімічних реакціях.
Негативні іони, що залишаються в молекулі кислоти після відщеплення одного або кількох іонів водню називаються кислотними залишками. Основні кислоти утворюють один кислотний залишок, а дво- чи триосновні – два чи три кислотні залишки. Наприклад, ацетатна (оцтова) кислота є одноосновною, оскільки у водних розчинах в її молекулі може заміщуватись лише один Н+-іон. При цьому утвориться один кислотний залишок.
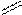 О -Н+
О -Н+
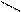 Н3С-С
Н3С-С  СН3СОО -
СН3СОО -
О-Н ацетат-іон
Для багатоосновних кислот процес заміщення Н+-іонів відбувається ступінчасто:
-Н+ -Н+ -Н+
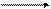
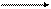
 Н3РО4 Н2РО4- НРО42- РО43-
Н3РО4 Н2РО4- НРО42- РО43-
утворюються утворюються
кислі солі середні солі
Кислоти та їх залишки
| Формула кислоти | Назва | Основність | Кислотний залишок | |
| Формула | Назва | |||
| HCl | Хлоридна | Cl - | Хлорид – іон | |
| HJ | Йодидна | J - | Йодид – іон | |
| HBr | Бромідна | Br - | Бромід – іон | |
| HNO2 | Нітритна | NO2 - | Нитрит – іон | |
| HNO3 | Нітратна | NO3 - | Нитрат – іон | |
| HCN | Цианідна | CN - | Цианід – іон | |
| H2S | Сульфідна | S 2- | Сульфід – іон | |
| H2SO3 | Сульфітна | SO3 2- | Сульфіт – іон | |
| H2SO4 | Сульфатна | SO4 2- | Сульфат – іон | |
| H2CO3 | Карбонатна | CO3 2- | Карбонат – іон | |
| H2SiO3 | Силікатна | SiO3 2- | Силікат – іон | |
| H3PO4 | Ортофосфат-на | PO4 3- | Ортофосфат – іон | |
| CH3COOH | Ацетатна | CH3COO - | Ацетат – іон |
Найхарактернішою ознакою кислот є їх здатність утворювати солі при взаємодії з основами (реакція нейтралізації), основними оксидами і металами.
Солі – це сполуки, до складу яких входять катіони металів та аніони кислотних залишків. Солі бувають середні, кислі і основні.
Середні солі можна розглядати як продукти повного заміщення водню кислоти металом, наприклад, Al2(SO4)3, MgCl2.
Кислі солі – продукти неповного заміщення водню багатоосновної основи на кислотні залишки, наприклад, Mg(НSO4)2, Ca(HSO4)2.
Основні солі – продукти неповного обміну гідроксогруп (ОН-) багатокислотної основи на кислотні залишки, наприклад, CuOHCl, Al(OH)2Cl.
Існує багато методів добування солей, які детально описані в літературі. Зверніть увагу на те, що за реакцією нейтралізації можна добути (залежно від молярних співвідношень реагентів) як середні, так і кислі та основні солі.
2Al(OH)3 + 3 H2SO4 = Al2(SO4)3 + 6 H2O
алюміній сульфат
2Al(OH)3 + 3 H2SO4 = Al2(НSO4)3 + 3 H2O
алюміній гідросульфат
2Al(OH)3 + H2SO4 = [ Al(OH)2]2 SO4 + 2 H2O
алюміній дигідроксосульфат
Al(OH)3 + H2SO4 = Al(ОН)SO4 + 2 H2O
алюміній
гідроксосульфат
Для перетворення кислих і основних солей в середні треба подіяти на них відповідно основою або кислотою.
Назви солей складаються з назви хімічного елементу і назви кислотного залишку в називному відмінку і залишку в родовому відмінку. Багато солей мають також технічну назву.
1.2 Проведення дослідів
| <== предыдущая лекция | | | следующая лекция ==> |
| ЛАБОРАТОРНА РОБОТА №1 | | | ЛАБОРАТОРНА РОБОТА №3 |