
Головна сторінка Випадкова сторінка
КАТЕГОРІЇ:
АвтомобіліБіологіяБудівництвоВідпочинок і туризмГеографіяДім і садЕкологіяЕкономікаЕлектронікаІноземні мовиІнформатикаІншеІсторіяКультураЛітератураМатематикаМедицинаМеталлургіяМеханікаОсвітаОхорона праціПедагогікаПолітикаПравоПсихологіяРелігіяСоціологіяСпортФізикаФілософіяФінансиХімія
ЛАБОРАТОРНА РОБОТА №7
Дата добавления: 2014-10-22; просмотров: 676
|
|
| Тема: | Визначення концентрації розчинів методом титрування. | ||
| Мета: | Освоїти метод об’ємного хімічного аналізу – титрування. | ||
| Реактиви: | |||
| Розчини: | - Натрій гідроксид; | ||
| - Сульфатна (сірчана) кислота | |||
| - Хлоридна кислота | |||
| Індикатори: | - Метилоранж. | ||
| Обладнання: | Хімічний штатив з пробірками, бюретки, конічні колби. |
1.1 Методичні вказівки до вивчення теоретичного матеріалу
Більшість хімічних реакцій відбуваються в розчинах при певному оптимальному співвідношенні розчиненої речовини і розчинника.
Звернути увагу на приготування розчинів і на розрахунки, що пов’язані з обчисленням концентрації.
Розрахункові формули для визначення концентрації розчинів
| Спосіб вираження концентрації | позначення | Розрахункова формула | Розмірність |
| Масова доля (процентна)- кількість грамів розчиненої речовини в 100 г розчину | С% | 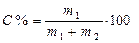
| % |
| Молярність – число молей розчиненої речовини в одному літрі розчину | СМ | 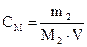
| моль/л |
| Моляльність – число молей розчиненої речовини в 1000 г розчинника | Сm | 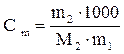
| моль/г |
| Нормальність – число еквівалентів розчиненої речовини в 1 л розчину | СН | 
| екв/л |
| Титр – число грамів розчиненої речовини в 1 мл розчину | Т | 
| г/мл |
1.2 Проведення дослідів
| <== предыдущая лекция | | | следующая лекция ==> |
| ЛАБОРАТОРНА РОБОТА №6 | | | Дослід 1. Визначення нормальної концентрації розчину лугу та його титру методом титрування. |