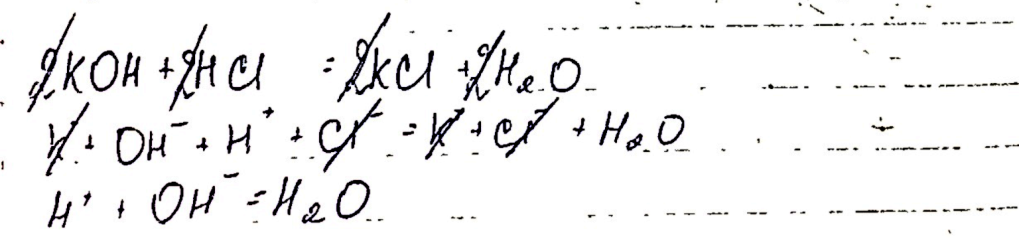Билет №6. 1. Химические реакции. Признаки и условия их протекания
1. Химические реакции. Признаки и условия их протекания. Химические уравнения. Закон сохранения массы веществ. Типы химических реакций. 2. Какой объем газа можно получить при взаимодействии 60г, 12% раствора карбоната калия с серной кислотой. Химическая реакция — превращение одного или нескольких веществ в другое. 1)Реакция соединения – это реакции в результате которых из двух веществ образуется одно более сложное. 2)Реакция разложения - это реакция в результате которых из одного сложного вещества образуется несколько более простых. 3)Реакция замещения – это реакции между простым и сложным веществами, в результате которых образуется новое простое и новое сложное вещество. 4)Реакция обмена – это реакции между двумя сложными веществами, в результате которых они обмениваются своими составными частями. 1)Тесное соприкосновение веществ. Химическое уравнение – это условная запись химической реакции с помощью химических формул и коэфицентов. В основе химических уравнений лежит закон сохранения массы вещества: массы веществ вступивших в реакцию равна массе веществ получившихся в результате реакции. · Изменение окраски · Выделение газа · Выпадение осадка · Выделение тепла и света · Выделение запаха 2.
1. Основные положения Т.Э.Д. – теория электрической диссоциации. 2. Сколько грамм магния, содержащего 8% примесей, может прореагировать с 40г соляной кислоты.
Вещества, растворимые в воде могут диссоциировать, т.е. распадаться на противоположно заряженные ионы.
Кислота – электролит, который диссоциирует на катионы водорода и анион кислотного остатка.
Соли – электролит, который в водном растворе диссоциирует на катионы металла и анионы кислотного остатка.
2.
Билет №8 1. Реакции ионного обмена. 2. Сколько грамм 7% раствора гидроксида натрия должно прореагировать с кремниевой кислотой, чтобы получить 32г силиката натрия.
1. Выпадает осадок. 2. Выделяется газ. 3. Образуется вода. 2.
|