Электролиздің физикалық және энергетикалық негіздері
Электр химиялық ө ндеу негіздері. Электр химиялық ертіндіде ионның қ асиеттерін, қ атты дене мен ерітіндінің арасындағ ы шектің қ ұ былыстары талданады. Ол электролитті пайдалануғ а негізделген. Электролит дегеніміз электролиттік диссоциация нә тижесінде тү зілген иондармен электр тогын ө ткізе алатын ерітінділер мен балқ ымалар. Металл мен жартылай ө ткізгішке қ арағ анда, ерітінділер мен балқ ымалар электролиттері иондық ө ткізгіштікке ие. Молекулалық электролиттік дисоцациялану теориясына сә йкес кейбір заттар, тұ здар, сілтілер, негіздер жә не т.б. полярлы екі қ арсы бірдей заряд иондары бар, олардың арасындағ ы тартылыс кү ші молекулалардың тұ тастығ ын қ амтамасыз етеді. Егер мұ ндай молекулалар еріткіш (су) молекулалардың арасында тұ рса, онда ион арасындағ ы байланыс ә лсірейді. Бұ л жағ дайда жылулық қ озғ алыстан екі молекула соқ тығ ысса, молекулалар ионғ а бө лінеді жә не т.с.с. Олардың диссоциациясы болады, сә йкесінше, электролитті дисоцация дегеніміз заттың ә р тү рлі зарядталғ ан ерітудің немесе балқ ытудың ыдырау ү рдісі. Электролиттің диссоциация ү рдісіне шық қ ан оң жә не теріс иондарының сандары бір біріне тең болады. Оның иондары бір немесе бірнеше электроннан айырылғ ан атом немесе молекулалар, ол теріс иондар бір немесе бірнеше артық электрондары бар атомдар немесе молекулалар. Мысалы: ас тұ зын суда ерітсек, оның молекулары екі ионғ а- Na+ жә не Ce- ыдырайды. Кейде ион жеке атом қ айта кері иондардың жеке молекулағ а бірігу ү рдісі болуы мү мкін. Бұ л екі ү рдістің бір уақ ытта болу нә тижесінде ерітіндіде тү зілген ион мен оғ ан қ осылатын ионның тепе тендігін сақ тап отырады. Егерде электродты ерітіндіге салсақ, жү йеде электрод–электролит тепе тендік жағ дайы орнайды, сонымен қ атар атомдар тобы пайда бола алады. Мысалы: суда мырышты кү кірт қ ышқ ылының екі ионы тү зіледі: оң - Zn+ жә не теріс - So24-. Еріткіштің молекулалардан бір бө лігі диссоциациялануы мү мкін. Электролиттерде диссоциация ү рдісімен металл-ерітінді шекарасы арқ ылы сыртқ ы ток ө тпейді, себебі электрод сыртқ ы электр тізбегіне қ осылғ ан. Электрод–электролит жү йесінде металл мен электролитте бірдей иондар жү реді. Металл кристалл тор тү йінінде, ал электролитте ерітінді молекуласымен байланысқ ан. Ион кристалл тордың тү йінінен электролитке ө ту ү шін энергия жұ мсалу керек, ол металлдан ион шығ ару жұ мысы деп аталады. Ионның электролиттен металлғ а шығ уы ү шін, гидротация энергиясына тең жұ мыс жасауы керек. Электролитке салынғ ан электродтың бетінде кері электр химиялық реакция жү реді:
мұ ндағ ы n - металл білікенттілігі; Men+ - ерітіндідегі ион.
Жалпы жағ дайда ерітіндідегі Men+ ион энергиясымен кристалл торы ыдырайды, Me атом энергиясы тең емес. Ерітінді – металл шегі арқ ылы зарядталғ ан бө лшектер ө теді, электр потенциалының тең дігі анық талады. Кристалл торының иондық байланыс энергиясы гидротация энергиясынан артық, алғ ашқ ы моментте металл иондар ерітіндіден кристалл торына ө теді. Металлдың ішкі қ абатынан артық электродтар шеткі бетіне жақ ындайды, оң иондар терең нен бетіне кө теріліп, қ ос электрлік қ абат тү зеді. Тепе тендік жағ дайында Men кері реакциялар жылдамдығ ына тең, сә йкесінше Ne - атомның тотығ уы жә не Men+ - ионның тотық сыздану жылдамдығ ы. Электролит арқ ылы электр тогының ө туі. Электролитте иондар, молекулалар ретсіз қ озғ алады. Егер де электролитке тү сірілген электродқ а электр тогын қ осса, ретсіз жылу қ озғ алысынан басқ а бағ ытталғ ан ион қ озғ алысы туады. Оң иондар (катиондар) катодқ а, ал теріс (аниондар) –анодқ а бағ ытталғ ан. Сә йкес электродқ а жеткен соң, ион ө зінің зарядын беріп, қ арапайым атом немесе молекулағ а айналады, электродтан бө лінеді немесе электронмен химиялық реакцияғ а тү седі. Сонымен электролиттердегі электр тогы электр ө рісінде бағ ытталғ ан иондар қ озғ алысын береді. Металлдағ ы жә не жартылай ө ткізгіштегі электр тогының ө суі, зат массасының электролиттен тасымалдануы арқ ылы жү реді. Электролит ерітіндісі арқ ылы электр тогының ө туінің арқ ылы электродтан бө лінген зат мө лшері Фарадей заң ымен анық талады:
мұ ндағ ы
Электр химиялық эквибілікент (α) - бір кулон электр ө ткенде электролиттен бө лінген зат мө лшері. Сандық химиялық эквибілікент заты Фарадей саны қ атынасына тең. Фарадей саны (Fф) – бір грамм эквибілікент затта қ ажеті электр кө лемі Fф = 96485Кл/(г*экв) тең. Электролиттегі ү рдістер Ом заң ына бағ ынады. Мұ ны дә лелдеу ү шін электр ө рісінің ә серінен болатын электролиттегі ион қ озғ алысын қ арастырамыз. Ө ріс ә серінен электролитте иондар қ озғ алысы молекулалар кедергісіне ұ шырайды. Бұ л молекулалардың ретсіз қ озғ алысының ә серінен электролит қ ыздырылады. Иондар «бос жү ріс ұ зындығ ы» болмағ андық тан, ортада барлық уақ ытта ә сер етеді. Ионғ а ә сер ететін кедергі кү ші (тұ рақ ты ү йкеліс кү ші) Егер бастапқ ы ион жылдамдығ ы аз болса, онда Fэ кү ші оны арттырады, сонымен бірге ү йкеліс кү ші артады. Бұ л кү штер ион қ озғ алысының барлық уақ ытында тең еседі. Қ озғ алыстың орташа жылдамдығ ын
мұ ндағ ы
Электролит арқ ылы ө тетін ток тығ ыздығ ы:
Теріс жә не оң иондардағ ы токтың тығ ыздығ ын ескерсек, Электролиттегі токтың тығ ыздығ ы j электр тогының кернеуіне пропорционал жә не Ом заң ына сә йкес. Электролит ө ткізгіштігінің ионының концентрациясы Ерітінді мен балқ ымалар электролизі. Электролиттен ток ө ткенде электродтан заттың бө лінуін, сонымен бірге электродтағ ы тотығ у немесе тотық сыздану ү рдістерін, электрон қ осып алу немесе бө ліп шығ аруын электролиз деп атайды. Ө неркә сіпте анодтық металл ерітіндіні мен балқ ыманы катодтық тұ ндыру кезінде электролиз пайдаланылады. Қ алыпты сутегінің электродқ а қ атысты қ алыпты потенциалы электролиз ерітіндісімен (мыс, мырыш) алынады. Қ алыпты потенциалы 1-ден аз металлдар мұ ндай ә діспен алынбайды. Сондық тан ө неркә сіпте бұ л металлдар (литий, калий, алюминий, магний) тұ здарының балқ ымасының электролизі қ олданылады. Егер де электролиз ваннасында электр энергиясы жұ тылатын болса, онда ванна электролиздері деп аталады. Электролиз сұ лбасы 3.23-суретте кө рсетілген.
3.23-сурет. Электролиз қ ондырғ ысының сұ лбасы жә не электродтар арасындағ ы потенциалдардың тарауы
Анодта металлдың металлдық кү йінен (Me0) иондық тү рге ауысуы жү реді, нә тижесінде Электролиз ваннасында кернеуді ү ш қ ұ раушы тү рінде кө реміз: заттың электр химиялық ыдырау кернеуі, электролиттегі анодтық жә не катодтық потенциалдардың тү суі:
мұ ндағ ы U1 - заттың электр химиялық ыдырау кернеуі; Ua , Uk - сә йкесінше анодтық жә не катодтық потенциалдардың тү суі: I - ваннадағ ы ток кү ші;
Электролиз ваннасынан бө лінетін қ уат:
Тек осы қ уаттың (IU1) бө лігі заттың электр химиялық ыдырауына, ал қ алғ аны электролитті қ ыздыру мен иондардың ерітіндіден тасымалына жұ мсалады. Эликтролизден алынғ ан зат мө лшерінің теориялық мү мкіндігіне қ атынасы Фарадей заң ымен анық талады жә не ток бойынша деп аталады Ai, (%):
мұ ндағ ы q1 - іс жү зінде бө лінген зат мө лшері, q2 - фарадей заң ы бойынша электр шығ ынысыз бө лінетін зат мө лшері.
Ток бойынша шығ ын электролиз ү рдісінің ө туінің тиімділігін кө рсетеді. Электролиз ү рдісінің тиімділігі энергия бойынша шығ ынмен де бағ аланады:
мұ ндағ ы
Сонымен энергия бойынша металл шығ ыны 1 Дж жұ мсалғ ан энергиядан салынғ ан грамм бойынша металл мө лшері. Электролиз интевсивтілігін анық тайтын шама электродтық ток тығ ыздығ ы деп аталады, (A/ м2):
мұ ндағ ы J - ток кү ші; S - электродтың электролитке батырылғ ан беті.
Электрод бетінде тү зілген электр қ абаты электродқ а ионның келуін, электродтан ионның шығ уын қ иындатады. Бұ ны бұ зу ү шін электролит циркуляциясы, импульсті кернеумен электролиз ваннасын қ оректендіру, электродты дірілдету (вибрациялау) қ олданылады. Электролит циркуляциясы электрод аймағ ының бұ зылуынан басқ а, электролит ваннасындағ ы температураны тең естіруге мү мкіндік береді. Электролиз ваннасын импульс кернеумен бейтараптау жү реді. Электролиздің ө неркә сіптік ү рдісін жү ргізгенде, теориялық мә ндерін электрод бойынша шығ ару мү мкін емес. Бұ л қ ұ былыс келесі себептермен тү сіндіріледі: ионның қ айта зарядталуы; ә р тү рлі білікентті иондардың электролитте болуы; ионның ө зара немесе электролитпен ә серлесуі; катодтық ө німнің тотық сыздануы. Мыс электролизі. Мыс электролизінің мақ саты шағ ылыстырғ ыш пештерде балқ ытылып алынғ ан қ ара мыстан қ оспаларды тазарту, бірге жү ретін қ ымбат металлдарды шығ ару жә не электролиттік таза мыс алу. Бұ л ү рдісті жә шік тү ріндегі электролиз ваннасында жү ргізеді. Ваннағ а қ ұ йылғ ан қ ара мыс анодтары орнатылады, араларына жұ қ а таза мыс пластинасы қ ойылады, cодан кейін ваннағ а мыс купоросының кедергісін азайту ү шін кү кірт қ ышқ ылы қ осылғ ан сулы ерітіндісі бар электролит қ осылады. Қ ара мыстан қ ұ йылғ ан анодтар тік бұ рышты, қ алың дығ ы 35-45 мм, салмағ ы 300 кг плита тү рінде, катодтар электролиттік мыс 0, 6 - 0, 7 мм жапырақ шадан жасалады. Ваннағ а катод асу ү шін қ ұ лақ ша ілмек ілінеді, кө рші анод пен катод бетінің арақ ашық тығ ы 30 - 40 мм. Ванна арқ ылы тұ рақ ты электр тогын жібергенде қ ара мыс аноды еріп, катодта таза мыс тұ нады. Қ ымбат металлдар мен қ оспалар шлак тү рінде тұ нбағ а, кейбіреуі (никель) ерітіндіге ө теді. Электролиздерде келесі электрхимиялық ү рдістер жү реді:
анодта
катодта
ерітіндіде
Электролиздеу ү рдісі ваннада 0, 3-0, 35 B кернеуде басталады. Токтың тығ ыздығ ы мыс катодында ұ сақ, тығ ыз, ә рі тегіс тұ нба алумен шектеледі. Қ ара мыстың қ ұ рамына байланысты, токтың тығ ыздығ ы 180-270 A/м2 аралық та ауытқ иды. Ток бойынша шығ ын 92-98% қ ұ райды. Таза мыс бойынша электр энергияның меншікті шығ ыны 200-379 кВт·сағ /т. Электролиздеу кезінде ваннаның ә р бө лігіндегі электролиттің иондық концентрациясы ө згеріп отырады. Ол электр энергия бойынша шығ ынды арттырады. Электродта мыс иондарының концентрациясын тең естіру мақ сатында қ ажетті температурамен қ амтамасыз ету ү шін тікелей циркуляцияның кө мегімен ванна тү бінен қ ұ йылып, ү стінен ағ ызылып қ олданылады. Электролиттің температурасы 333±3 К дең гейінде ұ сталады. Электролиттің қ ажетті қ ыздырылуы графит, титан немесе тот баспайтын болаттың жылу алмастырғ ышының кө мегімен жү зеге асады. Электролиз ваннасында электролиздеу жү ргізу ток бойынша ү лкен шығ ынды болдырады, бұ л электр энергиясының шығ ынын азайтып, ө німділікті арттырады. Металлдың ток бойынша шығ ынының азаюы, токтан басқ а тағ ы да басқ а шығ ын кө здері бар екендігін білдіреді, ол электролиз цехында жайсыз жағ дайғ а: қ ышқ ылдық булану артуына; ваннаның ағ аш бө лшектерінің кө терілуіне (ісінуіне); ванна бө лшектерінде тұ з жиналуынв; жерге қ атысты ваннаның потенциалы жоғ арылауына ә келіп соқ тырады. Электролиз қ ондырғ ыларындағ ы токтың артық шығ ындары: а) электролиттің циркуляциялық жолы; б) су мен бу жолы; в) жерден ванна изоляциясы; г) ванна арасындағ ы изоляция; е) электродтардың арасындағ ы қ ысқ а тұ йық талу. Мырыш электролизі. Жоғ ары сапалы мырышты оның тұ здарының сулы ертінділерін электролиздеу жолымен алады. Ваннада алюминий катоды мен қ орғ асын аноды орнатылады. Сосын кү кіртті мырыш қ ышқ ылының ZnSO4 (5-6%) сулы ертіндісімен толтырылады, ол мырыш Zn2+ катионы, 3О аноины жә не H+ катионы мен SO Электролиздеу кезінде катодта металл мырыш, анодта газ тү ріндегі оттегі, ал ертіндіде *** кү кірт қ ышқ ылы тұ нады. Сонымен электролиздерде келесі ү рдістер жү реді:
катодта
анодта
ваннада
Катодта мырыштың тұ нуын қ амтамасыз ету ү шін электролиздеуді жоғ ары ток тығ ыздығ ында (400-600 A/м2 ) жү ргізеді жә не ерітіндіге катодта сутегі бө луіне кедергі ететін беттік активті зат қ ойылады. Электролиз цехтарында қ ышқ ылғ а тө зімді материалдан, яғ ни жиналмалы темір бетоннан ванна жасалады. Ванна ө ң деу мен қ алдық тар ыдысын винипласт атқ арады. Ванна сыртын қ ышқ ылғ а тө зімді баяу, битуммен жабады немесе резең кемен қ аптайды. Ванна тү бінде шлак тү сіретін тесік бар. Ұ зын бортты ванналар қ атар орнатылып, 20-30 ванна блокпен қ осылады. Ток бойынша жақ сы шығ ын алу ү шін, электролит температурасын 308-313 К дең гейінде ұ стау керек. Тә жірибеде ә рбір ваннадағ ы электролитті суыту ү шін алюминий немесе кө мірсутекті ауытқ ыштар қ олданылады. Мырыш ө ң дірісінде ток бойынша мырыш шығ ыны 88-94% қ ұ райды, 1 тонна мырыш ү шін электр энергия шығ ыны 3500 кВт·сағ қ ұ райды. Электролит кедергісі ерітіндідегі мырыш концентрациясы мен температурасын анық тайды. Ваннадағ ы кернеудің бір ө сіп, бір тө мендеуі (3, 3-3, 6 B дейін) анодты тазарту керектігін білдіреді. Анодта тоттануды тө мендету ү шін, 1 % кү міс қ осылғ ан қ орғ асыннан дайындайды. Анодтың қ алың дығ ы 5-8 мм. Катодты жапырақ ты алюминийден 4 мм дайындайды. Алюминий катодынан мырышты тү сіру тә улігіне бір рет немесе екі тә улікте бір рет болады. Оларды жү йелік тазарту ү шін катод тазартқ ыш машинамен 10 кү нде бір рет тазартады. Анодты 20-25 кү нде бір тазартады. Ауыстыру 1 тонна мырышқ а 1, 5 катод, 0, 8-1, 5 кг анод шығ ындалады. Алынғ ан катодты мырыш пластиналарын сумен жуып, пакетке салады да, индукциялы канал пештеріне жібереді. Алюминий электролизінен қ алыпты потенциал 1 В кезінде металл бө лінеді, ерітінді электролизімен катодта бө лу мү мкін емес, себебі негізінен электролиттегі сутегі катодтан жә не анодтан қ оспалар бө леді. Алюминийдің қ алыпты потенциалы 1, 67 В болады, оны ерітілген тұ з электролизінің кө мегімен алады. Бұ л жағ дайда балқ ытылғ ан криолиттегі ( Фторид балқ ымасы кү шті орта, алюминий электролиз кө мір электрод шығ ын береді, ваннаның ішкі беті кө мір плиталы блокпен қ апталады. Алюминий алу ү шін электролиздер келесі белгілер қ атарымен классификацияланады: 1. қ уат (ток кү ші) бойынша: - 40-50 кА - аз қ уатты; - 60-80 кА -орта қ уатты; - 100-160 кА - жоғ ары қ уатты; - 200-250 кА - ө те жоғ ары қ уатты. 2. ток тасымалдану ә дісі бойынша: - жанынан аз жә не орта қ уатты электролиздер; - жоғ арысынан ү лкен қ уатты электролиздер. 3. анодтың қ ұ рылысы бойынша: - ванна жылу есебінен ө здігінен пісетін жә не кү йдірілген болып бө лінеді. Кү йдірілген анод тек жоғ ары дә режеде ток тасымалдануынан болады. Ө здігінен пісетін анод ә р ваннағ а біреуден қ ондырылады. Алюминий алу ү шін электролиз ваннасының арнайы қ ондырғ ысы қ олданылады (3.24-cурет). Тік бұ рышты ванна. Электролиз корпусы болат жапырақ шалардан тү псіз немесе тү пті тү рде жасалуы мү мкін, ванна корпусы, астынан жылу шығ армас ү шін, қ апталады. Оның табанына газ бетон блогы қ ондырылады, арнайы ток ө ткізгіш блюмстер қ ойылады. Кө лденең жақ тары асбестпен жабылып, жылу шығ армас ү шін сазбен қ апталып, кө мір плиталармен футерленеді. Кө мір жабынның барлық тігісі кө міртекті маң ызбен сыланады. Еріген алюминийге магнит ө рісінің ә лсіз ә сер етуіне байланысты ток екі жақ тан ә келінеді.
3.24-cурет. Алюминий алуғ а арналғ ан электролиз ваннасының қ ондырғ ысы
Анодтың мө лшері ваннаның берілген қ уаты мен мү мкін токтың тығ ыздығ ымен анық талады, токтың тығ ыздығ ы орташа қ уатты ваннада - 0, 80-0, 95 A/см2, жоғ ары қ уатты ваннада - 0, 65-0, 7 A/см2 дейін тө мендейді. Кү йдірілген анод 0, 75-1, 0 A/см2 тең ток тығ ыздығ ымен жұ мыс істейді. Ө здігінен пісетін электродтың тиімділігі - электродты тығ ыздау мен ө ртеу шығ ынының аздығ ы. Кемшілігі - электролиз цехындағ ы ә рбір ваннадан улы газдың бө лінуі, жоғ ары кедергі, бояу, электролиттен кө мір қ алдығ ының кө бігін алу керек. Анодты қ озғ алмалы рамағ а іледі. Анодтың тасымалы электролиттегі кернеу жоғ алту функциясымен жү зеге асады. Ваннағ а ток екі жағ ынан алюминий шинасымен ә келінеді, ал анодқ а болат штырьмен (істікпен) ә келінеді. Егер де ток жоғ арыдан келсе, анод штырь мен шина серіппесінің қ ышқ ышымен қ осылады. Электролизердер 160-170 данадан, 4-5 қ оймақ ты біріктіреді. Ванна сериялары екі корпустан екі қ атармен ә рқ айсына орнатылады. Электролиз цехының едені электр оқ шауламамен оқ шауланады. Қ алқ ыма электролизі кезіндегі ваннадағ ы ток 100 кА асады, сондық тан ванналар серияғ а алдын ала қ осылмай тұ рады. Жеке ванналар мен блоктардың ө зара сериясымен, ә рі қ орек кө зіне қ осылу шинасымен жасалады. Қ алыпты жұ мыс кезінде ваннадағ ы кернеу 4, 2-4, 5 В тең, берілген электролит қ ұ рамы мен кө рсеткіш режимін қ олдануғ а болады. Топырақ ты жер жетіспеген жағ дайда (0, 5-1, 5%) анодтық эффект байқ алады. Ваннадағ ы кернеу ақ ырын, кейін кү рт 50-60 В жетеді. Эффект жарық тану, газ бен бу бө ліну, электролит қ ызуымен жалғ асады, бұ л фторлы тұ зды жоғ алтуғ а мен электр энергиясының шығ ынына ә келіп соқ тырады. Бұ л эффектіні электролитке топырақ ты жер қ осу арқ ылы жоюғ а болады. Металлды ваннадан қ ұ йып алу вакуум ожаумен (ковш) жү зеге асады. Қ ұ йып алынғ ан алюминий қ ұ йылғ ан корпусты шиксерге тү седі, онда суытылып, қ алыпқ а қ ұ йылады. Алюминий ө ндірісі энергия сыйымды болып саналады. Алюминий ө ндірісінде электр энергия шығ ыны 14000-16000 кВт·сағ /т. 1 кВт·сағ -қ а металл шығ ыны 60-77 гр, 1 тонна алюминийге жұ мсалатын энергия (16000 Электролиз ө ндірісінің электр қ ондырғ ылары. Электролиз қ ондырғ ыларын тұ рақ ты токпен қ оректендіру генератордан келетін тұ рақ ты ток немесе айнымалы токты ө ндірістік жиілікте тұ рақ ты токқ а тү рлендіретін жартылай ө ткізгіш агрегатпен жү зеге асады. Соның ішінде ең кө п тарағ аны кремнийлі тү зеткіш агрегаттар (ПӘ К 97-99%), айнымалы токты тарату қ ұ рылғ ылар, кернеу реттеу қ ондырғ ысы бар кү штік трансформатор, жартылай ө ткізгіш агрегат, тұ рақ ты токты таратқ ыш қ ондырғ ы мен жеке қ ажеттілік қ ондырғ ысы. Электр қ ондырғ ыларын қ оректендірудің ү ш фазалы кү штік трансформаторлар жоғ ары кернеуде жү ктеме астында жә не екінші орамалардың қ асына орнатылуы мү мкін. Ә рбір екінші орама тү зеткіш фаза санына тә уелді, жартылай ө ткізгіш блогын қ оректендіреді. Электролиз ө ндірісі ү шін кү штік трансформаторды техникалық дамыту, экономикалық арттыру жә не орнату кезінде қ оршағ ан ортағ а улы заттар шығ уын азайтады. Экономикалық факторлар жалпы шығ ын мен энергия шығ ынын азайтады. Қ оршағ ан ортағ а улы заттар бө лінуінің азаюы жаң а суытқ ыш агент (силикон майлары) жә не шу азайюымен жү зеге асады. Кү штік тү зеткіш трансформатордың тө менгі кернеулі орамасын алюминий табақ шадан жасайды, ені магниттік ортаның ұ зындығ ына сә йкес, жоғ ары кернеулі орамасы - алюминий сымынан немесе табақ шалардан жасалады. Реттегіш трансформатор ретінде ү ш фазалы автотрансформатор қ олданылады, кү штік трансформатордың номиналды қ уатына тең кірмелік қ уатқ а есептелген. Автотрансформатор ішінде кернеу ЖАР (жү ктеме астында реттеу) қ ондырғ ысы кө мегімен кернеу реттеу бір қ алыпты Қ А (қ озусыз ауысу) қ ондырғ ысымен бірнеше сатылы тү рде реттеп отырады. Тү зеткіш агрегаттар басқ арылатын жә не басқ арылмайтын вентильмен орындалады. 3.24-суретте басқ арылмайтын вентилді ауыстырғ ыштың кү штік бө лім сұ лбасы кө рсетілген. Кү штік трансформатордың желілік орамасы ү шбұ рышқ а тізбектей жә не параллель Қ А ауыстырғ ыштарымен қ осылады. Екі вентиль орамасы ү шбұ рышша, екеуі - жұ лдызша қ осылғ ан.
3.24-сурет. Басқ арылмайтын вентильді ауыстырғ ыштың кү штік бө лімінің сұ лбасы
3.25-суретте трансформаторлы тү зеткіштің сұ лбасы кө рсетілген. Трансформатор тө рт параллель қ осылғ ан вентиль блогымен алты фазалы кө пір сұ лбасы (Ларионов сұ лбасы) бойынша қ осылғ ан. ДрУ1 мен ДрУ2 тең естіргіш дроссельдерді ток тү зеткіш арасында біркелкі таралуы ү шін орнатылады, себебі ү шбұ рышша орамасындағ ы кернеу жұ лдызша орамасындағ ыдан 1% артық. ДрН1 – ДрН2 қ анығ у дроссельдері кернеуді қ алыпты реттейді. Ә рбір комплект алты фазалы дроссельден қ ұ ралғ ан. Дроссельді ә рбір агрегат ү шін жеке сипаттамамен таң дайды.
|

 , (3.96)
, (3.96) , (3.92)
, (3.92)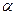 - электр техникалық эквибілікент, г/Кл; I - ток, А;
- электр техникалық эквибілікент, г/Кл; I - ток, А;  - ток ө ту уақ ыты, сек.
- ток ө ту уақ ыты, сек. (К - ү йкеліс коэффициенті) реттелген қ озғ алыс жылдамдығ ының бірінші дә рә жесіне тә уелді. Электрон қ озғ алысының бағ ыты бойынша жер бетінде электр кү ші
(К - ү йкеліс коэффициенті) реттелген қ озғ алыс жылдамдығ ының бірінші дә рә жесіне тә уелді. Электрон қ озғ алысының бағ ыты бойынша жер бетінде электр кү ші  , мұ ндағ ы е – ион заряды.
, мұ ндағ ы е – ион заряды. э, электр кү шінің eE=kv қ атынасынан анық таймыз:
э, электр кү шінің eE=kv қ атынасынан анық таймыз: , (3.93)
, (3.93) - ион қ озғ алтқ ыштығ ы.
- ион қ озғ алтқ ыштығ ы. . (3.94)
. (3.94) -сә йкесінше оң жә не теріс иондар концентрациясы мен қ озғ алтқ ыштығ ы болып саналады.
-сә йкесінше оң жә не теріс иондар концентрациясы мен қ озғ алтқ ыштығ ы болып саналады. қ озғ алтқ ыштың артуымен ө седі. Температура артуымен электролиттің ө кізгіштігі ө седі, қ озғ алтқ ыштың (сұ йық тық тың тұ тқ ырлығ ы азаяды) артуымен диссоциация дә режесі тү сіндіріледі.
қ озғ алтқ ыштың артуымен ө седі. Температура артуымен электролиттің ө кізгіштігі ө седі, қ озғ алтқ ыштың (сұ йық тық тың тұ тқ ырлығ ы азаяды) артуымен диссоциация дә режесі тү сіндіріледі.
 анодтық еру (n - заряд саны) металл электронын береді. Катодта ион электронғ а ие болады жә не металлдық жағ дайғ а
анодтық еру (n - заряд саны) металл электронын береді. Катодта ион электронғ а ие болады жә не металлдық жағ дайғ а  (катодтық тұ ну) ауысу болады.
(катодтық тұ ну) ауысу болады. , (3.95)
, (3.95) - электродтардың арақ ашық тығ ы;
- электродтардың арақ ашық тығ ы;  - электролит ө ткізгіштігі.
- электролит ө ткізгіштігі. . (3.96)
. (3.96) , (3.97)
, (3.97) , (3.98)
, (3.98) , (3.99)
, (3.99) ;
;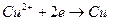 ;
; .
. анионына ыдырайтын H2SO4 диссоциациясын жү ргізеді.
анионына ыдырайтын H2SO4 диссоциациясын жү ргізеді. ;
; ;
; .
. ) алюминий оксид
) алюминий оксид  ерітіндісімен электролит дайындалады.
ерітіндісімен электролит дайындалады.
 500) кВт·сағ.
500) кВт·сағ.



