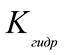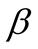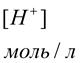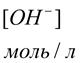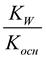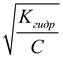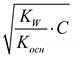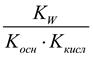Гидролиз солей. Гидролиз – реакция обмена между водой и растворенной в ней солью
Гидролиз – реакция обмена между водой и растворенной в ней солью. Таким образом, гидролиз соли во многом обратен процессу нейтрализации. Процесс гидролиза – обратимый процесс, подчиняющийся принципу Ле Шателье: равновесие в системе смещено в сторону реакции, в результате которой образуются газы, осадки или слабодиссоциированные соединения или сложные ионы. С этой точки зрения гидролизу могут подвергаться только соли, в которых хотя бы один из составляющих ее ионов принадлежал слабому электролиту (основанию или кислоте). Этот ион в растворе связывает противоположный ему по заряду ион из состава воды (Н+ или ОН-), образуя слабо диссоциированную молекулу или сложный ион и сдвигая равновесие H2О↔ Н++ОН-в сторону диссоциации очередной порции Н20. Так, ацетат натрия - соль, содержащая катион сильного основания (NaOH) и анион слабой уксусной кислоты (СНзСООН), сама является сильным электролитом и диссоциирует в воде по схеме: NaCH3COO↔ Na+ + СН3СОО-. Находящиеся в растворе в избытке ионы СН3СОО-связывают в молекулу слабой уксусной кислоты катионы Н+. При этом равновесие диссоциации воды сдвигается в сторону образования новой порции Н+, которые снова связываются ацетат-ионами в уксусную кислоту. Анионы ОН- при этом остаются не связанными, так как основание NaOH полностью диссоциировано в воде. Таким образом ионы ОН- остаются в избытке. То есть водный раствор в результате гидролиза соли, образованной сильным основанием и слабой кислотой, имеет щелочную реакцию (рН> 7). Уравнение реакции гидролиза ацетата натрия: NaCH3COO + НОН↔ СН3СООН+NaOH или в ионной форме:
Количественными оценками гидролиза являются величины степени гидролиза:
где Сгидр и С – концентрации гидролизованных молекул и исходных молекул соли.
Константа гидролиза Kгидри значение pH раствора соли Под величиной Kгидр принято понимать величину, равную произведению константы равновесия процесса гидролиза на равновесную концентрацию воды, которая считается постоянной:
По аналогии с величиной степени диссоциации, степень гидролиза может быть выражена через величину Kгидр и концентрацию раствора соли:
Ниже в таблице приведены формулы для расчета величин Kгидр, равновесных концентраций катионов H+ и анионов OH- и степени гидролиза солей различной природы. KW – ионное произведение воды, Kосн – константа диссоциации основания, Kкисл – константа диссоциации кислоты, С – концентрация соли, моль/л. Таблица 1
Формулы табл. 1 приведены с учетом того, что в справочниках обычно приводятся именно величины констант диссоциации слабых кислот и оснований, а не константы гидролиза солей.
|


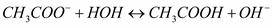 .
. , (3.15)
, (3.15)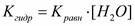 ,
,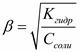 .
.