Свойства комплексных соединений.Устойчивость комплексных соединений в растворе (диссоциация) В растворе комплексные соединения диссоциируют на комплексный ион и ионы внешней сферы. Эта диссоциация протекает практически нацело, по типу диссоциации сильных электролитов и называется первичной: [Co(NH3)6]Cl3 ® [Co(NH3)6]3+ + 3Cl– Лиганды связаны с центральным атомом значительно прочнее и отщепляются в незначительной степени. Этот процесс называется вторичной диссоциацией, подчиняется закону действующих масс и количественно характеризуется константой равновесия, которая характеризует устойчивость комплексных ионов в растворе и называется константой нестойкости комплексов K н: [Co(NH3)6]3+ Co3+ + 6NH3 K н = Диссоциация комплексных ионов всегда протекает по стадиям аналогично диссоциации многоосновных кислот и солей: [Co(NH3)6]3+ [Co(NH3)5]3+ + NH3 K н 1 [Co(NH3)5]3+ [Co(NH3)4]3+ + NH3 K н2 [Co(NH3)4]3+ [Co(NH3)3]3+ + NH3 K н 3 [Co(NH3)3]3+ [Co(NH3)2]3+ + NH3 K н 4 [Co(NH3)2]3+ [Co(NH3)]3+ + NH3 K н 5 [Co(NH3)]3+ Co3+ + NH3 K н 6 Константы K н 1, K н 2, K н 3 ….. K н 6 называются ступенчатыми константами нестойкости. Общая (суммарная) константа нестойкости оценивает общую устойчивость комплексных ионов K н= K н1× K н2× K н3× K н4× K н5× K н6 (табл. 12, также приложение). Таблица 12 Константы нестойкости комплексных ионов
Чем меньше константа нестойкости, тем устойчивее комплексный ион. Величина обратная константе нестойкости называется константой устойчивости: K у =
|

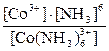
 .
.


