Изомерия комплексных соединений. В химии комплексных соединений изомерия очень распространена
В химии комплексных соединений изомерия очень распространена. Различают ионизационную, гидратную, координационную, геометрическую (пространственную), оптическую и другие виды изомерии. 1. Ионизационная изомерия. Соединения, которые имеют одинаковый состав, но образуют в растворе разные ионы, называют ионизационными изомерами. Примеры: [Co(NH3)5Br]SO4 и [Co(NH3)5SO4]Br красно-фиолетовый красный
[Co(NH3)5Br]SO4 ® [Co(NH3)5Br]2+ + SO [Co(NH3)5SO4]Br ® [Co(NH3)5SO4]+ + Br-
[Co(NH3)5Br]SO4 ¾ ® + AgNO3 ® Ag2SO4 ¯
[Co(NH3)5SO4]Br ¾ ® + AgNO3 ® AgBr ¯
Иногда встречается особый случай ионизационной изомерии, часто называемый гидратной. Например, в трех изомерах CrCl3×6H2O:
1) [Cr(H2O)6]Cl3 – фиолетовый, не теряет воду при высушивании над H2SO4, все ионы Cl– осаждаются ионами Ag+. 2) [Cr(H2O)5Cl]Cl2×H2O – зеленый, теряет одну молекулу Н2О при высушивании над H2SO4, два иона Cl– осаждаются ионами Ag+. 3) [Cr(H2O)4Cl2]Cl×2H2O – зеленый, теряет две молекулы Н2О при высушивании над H2SO4, один ион Cl– осаждается ионами Ag+.
2. Солевая изомерия – наблюдается для лигандов, способных координироваться более чем одним способом. Наиболее известным примером является изомерия нитро- и нитритокомплексов: [Co(NH3)5NO2]2+ – нитроизомер [Co(NH3)5ОNO]2+ – нитритоизомер 3. Координационная изомерия. В соединениях, в которых катион и анион являются комплексными, распределение лигандов может изменяться между двумя координационными сферами: [Cu(NH3)4] [PtCl4] и [Pt(NH3)4] [CuCl4] - изомеры 4.
цис-изомер транс-изомер (оранжевые кристаллы) (желтые, менее растворимые в воде, кристаллы)
|

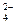
 ® + ВаCl2 ® BaSO4 ¯
® + ВаCl2 ® BaSO4 ¯ Геометрическая изомерия. Разные типы геометрической изомерии обнаруживаются в плоских квадратных и октаэдрических комплексах:
Геометрическая изомерия. Разные типы геометрической изомерии обнаруживаются в плоских квадратных и октаэдрических комплексах:



