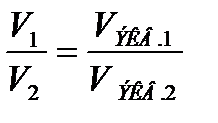Определение числа эквивалентности.
Z (атома элемента в соединении) = степени окисления элемента в веществе (с.о.). Например: Чему равняется число эквивалентности серы в следующих соединениях: 1. H2S; 2. SO2; 3. SO3. Z = с.о. - степень окисления элемента в химическом соединении. с.о.(S) = - 2; Z = 2; 2. с.о.(S) = + 4, Z = 4; 3. с.о.(S) = + 6; Z = 6. Z(кислоты) = основности кислоты в данной реакции, т.е. числу замещенных катионов водорода (nH+) на другие катионы. Z (кислой соли) = числу замещенных катионов водорода (nH+). Z(основания) = кислотности основания в данной реакции, т.е. числу гидроксил ионов (nOH--), замещенных на кислотные остатки. Z(основной соли) = числу гидроксил - ионов (n OH--), замещенных на кислотные остатки. Z(нормальной (средней) соли) = суммарному заряду катиона. Z (вещества, участвующего в ОВР) = числу принятых электронов одним молем окислителя или отданных одним молем восстановителя (ne). Количество вещества эквивалента nЭКВ.(в-ва) – количество вещества, в котором частицами являются эквиваленты. Выражается в молях, как и любое количество вещества. nЭКВ.(в-ва)= m(в-ва) / MЭКВ.(в-ва) [моль] или nЭКВ. (в-ва) = m(в-ва) / mЭКВ.(в-ва) [моль]. Молярный объем эквивалентов газообразного вещества (эквивалентный объем) Широко используется такое понятие, как объем эквивалента газообразного вещества (эквивалентный объем). Это объем, который занимает при нормальных условиях 1моль эквивалентов газообразного вещества. Известно, что один моль любого газа (н.у.) занимает постоянный объем, равный 22,4 л (следствие из закона Авогадро). VЭКВ .– объем одного моль эквивалента газа. VЭКВ.= fЭКВ · VМ(газа) = VМ(газа) / z [л/моль], где VМ(газа) – молярный объем газа, л (н.у.), который равен 22,4 л/моль.
Закон эквивалентов:массы реагирующих веществ, прямо пропорциональны молярным массам эквивалентов этих веществ. На основе закона эквивалентов можно вывести следующие формулы для вычисления эквивалентных масс сложных веществ: Например, для двух компонентной системы:
где m1 и m2 – массы реагирующих веществ; МЭКВ,1 и МЭКВ,2 – молярные массы эквивалентов реагирующих веществ, VЭКВ,1 и VЭКВ,2 – молярные объемы эквивалентов реагирующих веществ. Эквивалентом сложного вещества является такое его количество, которое взаимодействует без остатка с одним эквивалентом любого другого вещества. Такие расчеты возможны благодаря закону эквивалентов. Таблица1
|

 ,
,