Внутренняя энергия идеального газа. Первое начало термодинамики
Первое начало термодинамики
где Q—теплота, сообщенная системе (газу); D U — изменение внутренней энергии системы; А — работа, совершенная системой против внешних сил. Работа расширения газа:
где g =Ср/СV— показатель адиабаты. Уравнения Пуассона, связывающие параметры идеального газа при адиабатическом процессе:
Термический КПД цикла Карно
где Q1 — теплота, полученная рабочим телом от теплоотдатчика (нагревателя); Q2 — теплота, переданная рабочим телом теплоприемнику (холодильнику), T 1 и T 2 — термодинамические температуры теплоотдатчика и теплоприемника. Изменение энтропии при переходе системы из состояния 1 в состояние 2 определяется формулой
где dQ — элементарное количество теплоты, полученное или переданное системе в каком-либо процессе, T — температура системы при этом процессе. Средняя длина свободного пробега молекул газа
где < v > — средняя арифметическая скорость молекул, < z > — среднее число столкновений молекулы в единицу времени, d — эффективный диаметр молекулы, n — число молекул в единице объема (концентрация молекул).
|

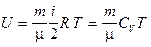 .
. ,
, в общем случае;
в общем случае; при изотермическом процессе;
при изотермическом процессе; при изобарическом процессе;
при изобарическом процессе; при изохорическом процессе;
при изохорическом процессе; при адиабатическом процессе,
при адиабатическом процессе, ,
,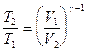 ,
,  ,
, 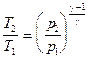 .
. ,
, ,
, ,
,


