Концентрации растворов
Раствором называется гомогенная (однородная) система, состоящая из двух или более компонентов, состав которой может непрерывно изменяться в определенных пределах. По агрегатному состоянию растворы могут быть газообразными, жидкими и твердыми. В растворах выделяют растворитель и растворенное вещество. Растворителем называют компонент, который образует непрерывную среду. остальные компоненты, которые распределены в среде растворителя в виде дискретных частиц, называются растворенными веществами. Состав раствора (концентрация) чаще всего выражается следующими способами. Массовая доля или процентное содержание w – соотношение масс растворенного m в вещества и раствора m р-р, выраженное в долях или процентах.
Концентрация, выраженная в граммах на литр, С г/л – показывает, какая масса растворенного вещества m в, выраженная в граммах, содержится в единице объема раствора V р-р:
Молярная концентрация или молярность, СМ – число молей растворенного вещества n в в одном дм3 (л) раствора:
Моляльная концентрация или моляльность, Сm – число молей растворенного вещества, приходящееся на один килограмм растворителя:
Мольная доля или мольные проценты xi – число молей компонента (растворителя или растворенного вещества) содержащееся в одном моле раствора:
5. Нормальная концентрация или нормальность, CN – количество эквивалентов, n эв растворенного вещества, содержащееся в одном литре раствора:
где z – количество обменных эквивалентов растворенного вещества, содержащееся в одном его моле. Для кислот z соответствует основности кислоты, т. е. числу атомов водорода в составе кислоты, обмениваемых в данной реакции на металл или нейтрализуемых основанием. Для оснований z соответствует кислотности основания, т.е. числу гидроксильных групп в составе основания, обмениваемых на кислотный остаток или нейтрализуемых кислотой. Для солей z рассчитывают как произведение числа атомов и степени окисления металла в составе соли. Для окислителей и восстановителей в окислительно-восстановительных реакциях z – изменение их степени окисления в ходе реакции.
|

 .
.
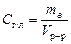 , г/л.
, г/л.
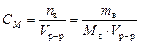 , моль/л.
, моль/л.
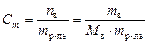 , моль/кг.
, моль/кг.
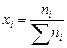 .
.
 , экв/л,
, экв/л,



