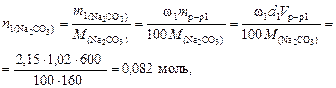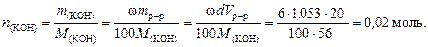Примеры решения задач. Пример 1.Раствор серной кислоты в воде с концентрацией 16 % (мас.) имеет плотность d = 1,109 г/см3
Пример 1. Раствор серной кислоты в воде с концентрацией 16 % (мас.) имеет плотность d = 1,109 г/см3. Выразить концентрацию этого раствора всеми способами. Решение. 1. Выделим мысленно 1 кг раствора и найдем его объем: 2. Найдем массу растворенного вещества (H2SO4) по формуле (34): 3. По формуле (35) вычислим концентрацию раствора серной кислоты в г/л: 4. Найдем количество молей серной кислоты:
5. По формуле (36) вычислим молярную концентрацию раствора серной кислоты:
6. Найдем массу растворителя (Н2О):
7. По формуле (37) вычислим моляльную концентрацию раствора серной кислоты: 8. Найдем количество молей воды:
9. По формуле (38) найдем мольную долю серной кислоты: 10. По формуле (39) определим нормальную концентрацию раствора серной кислоты (для серной кислоты количество обменных эквивалентов в одном моле вещества z = 2):
Пример 2. Какой объем раствора серной кислоты концентрацией 10 % (d = 1,066 г/см3) требуется для приготовления 200 мл 1 н. раствора? Решение. 1. найдем массу серной кислоты, содержащейся в 200 мл 1 н. раствора. Для этого вычислим молярную концентрацию раствора по формуле (39):
2. Подставим найденную массу серной кислоты в уравнение (34) и вычислим объем 10 % раствора
Пример 3. Какой объем воды следует прибавить к 500 мл раствора, содержащего 40 г сульфата никеля, чтобы понизить его концентрацию до 0,05 моль/л? Решение. 1. По уравнению (36) найдем объем 0,05 М раствора (V 2): 2. Найдем объем воды: Пример 4. Найти молярную концентрацию раствора карбоната натрия, полученную при смешивании 600 мл 2,15 % раствора (d = 1,02 /см3) и 200 мл 8,82 % раствора (d = 1,09 г/см3). Решение. 1. Найдем количество вещества карбоната натрия в каждом из смешиваемых растворов:
2. Вычислим молярную концентрацию полученного раствора: Пример 5. Какой объем раствора серной кислоты концентрацией 0,42 моль/л потребуется для нейтрализации 20 мл раствора гидроксида калия концентрацией 6 % (d = 1,053 г/см3)? Решение. 1. Составим уравнение реакции: 2KOH + H2SO4 ® K2SO4 + 2H2O 2. По уравнению (34) найдем количество вещества KOH
3. По уравнению реакции на 2 моль KOH приходится 1 моль Н2SO4, следовательно, для реакции с 0,02 моль гидроксида калия требуется 0,01 моль серной кислоты. 4. По уравнению (36) найдем объем раствора серной кислоты:
|


 .
.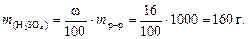





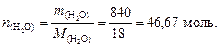
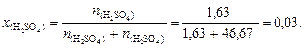
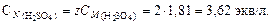
 количество вещества серной кислоты по формуле (36)
количество вещества серной кислоты по формуле (36)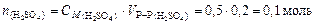 и ее массу
и ее массу  .
.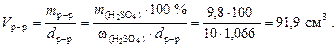
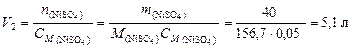 .
. .
.