Решение. 1.Запишем уравнением Менделеева-Клайперона для начального и конечного состояния газа:
1.Запишем уравнением Менделеева-Клайперона для начального и конечного состояния газа:
где М – молярная масса аргона, М = 40 г/моль = 40×10-3 кг/моль; R – молярная газовая постоянная, R = 8,31 Дж/К×моль. 1.Выразим из (1)и (2) массу аргона в начальном и конечном состояниях, учитывая, что V1 = V2 = V:
2.Найдем искомую массу Dm:
3. Осуществим подстановку числовых значений в системе СИ (р1 = = 600кПа = 6×105 Па, р2 = 400 кПа = 4×105 Па, V = 15л = 15×10-3м3) в (4):
Ответ: Dm = 37,54 г. Задача 7. Кислород массой 320 г. нагревают при постоянном давлении от 300 до 310 К. Определить количество теплоты, поглощенное газом, изменение внутренней энергии и работу расширения газа. Решение. 1.Количество теплоты, необходимое для нагревания газа при постоянном давлении, определим из первого начала термодинамики:
где Ср - молярная изобарная теплоемкость, M – молярная масса газа, M = 32 г/моль = 2.Подставляя в (1) числовые значения, получим:
3.Изменение внутренней энергии газа:
5.Работа расширения газа при изобарном процессе:
где 6. Изменение объема газа при расширении можно найти из уравнения Клапейрона-Менделеева. Для двух состояний газа при изобарном процессе имеем:
и тогда вычитая почленно (5) из (4), получим:
7. Подставляя (6) в (3), находим:
А = Ответ: Q = 2910 Дж, U = 2080 Дж, A = 830Дж.
|

 (1)
(1) (2)
(2) (3)
(3)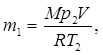 (4)
(4) (4)
(4)
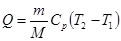 (1)
(1) , где
, где  для кислорода как двухатомного газа;
для кислорода как двухатомного газа; .
.
 . 4.Подставляя числовые значения и учтя, что
. 4.Подставляя числовые значения и учтя, что  , получим:
, получим:
 , (3)
, (3)
 , (4)
, (4) . (5)
. (5) . (6)
. (6) , (7)
, (7)



