Задания. 81-84. В гомогенной газовой системе установилось равновесие
81-84. В гомогенной газовой системе установилось равновесие. Напишите выражение для константы равновесия. Дайте обоснованные ответы на вопросы: а) как и во сколько раз изменится скорость прямой реакции при увеличении давления в системе в два раза; б) как увеличение давления отразится на состоянии равновесия; в) в каком направлении сместится равновесие при увеличении температуры?
85-88. В гетерогенной системе установилось равновесие. Напишите выражение для константы равновесия. Дайте обоснованные ответы на вопросы: а) как уменьшение давления отразится на состоянии равновесия; б) в каком направлении сместится равновесие при уменьшении температуры; в) как и во сколько раз изменится скорость прямой реакции при уменьшении давления в системе в два раза?
89. Напишите выражения для скоростей прямой и обратной реакций и для константы равновесия:
2CO(г) + O2(г)
Как следует изменить в реакционном сосуде: а) температуру; б) давление, чтобы сместить равновесие в прямом направлении?
90. Напишите выражения для скоростей прямой и обратной реакций и константы равновесия:
MgCO3(к)
В каком направлении сместится равновесие: а) по мере накопления в реакторе MgO; б) при увеличении в реакторе давления; в) при увеличении температуры?
91. Напишите выражения для скоростей прямой и обратной реакций:
2NO2(г)
Как изменятся эти скорости: а) при увеличении концентрации NO в три раза; б) при увеличении давления в реакционном сосуде в два раза? Как эти воздействия повлияют на состояние равновесия и величину константы равновесия? Напишите выражение для константы равновесия.
92. Константа равновесия гомогенной системы
N2 + 3H2 = 2NH3
при температуре 400°С равна 0,1. Равновесные концентрации водорода и аммиака соответственно равны 0,2
93. При некоторой температуре равновесие гомогенной системы
2NO + O2 = 2NO2
установилось при следующих концентрациях реагирующих веществ: [NO] = 0,2
|

 2HI
2HI
 2CO2(г); ΔH0 < 0.
2CO2(г); ΔH0 < 0.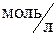 и 0,08
и 0,08 


