Абсорбция диоксида азота
Все оксиды азота, за исключением NO, реагируют с водой с образованием азотной кислоты. Азотистая кислота является малоустойчивым соединением и распадается на азотную кислоту, оксид азота (II) и воду. Абсорбция протекает по схеме: 2NO2 + H2O 3HNO2 Суммарно взаимодействие NO2 с водой можно представить уравнением реакции:
В пограничном слое газ-жидкость происходит переход NO2 в жидкую фазу. Затем после растворения NO2 происходит химическая реакция (3), которая по сравнению с процессом диффузии протекает относительно быстро. Далее в жидкой фазе происходит сравнительно медленное разложение азотистой кислоты по реакции (4). Образующийся NO частично окисляется кислородом в растворе, но большая часть – в газовой фазе. Медленным процессом, определяющим скорость поглощения оксидов азота, является диффузия их в газовую фазу. Степень поглощения диоксида азота водными растворами азотной кислоты определяется такими факторами, как температура, давления, концентрация кислоты. При понижении температуры и концентрации кислоты и повышении давления степень превращения диоксида азота растет. При концентрации азотной кислоты выше 65% поглощение почти прекращается. Также степень превращения NO в NO2 зависит от свободного объема, а количество поглощаемых оксидов азота – от поверхности соприкосновения газа с жидкостью. Поэтому одно из основных требований, предъявляемое к абсорбционной аппаратуре, – создание максимального свободного объема при одновременно сильно развитой поверхности поглощения.
|

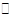 HNO3 + HNO2; кДж(4.7)
HNO3 + HNO2; кДж(4.7)



