Расчеты по химическим формулам и уравнениям химических реакций
Постоянное число Авогадро (N) показывает число молекул в 1 моле вещества. N= Моль – единица количества вещества. n – число молей вещества. M – молярная масса ( V0 - Молярный объем газов при нормальных условиях =22.4 л
Для выполнения заданий используют следующие формулы
Задание 9. Рассчитайте, какое число молекул содержит 5 моль CO2? _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 10. Рассчитайте, сколько весит 1 атом хлора, 1 молекула хлора? _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 11. Чему равен объем 4.4 г СО2 при нормальных условиях? _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 12. Какой объем при нормальных условиях займут 1.5* _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 13. Одинаковое или разное число молекул содержится в 20 г СО2 и 11.2 л Н2S (н.у.)? _________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Задание 14. Определите массу алюминия, который может вытеснить 6.72 л водорода (н.у.) из Н2SO4 _________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Задание 15. Какой объем кислорода расходуется на сжигание 6 г серы? _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 16. Водород, полученный в результате реакции цинка с НСl использовали на восстановление 40 г оксида меди (II). Вычислить массу цинка. _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 17. Растворили в воде 2.3г натрия. Полученная щелочь была использована на реакцию с CuSO4. Вычислить массу осадка. _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 18. Сожгли 5,6л водорода. Вычислить массу калия, который растворится в полученной воде. _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 19. Вычислить массу алюминия, вступившего в реакцию с серной кислотой, если при этом образовалось 0.6 моль водорода. _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 20. Сколько меди выделилось в чистом виде, если на восстановление ее из CuO потрачено 2.24л водорода? _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 21. Какое количество соляной кислоты необходимо для нейтрализации гидроксида натрия массой 20г? _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 22. Сколько литров водорода выделится при взаимодействии 3.9г калия с фосфорной кислотой? _________________________________________________________________________________________________________________________________________________________________________________________________________________________________ Задание 23. Какая масса серы сгорела, если образовалось 112л SO2? _______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Задание 24. Заполните таблицу
Тема 3: Периодический закон и периодическая система Менделеева
|

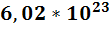
 )
) =n*M
=n*M

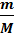
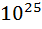 молекул азота?
молекул азота?



