Энтропия и вероятность
Если макросистема находится в неравновесном состоянии, то она самопроизвольно будет переходить в состояние с большей вероятностью – равновесное. Вместе с тем, все самопроизвольные процессы согласно второго закона в замкнутых макросистемах сопровождаются возрастанием энтропии. Поэтому, между S макросистемы в каждом состоянии и вероятностью того же состояния должна существовать определенная связь. Эта связь была найдена Больцманом: Рассмотрим для примера самопроизвольный изотермический процесс расширения газа в вакуум от V1 до V2 , (A=0)
0 V1 V2 V0 Рис.
Найдем вероятности размещения молекул газа в объемах Вероятность одной молекулы находиться в объеме Вероятность всех N молекул находиться в объеме Вероятность всех N молекул находиться в объеме
Приращение энтропии здесь считают по обратимому изотермическому процессу.
Тогда, подставляя сюда отношение объемов из уравнения (*), получим:
 ~ ~ 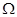 , то , то
Т.е., следует знаменитая формула Больцмана:
Принцип возрастания энтропии со статистической точки зрения привел Больцмана к фундаментальному выводу: все макросистемы стремятся переходить от состояний менее вероятных к состояниям более вероятным. При этом сама энтропия характеризует степень беспорядка в макросистеме: состояниям с большей S соответствует больший беспорядок. С этим связана и необратимость реальных самопроизвольных тепловых процессов: они протекают так, что беспорядок в макросистеме растет. С этим связано и то, что любой вид энергии в итоге переходит во внутреннюю, т. е., в состояние при котором «хаос» максимален. Это состояние называется равновесным, его энтропия S=max, распределение молекул по скоростям будет максвелловским.
[D1]Степень е – (-m(vz)2)/2kT [D2]Степень е – (-m(vz)2)/2kT [D3]Степень е – (-m(vx)2)/2kT [D4]Степень е – (-m(vy)2)/2kT [D5]Степень е – (-mv2)/2kT [D6]Степень е – (-mv2)/2kT [D7]Степень е – (-mv2)/2kT [D8]Степень е – (-mv2)/2kT [D9]Степень е – (-mv2)/2kT [D10]Степень е – (-mv2)/2kT [D11]Степень е – (-mv2)/2kT [D12]Степень е – (-mv2)/2kT [D13]Степень е – (-mv2)/2kT [D14]Степень е – (-mv2)/2kT [D15]Степень е – (-mv2)/2kT [D16]Степень е – (-mv2)/2kT
|

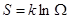
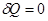 ,
, 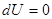 , рис.. Вначале газ находится в объеме V1, он отделен легкой перегородкой, затем ее мгновенно убирают, газ расширяется, но работы не совершает, т.к. ничто ему не препятствует, A=0, Q=0;
, рис.. Вначале газ находится в объеме V1, он отделен легкой перегородкой, затем ее мгновенно убирают, газ расширяется, но работы не совершает, т.к. ничто ему не препятствует, A=0, Q=0; 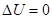 , поскольку, T=const.
, поскольку, T=const.
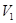 и
и 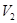 .
.
 , как вероятность независимых событий.
, как вероятность независимых событий.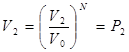 отсюда отношение этих вероятностей:
отсюда отношение этих вероятностей: 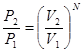 (*)
(*)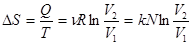 , т.к.
, т.к. 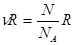
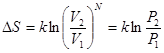
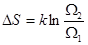
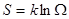 .
.


