Политропный процесс. Расчет процессов базируется на первом и втором началах термодинамики, записанных в дифференциальной форме для одного килограмма термодинамической системы:
Расчет процессов базируется на первом и втором началах термодинамики, записанных в дифференциальной форме для одного килограмма термодинамической системы:
Входящие в эти выражения дифференциалы вычисляются следующим образом:
Кроме того, для идеального газа имеем
На практике чаще всего имеют дело с термодинамическими процессами, в течение которых на каждых малых участках процесса можно с достаточной точностью считать постоянным соотношение между количествами работы и теплоты. Такие процессы называют политропными. Для них
Поскольку для идеального газа
т.е. политропный процесс можно определить как процесс с постоянной теплоемкостью, которая может принимать любые значения, Соотношения между параметрами в политропном процессе можно получить на основании уравнений политропного процесса в переменных
Перенеся слагаемые с
Комплекс (постоянный в случае политропного процесса)
носит название показателя политропы. Имеем, таким образом
Разделяя переменные в этом уравнении и интегрируя, получаем связь между давлением и объемом в политропном процессе:
Получим уравнение политропного процесса в переменных
Откуда Обычно на практике политропный процесс задается не значением теплоемкости c, а значением показателя политропы n, тогда теплоемкость процесса вычисляется как
где величина
|

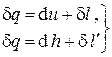 ,
,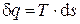 .
.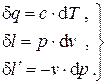
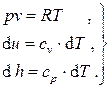

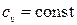 , уравнение политропного процесса может быть записано в виде
, уравнение политропного процесса может быть записано в виде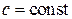 ,
,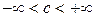 .
.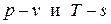 . Используем для этого две формы записи I начала термодинамики:
. Используем для этого две формы записи I начала термодинамики: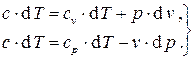
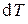 в левые части этих выражений и разделив второе уравнение на первое, получим
в левые части этих выражений и разделив второе уравнение на первое, получим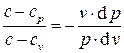 .
.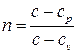
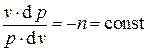 .
.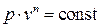 .
.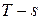 из уравнения для второго закона термодинамики:
из уравнения для второго закона термодинамики: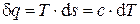 ,
,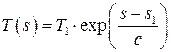 .
.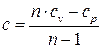 или
или 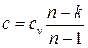 ,
,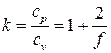 определена ранее.
определена ранее.


