Получение дикарбоновых кислот
При последовательном развитии реакций окисления циклоалканов выход дикарбоновых кислот все более возрастает, и, казалось бы, этим путем кислоты можно получать прямым одностадийным окислением циклоалканов. В действительности же, из-за образования многих побочных продуктов и за счет сгорания в углекислом газе, селективность окисления по целевой дикарбоновой кислоте не превышает 40-50 %, по этой причине в промышленности был реализован двухстадийный процесс – первоначальное окисление циклоалкана воздухом в смесь спирта и кетона и последующее их окисление азотной кислотой в дикарбоновую кислоту. Часто на вторую стадию направляют только спирт, а кетон используют для синтеза лактама. Вторая стадия двухстадийного окисления является одним из важнейших примеров использования азотной кислоты в качестве окислителя; оптимальная концентрация кислоты для этого случая составляет 40-60 %. Спирт вначале окисляется в кетон, а далее протекает нитрозирование, перегруппировка нитросоединений в оксимы, гидролиз последних в кетосоединения и т.д.
Карбоксинитриловая к-та
В результате побочных реакций образуется щавелевая, янтарная и глутаровая кислоты
НООС(СН2)3СООН + СО2
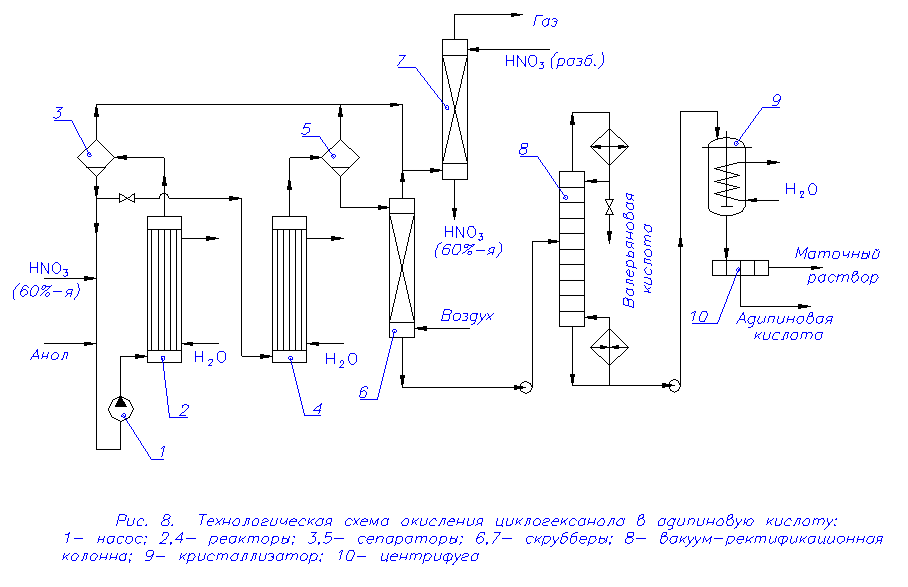
За счет отщепления СО или СО2 на одной из промежуточных стадий получается монокарбоновая (валериановая) кислота С4Н9СООН. Расход азотной кислоты на окисление составляет приблизительно 2,3 моля на 1 моль циклогексанола, причем образуется соответствующее количество оксидов азота. Выход адипиновой кислоты повышается, когда окисление осуществляется в двухтемпературном режиме при 60-800С на первой стадии и при 100-1200С на второй (это объясняется тем, что образование промежуточных продуктов синтеза адипиновой кислоты протекает с более низкой энергией активации, чем для промежуточных стадий получения побочных веществ, в то время как для гидролиза этих веществ в адипиновую кислоту требуется повышенная температура). Положительно влияет также медно-ванадиевый катализатор, добавляемый в виде оксида меди и метаванадата аммония. Медь связывает оксиды азота в комплексы, а ванадиевые соединения ускоряют целевую реакцию и повышают выход адипиновой кислоты до 90-95 %. Такой двухтемпературный процесс осуществляется в двух последовательных реакторах, работающих при разных температурах. При этом первый выполнен в виде аппарата смешения или проточно-циркуляционной установки, так как реакция очень экзотермична и прямой контакт циклогексанола с 60 % азотной кислотой может привести к взрыву. Экономичность процесса во многом зависит от утилизации выделяющихся оксидов азота, которые превращаются в азотную кислоту, сводя ее расход к минимуму. Чтобы улучшить условия абсорбции оксидов азота, окисление ведут при повышенном давлении(0,3-0,5 МПа). Технологическая схема процесса окисления циклогексанола в адипиновую кислоту представлена на рис. 8.
Одностадийное окисление циклогексана в адипиновую кислоту Одностадийный процесс дает значительно лучшие результаты. Окисление циклогексана воздухом осуществляют в растворе уксусной кислоты при температуре 80-1000С в присутствии катализатора (ацетата кобальта) и промотора (ацетальдегида или метилэтилкетона). Роль промотора состоит в том, что получаемая при его окислении перуксусная кислота окисляет Со2+ в Со3+:
СН3СОООН + 2Со2+ + 2Н+ ® СН3СООН +2Со3+ + Н2О
Эта форма катализатора способна к прямому окислению циклогексана или промежуточных продуктов его окисления, которое протекает более селективно, чем обычный радикально-цепной процесс. При 80-90 % степени конверсии циклогексана достигается селективность 70-75 % по адипиновой кислоте. Окисление ведут в барботажной колонне; из реакционной массы затем отгоняют непревращенный циклогексан, уксусную кислоту и образовавшуюся воду. Воду выводят из системы, а циклогексан и уксусную кислоту возвращают на окисление. На следующей установке разделения отгоняют побочные вещества и регенерируют катализатор; адипиновую кислоту направляют на очистку.
|

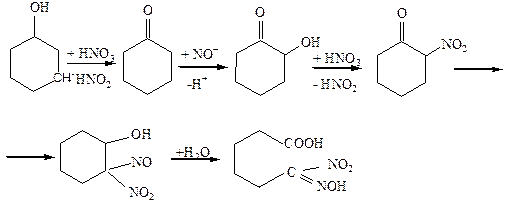
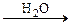 HOOC(CH2)4COOH
HOOC(CH2)4COOH О НООС(СН2)СООН + НООС-СООН
О НООС(СН2)СООН + НООС-СООН