Окисление нафтенов в спирты и кетоны
Окисление нафтенов в смесь спирта и кетона является одним из важных направлений переработки этих углеводородов. Ее можно осуществить воздухом в жидкой фазе при температуре 120-2000С – термически или в присутствии катализатора под давлением, обеспечивающим сохранение реакционной смеси в жидком состоянии. Обычное соотношение образующихся спирта и кетона составляет 2:3, но кроме них в продуктах реакции находится гидропероксид, гликоли, кетоспирты, дикетоны, карбоновые кислоты, лактоны и сложные эфиры. Содержание гидропероксида растет с увеличением размера цикла, при снижении температуры и концентрации катализатора. Каталитическое окисление
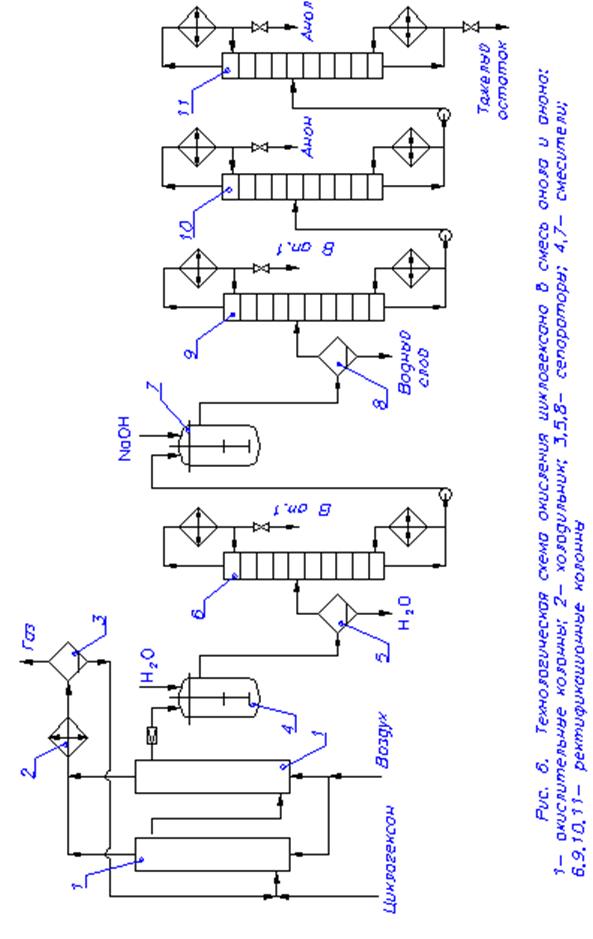
Каталитическое окисление дает лучшие результаты при окислении нафтенов С5-С6 и этим путем из циклогексана получают циклогексанол и циклогексанон. В качестве катализатора наиболее эффективны соли кобальта при температуре 120-1600С и давлении 1,0-2,0 МПа. Селективность по смеси спирта и кетона очень сильно зависит от степени конверсии циклогексана и последнюю приходится поддерживать на уровне 4-5 %, чтобы получить в конечном счете выход анола и анона 80 %. По этой же причине окисление ведут в каскаде из 3-х барботажных колонн. Технологическая схема окисления циклогексана в смесь анола и анона представлена на рис.6.
Термическое окисление циклоалканов в присутствии борной кислоты
Рассмотренный ранее способ каталитического окисления циклоалканов характеризуется малой селективностью даже при низкой конверсии сырья. Этот недостаток имеет особенно важное значение при окислении циклоалканов С8 и С12, когда каталитическое окисление идет еще менее селективно, а исходные углеводороды являются более дорогими по сравнению с циклогексаном. Поэтому предлагается окислять циклоалканы до гидропероксидов с разложением последних щелочью до смеси спирта с кетоном. Еще более эффективным оказался другой способ – термическое окисление воздухом обедненным кислородом (до концентрации 3-4 % кислорода). Эти условия способствуют преимущественно образованию спирта по сравнению с кетоном, а если проводить процесс в присутствии борной кислоты, то последняя связывает спирты в эфиры:
Н3ВО3 + 3ROH «B(OR)3 + 3H2O,
которые дальше не окисляются. Этим путем в значительной степени предотвращается более глубокое окисление и даже при сравнительно большой степени конверсии достигается относительно высокая селективность: при окислении циклододенана при a = 30-35 %, селективность по смеси спирта и кетона достигает 90 %, соотношение спирта и кетона равно 9:1. Недостатком этого процесса является наличие дополнительных установок по рециркуляции борной кислоты, так как она находится в твердом состоянии и это затрудняет транспортирование потоков и непрерывное осуществление процесса. Технологическая схема окисления циклододекана в присутствии борной кислоты представлена на рис.7.
Рис.7. Технологическая схема окисления циклододекана в присутствии борной кислоты: 1 – смеситель; 2 – окислительная колонна; 3 – хоодильник; 4 – ректификационная колонна; 5 – гидролизер; 6 – сепаратор; 7 – узел регенерации борной кислоты; 8 – кипятильник; 9 – циркуляционный компрессор; 10 – насос.
|