Влияние растворителя
Очевидно, что для реакций SN1, чем выше полярность растворителя, тем выше скорость реакции замещения (для нейтральных субстратов). Если же субстрат несёт положительный заряд, наблюдается обратная зависимость — повышение полярности растворителя замедляет реакцию. Сравнивая протонные и апротонные растворители, следует отметить, что если растворитель способен образовывать водородную связь с уходящей группой, он увеличивает скорость для нейтральных субстратов. Для реакций SN2 влияние растворителя оценить сложнее. Если в переходном состоянии заряд распределён аналогично исходному состоянию или снижен, апротонные полярные растворители замедляют реакцию. Если такой заряд возникает только в переходном состоянии, полярные растворители реакцию ускоряют. Протонные полярные растворители способны образовывать связь с анионами, что затрудняет протекание реакции. На скорость реакции в апротонных растворителях также оказывает влияние и размер атакующего атома: малые атомы обладают большей нуклеофильностью. Обобщая сказанное, можно эмпирически отметить: для большинства субстратов при увеличении полярности растворителя скорость SN1 реакций растёт, а SN2 — снижается. Иногда оценивают влияние растворителя рассматривая его ионизирующую силу (Y), используя уравнение Уинстейна-Грюнвальда (1948 год).
где:
Значение Y для некоторых растворителей[9]: вода: 3,493; муравьиная кислота: 2,054; метанол: −1,090; этанол (100 %): −2,033; диметилформамид: −3,500Существует и альтернативный I -параметр, введённый в 1969 году Другаром и Декрооком. Он аналогичен Y -фактору, но в качестве снандарта была выбрана SN2 реакция между три- н -пропиламином и йодистым метилом при 20°С.
Список литературы: 1. Mарч Дж. Органическая химия, пер. с англ., т. 2, — M.: Мир, 1988 2. Ненайденко В. Г. Алифатическое нуклеофильное замещение 2013. 3. Химическая энциклопедия./ Нуклеофильные реакции. // Главный редактор И. Л. Кнунянц. — М.: «Советская энциклопедия», 1988 год. — Т. 3. 4. Травень В. Ф. Органическая химия, М.: ИКЦ «Академкнига», 2004.
|


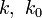 — константы скорости сольволиза стандартного субстрата (в качестве стандарта используется трет -бутихлорид) в заданном и стандартном растворителе (в качестве стандарта используется 80 % об. этанол).
— константы скорости сольволиза стандартного субстрата (в качестве стандарта используется трет -бутихлорид) в заданном и стандартном растворителе (в качестве стандарта используется 80 % об. этанол). — параметр чувствительности субстрата к ионизирующей силе растворителя.
— параметр чувствительности субстрата к ионизирующей силе растворителя.


