МОНОХРОМАТОРЫ
Монохроматор (моно- + chroma, chromatos цвет) — прибор для выделения оптического излучения в узком интервале длин волн; применяется при некоторых видах лабораторных исследований.
Монохроматор – это спектральный прибор для выделения узких участков спектра оптического излучения. Монохроматор состоит (рис. 14) из входной щели 1, освещаемой источником излучения, коллиматора 2, диспергирующего элемента 3, фокусирующего объектива 4 и выходной щели 5. Диспергирующий элемент пространственно разделяет лучи разных длин волн l, направляя их под разными углами υ, и в фокальной плоскости объектива 4 образуется спектр – совокупность изображений входной щели в лучах всех длин
Рис. 14. Общая схема монохроматора: 1 - входная щель, освещаемая источником излучения; 2 - входной коллиматор; 3 - диспергирующий элемент; 4 - фокусирующий объектив выходного коллиматора; 5 - выходная щель. Диспергирующими элементами монохроматора служат дисперсионные призмы и дифракционные решетки. Их угловая дисперсия D = ∆φ/∆λ вместе с фокусным расстоянием f объектива 4 определяют линейную дисперсию ∆l/∆f = Df (∆φ - угловая разность направлений лучей, длины волн которых отличаются на ∆λ; ∆l – расстояние в плоскости выходной щели, разделяющее эти лучи). До недавнего времени призмы были дешевле решеток в изготовлении, они обладают большой дисперсией в УФ-области. Однако их дисперсия существенно уменьшается с ростом λ, и для разных областей спектра нужны призмы из разных материалов. Решетки свободны от этих недостатков, имеют постоянную высокую дисперсию во всем оптическом диапазоне и при заданном пределе разрешения позволяют построить монохроматор с существенно большим выходящим световым потоком, чем призменный монохроматор. Основными характеристиками монохроматора являются: предел разрешения dl, т. е. наименьшая разность длин волн, еще различимая в выходном излучении монохроматора, либо его разрешающая способность R, определяемая, как и для любого другого спектрального прибора, отношением λ/dλ.
Рис. 15. Монохроматор Эберта (z-образная симметричная схема): 1- входная щель, 2 - сферическое зеркало, 3 - дифракционная решетка, 4 – выходная щель. Из большого количества существующих оптических схем благодаря небольшим габаритам при хороших спектральных характеристиках широкое распространение получили монохроматоры с дифракционной решеткой, изготовленные по схеме Черни – Тернера (рис. 16). Преимущество этой схемы перед монохроматором Эберта заключается в том, что отпадает необходимость в большом вогнутом зеркале 2 (рис. 15), которое заменяется на два зеркала меньшего размера.
18. Опишите устройство «горелки» индуктивно связанной аргоновой плазмы при ИСП-АСЭ Плазма формируется в горелке (Рис. 3) за счет поглощения рабочим газом (аргоном), высокочастотного (ВЧ) электромагнитного излучения от индуктора, присоединенного к ВЧ-генератору. Горелка изготавливается из тугоплавкого материала – кварца. Через один из газовых штуцеров в пространство между корпусом и центральной трубкой (инжектором) горелки подается плазмообразующий газ (охлаждающий газ, plasma gas, cool gas). Его расход составляет 12-14 л/мин. Профиль газового потока таков, что последний не дает плазме касаться стенок горелки. В пространство между промежуточной трубкой и инжектором подается вспомогательный поток аргона, назначение которого предотвратить контакт плазмы с торцевой частью инжектора. Расход вспомогательного газа составляет 0,7–1,5 л/мин. В инжектор подается аэрозоль из распылителя. Средний расход газа через пневматический распылитель составляет 0,8–1,2 л/мин.
Рис. 3. Схематическое изображение плазменной горелки в разрезе.
Наивысшая температура достигается в тороидальной зоне внутри индуктора. Температура в центральном канале плазмы, в который поступает аэрозоль образца, изменяется по длине факела от 8000 К до примерно 6900 K в зоне, из которой происходит отбор ионов.
Рис. 4. Распределение температур в факеле индуктивно связанной плазмы.
19. Атомно-эмиссионнная фотометрия пламени: особенности используемого горючего газа, применение. Основными критериями предъявляемые к газу-плазмообразователю является высокая инертность и высокое сродство к электрону. Инертные газы остаются химически неактивными при очень высокой температуре, находясь в состоянии равновесной плазмы, из-за стремления ионизированного атома газа заполнить внешнюю молекулярную орбиталь. Не менее важным показателем является энергия возбуждения плазмообразующего газа, и возможность его бесконтактной ионизации.
20. ПЛАМЕННАЯ АТОМНАЯ АБСОРБЦИЯ – обеспечивает относительно высокую скорость обработки проб при анализе большого количества образцов на ограниченное число элементов. Типичное определение одного элемента требует приблизительно от 3 до 10 секунд. Однако, пламенный АА-анализ требует специфические источники света и соответствующие параметры для каждого определяемого элемента, а также для разных элементов могут понадобиться разные газы. В результате, хотя он и часто применяется для многоэлементного анализа, пламенный атомно-абсорбционный метод обычно рассматривают как одноэлементный метод. Электротермическая атомная абсорбция – как и пламенный АА анализ, по существу является одноэлементным методом. Так как перед атомизацией образец нужно нагревать по определенной температурной программе для удаления растворителя и матрицы, метод ЭТААС имеет сравнительно низкую производительность. При анализе в графитовой кювете определение одного элемента в одном образце обычно занимает 2-3 минуты. Очень прост, широко распространен, доступна обширная информация по приложениям, относительно недорог.
21 АТОМНО-ФЛУОРЕСЦЕНТНЫЙ АНАЛИЗ (атомно-флуоресцентная спектрометрия), метод количественного элементного анализа по атомным спектрам флуоресценции. Пробу анализируемого вещества превращают в атомный пар и облучают для возбуждения флуоресценции таким излучением, которое поглощают атомы только определяемого элемента (длина волны излучения соответствует энергии электронных переходов этих атомов). Часть возбужденных атомов излучает свет – аналитический сигнал, регистрируемый спектрофотометрами. Обычно используют резонансную флуоресценцию, при которой длины волн поглощенного и излученного света одинаковы. Для атомизации растворов применяют пламена, индуктивно связанную плазму или электротермические атомизаторы (нагреваемые электрическим током графитовые трубки, нити, стержни, тигли). Атомизацию порошкообразных проб осуществляют в графитовых тиглях или капсулах, которые иногда вносят в пламя для дополнительного нагрева паров пробы. Химический состав пламени выбирают так, чтобы выход флуоресценции (т. е. доля поглощенной энергии, излучаемой в виде флуоресценции) и степень атомизации были максимальны. С целью увеличения выхода электротермические атомизаторы обычно помещают в атмосферу аргона. Для возбуждения флуоресценции используют интенсивные лампы с линейчатым или непрерывным спектром, а также лазеры с перестраиваемой длиной волны. Рентгеновская спектроскопия, раздел спектроскопии, изучающий спектры испускания (эмиссионные) и поглощения (абсорбционные) рентгеновского излучения, т.е. электромагнитные излучения в области длин волн 10-2-102 нм. Рентгеновскую спектроскопию используют для изучения природы химических связей и количественного анализа веществ (рентгеновский спектральный анализ). С помощью рентгеновской спектроскопии можно исследовать все элементы (начиная с Li) в соединениях, находящихся в любом агрегатном состоянии. Рентгеновские спектры обусловлены переходами электронов внутренних оболочек атомов. Различают тормозное и характеристическое рентгеновское излучение. Первое возникает при торможении заряженных частиц (электронов), бомбардирующих мишень в рентгеновских трубках, и имеет сплошной спектр. Характеристическое излучение испускают атомы мишени при столкновении с электронами (первичное излучение) или с рентгеновскими фотонами (вторичное, или флуоресцентное, излучение). В результате этих столкновений с одной из внутренней (К-, L- или М-) оболочек атома вылетает электрон и образуется вакансия, которую заполняет электрон с другой (внутренней или внешней) оболочки. При этом атом испускает квант рентгеновского излучения, который регистрируется и определяется его энергия, говорящая о типе перехода электрона и агрегатном состоянии вещества.
|

 волн, испускаемых источником. Нужный участок спектра совмещают с выходной щелью поворотом диспергирующего элемента; изменяя ширину щели 5, изменяют спектральную ширину dl выделенного участка.
волн, испускаемых источником. Нужный участок спектра совмещают с выходной щелью поворотом диспергирующего элемента; изменяя ширину щели 5, изменяют спектральную ширину dl выделенного участка.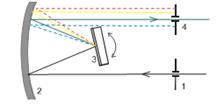 Объективы монохроматоров (коллиматорный и фокусирующий) могут быть линзовыми или зеркальными. Зеркальные объективы пригодны в более широком спектральном диапазоне, чем линзовые, и, в отличие от последних, не требуют перефокусировки при переходе от одного выделяемого участка спектра к другому, что особенно удобно для ИК- и УФ-областей спектра.
Объективы монохроматоров (коллиматорный и фокусирующий) могут быть линзовыми или зеркальными. Зеркальные объективы пригодны в более широком спектральном диапазоне, чем линзовые, и, в отличие от последних, не требуют перефокусировки при переходе от одного выделяемого участка спектра к другому, что особенно удобно для ИК- и УФ-областей спектра.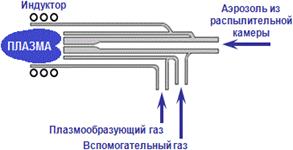 Горелка, помещается соплом в индуктор, представляющий собой 2–3 витка металлической трубки. На индуктор подается напряжение высокой частоты, составляющей 27,12 или 47,60 МГц, в зависимости от производителя прибора. Мощность, подаваемая на индуктор в стандартном режиме, составляет 1,2-1,5 кВт. Аргон, протекающий через горелку, поглощает электромагнитное излучение и ионизируется, вследствие чего возникает плазменный разряд. В качестве первичного источника ионизации выступает искровой разряд, который поджигает плазму.
Горелка, помещается соплом в индуктор, представляющий собой 2–3 витка металлической трубки. На индуктор подается напряжение высокой частоты, составляющей 27,12 или 47,60 МГц, в зависимости от производителя прибора. Мощность, подаваемая на индуктор в стандартном режиме, составляет 1,2-1,5 кВт. Аргон, протекающий через горелку, поглощает электромагнитное излучение и ионизируется, вследствие чего возникает плазменный разряд. В качестве первичного источника ионизации выступает искровой разряд, который поджигает плазму. Как и в обычном газовом факеле, температура в различных участках плазмы различается (Рис. 4).
Как и в обычном газовом факеле, температура в различных участках плазмы различается (Рис. 4).


