Общие сведения. 3.1 Аналитические реакции катиона свинца 5
Содержание. 1. Общие сведения 3 2. Получение 4 3. Качественный анализ 5 3.1 Аналитические реакции катиона свинца 5 3.2 Аналитические реакции нитрат-иона 6 4. Количественный анализ 8 5. Инструментальный анализ 10 5.1 Потенциометрическое титрование 10 5.2 Виды потенциометрического титрования 10 5.2.1. Кислотно-основное титрование 10 5.2.2. Комплексонометрическое титрование 11 5.2.3. Титрование по методу осаждения 11 5.2.4. Окислительно-восстановительное титрование 12 6. Применение 13 7. Список использованной литературы 14 Общие сведения. Формула: Pb(NO3)2 СВИНЦА НИТРАТ Pb(NO3)2, бесцв. кристаллы кубич. сингонии (а = 0,784 нм, z = 4, пространств. группа Ра3); плотн. 4,538 г/см3;
|

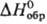 -451,75 кДж/моль;
-451,75 кДж/моль; 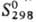 217,9 Дж/(моль·К). При нагр. выше 200 °С начинает разлагаться без плавления с выделением NО2 и О2 и последоват. образованием оксонитратов Pb(NO3)2 · 2РbО, Pb(NO3)2 x x 5РbО и оксида РbО при 500-550 °С. Р-римость в воде (г в 100 г):45,5 (10°С), 58,5 (25°С), 91,6 (60°С) и 116,4 (80°С). Хорошо раств. в гидразине, аммиаке, пиридине и форма-миде, не раств. вэтаноле, ацетоне и неполярных р-рителях. В водных р-рах диссоциирован, при избытке ионов NO3-образует нитратокомплексы [Pb(NO3)3]-, [Pb(NO3)4]2- и [Pb(NO3)6]4-. Степень гидролиза свинца нитрата в р-ре составляет 0,05-0,15.
217,9 Дж/(моль·К). При нагр. выше 200 °С начинает разлагаться без плавления с выделением NО2 и О2 и последоват. образованием оксонитратов Pb(NO3)2 · 2РbО, Pb(NO3)2 x x 5РbО и оксида РbО при 500-550 °С. Р-римость в воде (г в 100 г):45,5 (10°С), 58,5 (25°С), 91,6 (60°С) и 116,4 (80°С). Хорошо раств. в гидразине, аммиаке, пиридине и форма-миде, не раств. вэтаноле, ацетоне и неполярных р-рителях. В водных р-рах диссоциирован, при избытке ионов NO3-образует нитратокомплексы [Pb(NO3)3]-, [Pb(NO3)4]2- и [Pb(NO3)6]4-. Степень гидролиза свинца нитрата в р-ре составляет 0,05-0,15.


