Расчет условий существования нитридов, гидридов и оксидов в многокомпонентных расплавах
Пример 10.1. Определить минимальную концентрацию титана, при которой образуются нитриды титана (TiN) в расплаве Fe—Ti—N при 1873 К и рN2 =1 атм. Коэффициент активности титана в разбавленном растворе железа при 1600 °С равен g
Решение
Запишем уравнение реакции образования нитрида титана: Tiж + 1/2N2(г) = TiN; DG lg K = lg xTi = - lgK - lgg Пример 10.2. Определить концентрацию циркония, при которой образуются нитриды циркония при 1873 К и рN2 =1 атм.
Решение
Zr(т) + 1/2N2(г) = ZrN(т); DG0 = - 351800 + 91,29T; Zr(ж) = Zr(т); DG0 = -16736 + 7,883Т; [Zr](1%) = Zr(ж); DG = 80330 + 34,9T. ______ [Zr](1%) + 1/2N2(г) = ZrN(т); DG0 = - 288206 + 134,073T lgK = При 1873К lgK = 15057/ 1873 – 7,004 = 1.03, fZr =1, lg[%Zr]= –lgK = -1,03; [Zr] =0,093%. Пример 10.3. Определим, возможно ли образование гидридов церия в стали до ее затвердевания (при концентрации церия 0,1%, или xсе = 4×10-4):[Се] + Н2(г) = СеН2(конд); DG° = – 206500 + 148,7×T Дж.
Решение
Вычислим равновесное давление водорода, необходимое для выпадения гидридов, и сравним его с фактическим рH2: LgK = l/ (xce× рH2) = - (DG0/2,3×RT) = – [72570/(19,14×1873)] = –2,0; К= 10-2; рH2 = 1/ (K×xce) = l/ (10-2 × 4×10-4) = 2,5×105 атм. Поскольку равновесное давление существенно превышает реальные значения рH2, наблюдаемые на практике, то гидрид церия образовываться не будет.
|

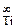 = 0,037 (стандартное состояние—чистый жидкий титан).
= 0,037 (стандартное состояние—чистый жидкий титан). = - 135140 Дж;
= - 135140 Дж;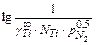 =
= 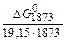 =
=  = 3,76;
= 3,76; = - 3,76 - lg 0,037; xTi = 3×10-3; [Ti] = 0,29%.
= - 3,76 - lg 0,037; xTi = 3×10-3; [Ti] = 0,29%.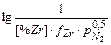 = 15057/ T – 7,004.
= 15057/ T – 7,004.


