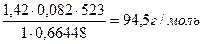Решение. Определим молярную массу вещества А, исходя из уравнения Менделеева-Клапейрона: , если R=8,31,
Определим молярную массу вещества А, исходя из уравнения Менделеева-Клапейрона:
Или, если R=1,22,4/273=0,082 атм л/К, М= Вещество А содержит углерод, водород, кислород и еще какой-то элемент или какие-то элементы (суммарный % углерода, водорода и кислорода <100). Определим соотношение углерода, водорода и кислорода в веществе А. С:Н:О=25,41/12:3,198/1:33,847/16=26362, т.е. простейшая формула вещества А С2Н3О2Хn. На долю С,Н и О приходится 37,545% или 37,545∙94,5/100=35,5 г. Эта величина соответствует молярной массе атома хлора, т.е. в первом приближении простейшая формула вещества может быть С2Н3О2Cl. Молярная масса С2Н3О2Cl равна 94,5 г/моль, что совпадает с молярной массой вещества А. Следовательно, истинная формула А совпадает с простейшей формулой. При реакции с цинком вещество А выделяет водород, что характерно для реакции кислот. Для соединения С2Н3О2Cl такой кислотой может быть хлоруксусная кислота: Cl-СН2-СООН. Подтвердим наш вывод расчетами. 2 ClСН2СООН + Zn→Н2↑+ Zn(ОСОСН2Сl)2 Согласно этому уравнению 1,42 г (0,015 моль) хлоруксусной кислоты образуют при н.у. 0,015∙22,4/2=0,1683 л = 168,0 мл водорода, что соответствует условию задачи. Следовательно, формула вещества А установлена правильно. Увеличение массы А при понижении температуры объясняется частичной димеризацией хлоруксусной кислоты. М∙2=189 г/моль.
|

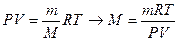 , если R=8,31,
, если R=8,31,