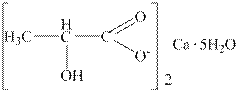
Кальция лактат (Calcii lactas)
С6H10CaO6×5H2O Mr 308,2
Кальция лактат служит источником ионов кальция, используется как противоаллергическое средство, применяется при кровотечениях, отравлениях солями магния, щавелевой и фтороводородной кислотами, и их солями оксалатами и фторидами. Описание. Кальция лактат представляет собой белый мелкокристаллический порошок, почти без запаха, на воздухе выветривается. Мало растворим в холодной воде, легко растворим в горячей воде, очень мало растворим в спирте, эфире, хлороформе. Определение подлинности проводят по аниону молочной кислоты и иону кальция. 1. Реакции на ион кальция: 1.1. С оксалатом аммония образуется осадок оксалата кальция, нерастворимый в уксусной кислоте, но растворимый в хлороводородной кислоте: Ca2+ + (NH4)2C2O4 ® CaC2O4¯ + NH4+ Белый 1.2. С раствором калия гексацианоферрата(II) в присутствии хлорида аммония образуется кристаллический осадок: Ca2+ + 2NH4+ + [Fe(CN)6]4- ® Сa(NH4)2[Fe(CN)6]¯ Белый 2. Реакции на анион молочной кислоты (лактат):
· Субстанцию кальция лактата растворяют в горячей воде, подкисляют разведенной серной кислотой, добавляют перманганат калия до красно-фиолетового окрашивания и нагревают. Появляется запах ацетальдегида и происходит обесцвечивание раствора: 5[CH3CH(OH)COO]2Ca + 4KMnO4 + 11H2SO4 ® 10CH3CHO + 2K2SO4 + 4MnSO4 + 10CO2+ 5CaSO4 +16H2O Оценка чистоты. В субстанции кальция лактата допустимыми примесями являются: хлориды, сульфаты, ионы натрия, железа, тяжёлых металлов, восстанавливающих веществ. Недопустимыми примесями являются ионы бария, летучие жирные кислоты (после нагревания с фосфорной кислотой не должно быть постороннего запаха). Потеря в массе при высушивании не более 22-27%. Определение проводят для навески массой 0,5 г при высушивании при 125 °C в течение 3 ч.
Количественное определение проводят методом комплексонометрического титрования. Титрант – раствор ЭДТА. Индикатор – кислотный хром темно-синий. Титруют до сине-фиолетового окрашивания.
|