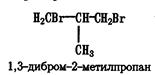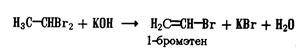Галогенопроизводные алифатических углеводородов
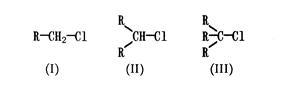
Галогенопроизводными (галогеналкилами) называют органические соединения, в молекулах которых один или несколько атомов водорода замещены на галогены (хлор, бром, йод, фтор). Атом галогена может быть связан с первичным, вторичным и третичным углеродным атомом. Поэтому галогеналкилы делятся на первичные, вторичные и третичные.
Номенклатура и изомерия По систематической номенклатуре название галогенопроизводного складывается из названия углеводорода и галогена с добавлением цифры, обозначающей его место в главной цепи.
Изомерия галогенопроизводных зависит от двух факторов: от строения углеродной цепи и от положения в ней галогена. Поэтому число изомеров у них намного больше, чем у соответствующих им углеводородов. Например, изомерия галогенопроизводных начинается с третьего члена гомологического ряда — пропана (у парафинов, как известно, с бутана). При замещении в нем атома водорода на галоген можно получить два изомерных галогенопроизводных: Для галогеналкиленов по систематической номенклатуре необходимо указывать цифрой не только положение атома галогена в углеводородной цепи, но и положение двойной связи, отдавая ей предпочтение при нумерации.
Способы получения 1. Из алканов реакцией последовательного замещения атомов водорода на атомы галогена:
2. Из алкенов присоединением к ним галогенов или галогеноводородов:
пропен 2-хлорпропан
Этен 1,2-дибромэтан 3. Замещение гидроксильной группы спиртов на галоген.
(Для замещения также используют галогениды фосфора - PCl3, PCl5, POCl3, PBr3, PBr5,- и SOCl2) 4. Взаимодействие дигалогенпроизводных со спиртовым раствором щелочи
Физические свойства Физические свойства моногалогенопроизводных определяются природой атомов галогена и строением углеводородного радикала. Низшие и средние галогеналкилы при обычных условиях – газообразные вещества или бесцветные жидкости с характерным запахом, а высшие – твердые вещества, окрашенные в желтый цвет. С увеличением массы радикала и связанного с ним галогена температуры кипения галогенопроизводных повышаются. Возрастает и плотность этих соединений от фтор- к йодпроизводным. Все моногалогеналкилы практически нерастворимы в воде, но хорошо растворимы в органических растворителях. Монобром- и моноиодалкилы менее горючи, чем монохлоралкилы, а некоторые из них вообще не обладают горючестью. Дигалогенопроизводные – тяжелые масла или кристаллические вещества, нерастворимые в воде. Полностью фторированные алканы (перфторуглероды) выдерживают высокие температуры (до 500 °С), стойки к действию кислот, щелочей и окислителей. В отличие от монофторпроизводных, они не обладают токсичными свойствами. Температуры кипения перфторуглеродов незначительно отличаются от температуры кипения алканов с тем же числом углеродных атомов, но резко отличаются от температуры кипения других галогенопроизводных.
Химические свойства
|