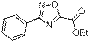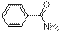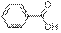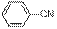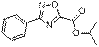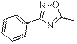КОНДЕНСАЦИЯ ЭТИЛХЛОРОКСАЛАТА С N'-ГИДРОКСИБЕНЗИМИДАМИДОМ В ПОЛЯРНЫХ СРЕДАХ
Байков С.В.,1 Воронова А.А.2 1 Ярославский государственный технический университет, Ярославль, Россия. Аспирант 2г. Chemist-baka@yandex.ru 2 Ярославский государственный технический университет, Ярославль, Россия. Студент IV курса. Научный руководитель: Кофанов Е.Р.
1,2,4-Оксадиазол-5-карбоновые кислоты и их производные широко востребованы в медицинской химии. В работе [1] описан синтез и биологические испытания серии 1,2,4-оксадиазол-5-карбамидов – селективных ингибиторов киназы гликоген синтазы 3 (GSK-3), регулятора, как дифференциации, так и пролиферации клеток. Ключевыми соединениями в данном случае являются алкил-1,2,4-оксадиазол-5-карбоксилаты, которые обычно получают взаимодействием амидоксимов с хлорангидридом моноэфира щавелевой кислоты [2]. Они служат прекурсорами в синтезе как самих 1,2,4-оксадиазолкарбоновых кислот, так и других их производных [1-5]. Данную реакцию проводят в неполярных растворителях (ТГФ, хлороформ, хлористый метилен, толуол, дихлорэтан) [1-5], однако согласно предполагаемому механизму [6] её следует проводить в полярных, слабоосновных или слабокислых средах. В связи с этим мы решили изучить конденсацию N '-гидроксбензимидамида (1) с этилхлороксалатом (2) в подобных растворителях: ацетон, ДМФА, ацетонитрил, ДМСО, уксусная кислота, пиридин, 1,4-диоксан. Ещё одной важной группой растворителей являются спирт, поскольку их часто применяют в однореакторном синтезе 1,2,4-оксадиазолов из нитрилов [7].
Таблица 1 Идентифицированные продукты реакции
При проведении реакции в ДМСО образуется сложная смесь продуктов, в которой в зависимости от условий преобладает амид бензойной кислоты (7) либо 3-фенил-1,2,4-оксадиазол (4). Также методом хроматомасс-спектрометрии зафиксированы бензойная кислота (8), целевой этил 3-фенил-1,2,4-оксадиазол-5-карбоксилат (3). В пиридине при 115 оС единственным продуктом является бензонитрил (5). При снижении температуры до 80 оС помимо бензонитрила был идентифицирован 3-фенил-1,2,4-оксадиазол (4). В уксусной кислоте кроме целевого эфира (3) образуется 5-метил-3фенил-1,2,4-оксадиазол (6), количество которого определяется температурой реакции. Состав продуктов реакции в ДМФА сильно зависит от температурного режима, однако основным продуктом при всех рассмотренных условиях является целевой эфир (3). Этиловый и изопропиловый спирты оказались не пригодны для проведения данной реакции. Было установлено, что в изопропиловом спирте в присутствии ТЭА происходит переэтерификация, которая приводит к изопропиловому эфиру (9). В этиловом спирте образуется трудноразделимая смесь продуктов, состоящая из эфира (3), 3-фенил-1,2,4-оксадиазола (4), амида (7), бензойной кислоты (8). В ацетоне, ацетонитриле, 1,4-диоксане и трет- бутаноле реакция проходит с образованием исключительно целевого эфира (3). Таким образом, из рассмотренных нами растворителей эти четыре в большей степени подходят для синтеза алкил 1,2,4-оксадизол-5-карбоксилатов.
Литература: [1] Koryakova A. G., Ivanenkov Y. A., et al. Bioorg. Med. Chem. Lett. 12 3661-3666 (2008) [2] Pace A., Piero P. Org. Biomol. Chem. 7, 4337-4348 (2009) [3] Huhtiniemi T., Rinne V.M., et al. J. Med. Chem. 15, 4377-4380 (2008) [4] Garfunkle J., Ezzili C., et al. J. Med. Chem. 15, 4392-4403 (2008) [5] Oh Chang-Hyun; Dong Hyun-Gu et al. Archiv de Pharmazie. 12,567-572 (2003) [6] Tsiulin P.A., Sosnina V.V., et. al. Russ. J. Org. Chem. 12, 1874-1877 (2011) [7] Davies S., Serradell N., et. al. Drugs of the Future 9, 733-736 (2008)
|