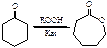ИСПОЛЬЗОВАНИЕ УСТОЙЧИВЫХ СОЕДИНЕНИЙ ПЕРЕКИСИ ВОДОРОДА В СИНТЕЗЕ ε-КАПРОЛАКТОНА
Кузнецов В.А. Институт органического синтеза им. И. Я. Постовского УрО РАН, Екатеринбург, Россия. Аспирант 1г. basilkv@yandex.ru Научный руководитель: Ятлук Ю. Г.
ε-Капролактон является ценным мономером, использующимся для получения биоразлагаемых полимеров как бытового, так и медицинского назначения. Производство ε-капролактона, его гомо- и сополимеров непрерывно растет в Европе, США, Японии – в большинстве развитых стран. Потребность в данных полимерах увеличивается и в нашей стране, в первую очередь в связи с вытеснением традиционного хирургического шовного материла (шёлк, кетгут) синтетическими биоабсорбируемыми материалами на основе полиоксиалканоатов. Традиционным методом синтеза ε-капролактона является окисление циклогексанона по реакции Байера-Виллигера.
На основе более чем столетнего опыта работы от первоначально использованных надкислот химики перешли практически к любым перекисным окислителям, варьируя растворители, катализаторы, температурные условия процесса и пр. В настоящей работе проведено сравнительное исследование по использованию устойчивых соединений перекиси водорода, выпускаемых в качестве дезинфектантов и отбеливателей, в качестве окислителей циклогексанона по реакции Байера-Виллигера. Для этой цели были использованы аддукт перекиси водорода с мочевиной (гидроперит), перборат натрия, пероксокарбонат натрия (персоль), монопероксофталаты магния (дисмозон) и натрия. Известно, что окисление гидроперитом (H2O2.CO(NH2)2) хорошо протекает при нагревании в среде гексафторизопропанола в присутствии п-толуолсульфокислоты. Нами показано, что в качестве растворителя могут быть использованы также теломерные спирты – тетрафторпропанол и октафторпентанол. Конверсия циклогексанона при этом в указанном ряду спиртов уменьшается, однако, это может быть компенсировано увеличением времени синтеза. Использование гидрата гексафторацетона позволяет достичь высокой конверсии, но увеличивает количество примеси – ε-оксикапроновой кислоты. При использовании 30% раствора перекиси водорода окисление практически количественное, но основным продуктом является ε-оксикапроновая кислота. В среде фторированных спиртов так же эффективно использование перкарбоната натрия. Перборат натрия (NaBO3.H2O2.3H2O) в качестве окислителя может быть использован в кислой среде. Как растворители мы применяли уксусную и трифторуксусную кислоты, уксусный ангидрид, а также их смеси. Количественная конверсия кетона достигается при нагревании в трифторуксусной кислоте – основным продуктом превращения является ε-оксикапроновая кислота. Перкарбонат натрия (NaСO3.1,5H2O2) также используют в кислой среде. Мы применяли те же растворители, что и в случае пербората натрия. Максимальная конверсия достигается в трифторуксусной кислоте. Также как и в случае пербората натрия основным продуктом является ε-оксикапроновая кислота. Окисление монопероксофталатом магния ([HOOOCС6Н4COO]2Mg) по литературным данным проводят в среде водного метанола при четырехкратном избытке реагента. Воспроизведение методики показывает, что в этом случае образуется много продуктов гидролиза и этерификации (ε-оксикапроновая, адипиновая кислоты и их метиловые эфиры). Нами установлено, что использование в качестве среды воды или ацетонитрила обеспечивает практически количественный выход ε-капролактона. Так как монопероксофталат магния достаточно просто синтезируется из перекиси водорода, фталевого ангидрида и оксида магния мы предприняли попытку синтеза пероксофталата натрия из персоли и фталевого ангидрида (вводили в виде раствора в этилацетате). Окисление протекает с тем же избытком реагента при комнатной температуре. Препаративный выход ε-капролактона составляет около 75%. Таким образом, в работе проведено сравнение методик окисления циклогексанона в капролактон устойчивыми и доступными соединениями: аддуктом перекиси водорода с мочевиной, перборатом натрия, пероксокарбонат натрия, монопероксофталатами магния и натрия. Показано, что наиболее дешевой системой является продукт взаимодействия персоли с фталевым ангидридом. Использование других окислителей приемлемо в случае регенерации растворителей типа гексафторизопропанола и трифторуксусной кислоты. Все окислители анализировали на содержание перекиси водорода титрованием - перманганато- или иодометрически. Конверсию циклогексанона и выход ε-капролактона оценивали по данным газожидкостной хроматографии. Идентификацию продуктов окисления осуществляли с использованием хромато-масс-спектрометрии, 1Н, 13С ЯМР и ИК-спектроскопии. Разработанные методики основаны на использовании доступного отечественного сырья и удобны для практического применения, в том числе в условиях малых предприятий.
|