МОЛЕКУЛЯРНЫЙ ВЕС И ВЯЗКОСТЬ ВМС.
Один из важнейших параметров ВМС — молекулярный вес М, и все методы его определения основаны на исследовании свойств макромолекул в растворе. Как уже отмечалось, реальные ВМС характеризуются некоторым усредненным значением
Расчет дает для
В нашем примере Основными методами измерения
где с — массовая концентрация; Μ — масса 1 моля.
где b — постоянная, зависящаяот природы растворителя и растворенного вещества. Это уравнение можно написать и в такой форме, разделив правую и левую часть на с:
Графическая зависимость величины p/с от с имеет вид прямой, не проходящей через начало координат (рис. 12). Отрезок, отсекаемый этой прямой на оси ординат, равен RT/M. Определив осмотическое давление раствора какого-либо высокомолекулярного вещества при нескольких массовых концентрациях, строят графическую зависимость л/с от с и продолжив полученную прямую до пересечения с осью ординат, находят RT/M, а затем М. Определение молекулярной массы полимера по осмотическому давлению разбавленных растворов является одним из самых распространенных методов. Естественно, что определяемая молекулярная масса полимера будет средней величиной.
где с — весовая концентрация ВМС; ηуд — удельная вязкость.
Дальнейшие исследования не подтвердили, однако, применимости выражения (ηуд = КМ с) для большинства изученных систем. Действительно, это уравнение описывает лишь предельный случай, выполняющийся как при отсутствии взаимодействия между макромолекулами, так и при их предельном выпрямлении. В отсутствие взаимодействия величина ηуд/ с, называемая п р и веденной вязкостью, не должна быть функцией с, согласно уравнениям Эйнштейна и Штаудингера (при М = const). Однако результаты вискозиметрических измерений показывают, что ηуд/ с возрастает (обычно почти линейно) с увеличением с (рис. 125). Поскольку рост этот обусловлен усилением взаимодействия между макромолекулами, целесообразно исключить его влияние путем экстраполяции ηуд/ с к значению с = 0. Полученная таким образом величина
не включающая взаимодействия между макромолекулами, называется характеристической вязкостью и может быть введена в вместо переменной ηуд/ с: [η] = КМ. Второе условие — полное выпрямление молекулы никогда практически не реализуется. Макромолекулы всегда в той или иной степени свернуты в статистические клубки, обладающие меньшим гидродинамическим сопротивлением, чем растянутые молекулы. Статистический расчет для молекул, обладающих полной свободой вращения всех звеньев цепи, дает: [η] = КМ1/2 Взаимодействие с растворителем приводит к ограничению свободы вращения звеньев (увеличению жесткости цепи). Это ограничение учитывается параметром [η] = КМ1/2 а 3 Для «плохих» (слабо взаимодействующих с ВМС) растворителей а ≈ 1 и ([η] = КМ1/2 а 3) переходит в ([η] = КМ1/2). Для «хороших» а пропорциональна где α — постоянная для полимергомологического ряда величина, значения которой лежат обычно в пределах 0,55—0,85. Величину [η] находят на основании измерений относительной вязкости растворов, из которой вычисляют η уд, ηуд/ с и далее, [η] путем графической экстраполяции кривой ηуд/ с к с = 0. Для нахождения К и α проводят совместное определение [η] и М (например, осмометрически) для нескольких низших членов полимергомологического ряда. Эти значения наносят на график в координатах lg[η]— lgМ и по тангенсу угла наклона (равному α) и отрезку, отсекаемому прямой на оси ординат (равному lgК), находят обе константы. Полученные таким образом значения К и α для различных систем приводятся в виде таблиц в справочниках и монографиях. Некоторые примеры представлены в табл. 13. Пользуясь этими таблицами, можно найти М по уравнению ([η] = КМα) и судить о его изменениях в процессах полимеризации, расщепления ВМС и т. д. Для этого нужно лишь измерить η (или η / η0), определить [η] способом, указанным выше (через η уд/ с), и вычислить М по ([η] = КМα). Этот метод дает средневязкостнуго величину
где α — показатель степени в (XVII. 9). При α ≈ 1 Мы рассмотрели наиболее общие свойства ВМС и их растворов без учета электрических зарядов. Между тем, многие набухшие и растворенные полимеры диссоциированы на ионы и представляют собой, таким образом, полиэлектролиты, относящиеся к классу коллоидных электролитов. Наличие заряда, α следовательно, и электрической компоненты свободной энергии, существенно изменяет термодинамические, кинетические и другие свойства и создает ряд особенностей поведения заряженных систем. Эти особенности очень важны не только для практики, но и для прогресса науки, главным образом в одном из важнейших ее направлений — в коллоидно-химической биологии. Перейдем к рассмотрению свойств коллоидных электролитов. Таблица 13
Тесты 1.Какие соединения называются высокомолекулярными? а) вещества имеющие молекулярную массу от 10000 до нескольких миллионов а.е.м.; б) вещества имеющие молекулярную массу от нескольких десятков до нескольких сотен а.е.м.; в) только вещества имеющие молекулярную массу больше 100 миллионов а.е.м.; г) все выше перечисленные категории. 2.Как можно классифицировать ВМС? а) только по происхождению; б) только по строению полимерной цепи; в) только по способности к электролитической диссоциации; г) по всем выше перечисленным признакам. 3.Чем определяется особенности строения полимеров? а) существованием двух типов связей; б) гибкостью цепей; в) природой растворителя; г) внешними условиями. 4.Что такое конформация полимеров? а) различные формы макромолекул, получающиеся под действием теплового движения и не сопровождающиеся разрывом химических связей; б) различные формы макромолекул, получающиеся под действием теплового движения и сопровождающиеся разрывом химических связей; в) только линейная форма макромолекул; г) только разветвленная форма макромолекул. 5.Чем вызвана гибкость и жесткость полимерных цепей? а) обусловлена внутренним вращением звеньев; б) межмолекулярными связями; в) реакционной способностью полимерного звена; г) молекулярной массы полимера. 6.Сколько уровней, структурной организации белков выделяют? а) 4; б) 3; в) 6; г) 8. 7.Что такое денатурация белков? а) нарушение конформации полипептидных цепей; вторичной и третичной структуры с разрывом пептидных связей; б) нарушение конформации полипептидных цепей; вторичной и третичной структуры без разрыва пептидных связей; в) только нарушение регулярных вторичных структур. 8.В чем состоят сходство и различие между растворами низкомолекулярных и высокомолекулярных соединений? а) раздроблены до коллоидных частиц; б) имеют молекулярную степень раздробленности; в) гетерогенны; г) гомогенны. 9.По каким признакам растворы ВМС относятся к коллоидным системам? а) растворы ВМС способны рассеивать свет; б) в растворах, молекулы ВМС совершают броуновское движение; в) по увеличенной вязкости растворов ВМС; г) по неоднородности растворов ВМС. 10.Почему растворы высокомолекулярных соединений являются термодинамически устойчивыми? а) при растворении ∆G < 0; б) при растворении ∆G > 0; в) при растворении ∆G = 0; г) при растворении ∆G = 0,125 кДж/моль 11. В чем состоит сходство между растворами высокомолекулярных соединений и коллоидными растворами? а) растворы ВМС, как и коллоидные растворы только пропускают свет; б) растворы ВМС, как и коллоидные растворы, могут рассеивать свет; в) растворы ВМС, как и коллоидные растворы единственно отражают свет; г) растворы ВМС, как и коллоидные растворы исключительно поглощают свет. 12.В чем особенность выражения молекулярной массы полидсперсных полимеров? а) это абсолютное значение; б) характеризует среднее значение молекулярной массы ВМС; в) зависит от химического строения; г) зависит от конформации макромолекулы полмера. 13.Методом измерения осмотического давления растворов ВМС можно опрелелить: а) средневязкостную молекулярную массу; б) среднечиленную молекулярную массу; в) средневесовую молекулярную массу; г) любую молекулярную массу. 14.Методом измерения интенсивности рассеяния света растворов ВМС можно опрелелить: а) среднечиленную молекулярную массу; б) любую молекулярную массу; в) средневязкостную молекулярную массу; г) средневесовую молекулярную массу. 15.Зависимость вязкости суспензии сферических частиц от концентрации подчиняется: а) закону Гука; б) правилу Марковникова; в) закону Эйнштейна; г) эмпирическому уравнению Макра-Хаувинка. 16. Зависимость характеристической вязкости растворов полимеров подчиняется: а) закону Гука; б) закону Эйнштейна; в) эмпирическому уравнению Макра-Хаувинка. г) правилу Марковникова. 17.Какую молекулярную массу полимера определяют методом вискозиметрии: а) среднечиленную молекулярную массу; б) любую молекулярную массу; в) средневязкостную молекулярную массу; г) средневесовую молекулярную массу. 18.Какой процесс называется набуханием? а)увеличение объёма и массы полимера во времени при контакте с растворителем; б)увеличение объёма и массы растворителя во времени при контакте с полимером; в) увеличение объёма полимера, без изменения его массы; г) увеличение массы полимера без изменения его объёма. 19. Что является количественной мерой процесса набухания? а) степень набухания; б) масса сухого полимера; в) объём сухого полимера; г) объём растворителя. 20.В чем состоят особенности ограниченного набухания? а) степень набухания достигает предельного значения, а затем не изменяется; б) степень набухания достигает предельного значения, а затем уменьшается в) степень набухания растет неограниченно; г) степень набухания равна нулю. 21.Как изменяется энтальпия при набухании? а) в первой стадии ∆Н≈0, а во второй стадии ∆Н>0; б) в первой стадии ∆Н<0, а во второй стадии ∆Н≈0; в) в первой стадии ∆Н>0, а во второй стадии ∆Н<0; г) в первой стадии ∆Н<0, а во второй стадии ∆Н>0. 22. Как изменяется энтропия при набухании? а) в первой стадии ∆S>0, а во второй стадии ∆S=0;; б) в первой стадии ∆S≤0, а во второй стадии ∆S=0; в) в первой стадии ∆S≤0, а во второй стадии ∆S>0; г) в первой стадии ∆ S >0, а во второй стадии ∆ S <0. 23.Что называется контракцией? а) постоянство суммарного объёма растворителя и полимера до набухания и после набухания; б) суммарный объём полимера и растворителя поглощенного полимером до набухания больше, чем объём набухшего полимера; в) суммарный объём полимера и растворителя поглощенного полимером до набухания меньше, чем объём набухшего полимера; г) избирательное поглощение растворителя полимером. 25.Что называется синерезисом? а) выделение жидкости из студня; б) выделение жидкости из растворов; в) только выделение воды из студня. 26.Какие высокомолекулярные соединения называются полиэлектролитами? а) полимеры, макромолекулы которых не содержат ионогенные группы; б) полимеры, макромолекулы которых содержат ионогенные группы; в) только полимеры, макромолекулы которых содержат анионактивные группы; г) полимеры, макромолекулы которых содержат катионактивные группы. 27.На какие группы делятся полиэлектролиты? а) только полиоснования и поликислоты; б) поликислоты, полиоснования и полиамфолиты; в) только полиамфолиты; г) только поликислоты и полиамфолиты. 28.Каково строение молекулы белка? а) молекулы белков построены, в основном, из остатков различных аминокислот; б) молекулы белков построены из остатков угольной кислоты; в) молекулы белков построены из остатков фосфорной кислоты; г) молекулы белков построены различных оксикислот. 29.Как диссоциирует молекула белка в кислой среде? а) H3N-R-COOH + Н2О ⇄ H3N+-R-COOH + OH-; б) H3N-R-COOH + Н+ ⇄ H3N+-R-COOH; в) H3N-R-COOH + НО- ⇄ H2N-R-COO- + НOH; г) H3N-R-COOH + Н+ ⇄ H2N-R-COO- + H2О 30.Что называется изоэлектрической точкой белка? а) значение рН, при котором наблюдается избыток отрицательных зарядов; б) значение рН, при котором нет избытка отрицательных или положительных зарядов; в) значение рН, при котором есть избыток положительных зарядов;
|

 . При этом различные методы измерения дают разные числовые значения
. При этом различные методы измерения дают разные числовые значения  :
:
 :
: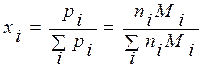



 Для выражения осмотического давления растворов высокомолекулярных соединений в это уравнение вводится дополнительный член, учитывающий взаимодействие гибких макромолекул в растворе друг с другом и с растворителем:
Для выражения осмотического давления растворов высокомолекулярных соединений в это уравнение вводится дополнительный член, учитывающий взаимодействие гибких макромолекул в растворе друг с другом и с растворителем:


 Интенсивность рассеяния света зависит от общего количества дисперсной фазы. Поэтому применяя метод светорассеяния, мы находим
Интенсивность рассеяния света зависит от общего количества дисперсной фазы. Поэтому применяя метод светорассеяния, мы находим  Растворы ВМС обычно не подчиняются закону Эйнштейна:
Растворы ВМС обычно не подчиняются закону Эйнштейна:
 Многочисленные наблюдения показа ли, что ηуд увеличивается с ростом М при с = const. Смысл этой зависимости определяется тем, что большие молекулы оказывают относительно большее сопротивление потоку. Штаудингер пришел к следующему выражению зависимости вязкости раствора от молекулярного веса полимера: ηуд = КМ с, где К — постоянная для всего полимергомологического ряда, определяемая криоскопически в растворах низших его членов.
Многочисленные наблюдения показа ли, что ηуд увеличивается с ростом М при с = const. Смысл этой зависимости определяется тем, что большие молекулы оказывают относительно большее сопротивление потоку. Штаудингер пришел к следующему выражению зависимости вязкости раствора от молекулярного веса полимера: ηуд = КМ с, где К — постоянная для всего полимергомологического ряда, определяемая криоскопически в растворах низших его членов. Это уравнение, по Штаудингеру, можно получить, считая, что гидродинамическое сопротивление молекулы потоку пропорционально ее эффективному сечению — проекции сферы вращения молекулы на плоскость, перпендикулярную потоку. Для палочкообразной молекулы это сечение пропорционально квадрату ее длины, а следовательно, М2. Общее сопротивление всех v молекул (в см3) пропорционально, таким образом, M2 v или М с, поскольку v = с/М.
Это уравнение, по Штаудингеру, можно получить, считая, что гидродинамическое сопротивление молекулы потоку пропорционально ее эффективному сечению — проекции сферы вращения молекулы на плоскость, перпендикулярную потоку. Для палочкообразной молекулы это сечение пропорционально квадрату ее длины, а следовательно, М2. Общее сопротивление всех v молекул (в см3) пропорционально, таким образом, M2 v или М с, поскольку v = с/М.
 , где
, где  — средний квадрат расстояния между концами цепи при взаимодействии, а
— средний квадрат расстояния между концами цепи при взаимодействии, а  — в отсутствие взаимодействия с растворителем. Теория, развитая Флори и Фоксом, показывает, что учет взаимодействия с растворителем приводит к следующему выражению:
— в отсутствие взаимодействия с растворителем. Теория, развитая Флори и Фоксом, показывает, что учет взаимодействия с растворителем приводит к следующему выражению: 0,1, а следовательно, [η] = КМ0,8. В общем случае [η] = КМα,
0,1, а следовательно, [η] = КМ0,8. В общем случае [η] = КМα, 



