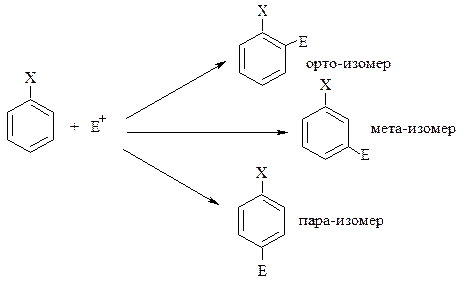Химические свойства бензола
Бензол является ненасыщенным соединением, но мы выяснили, что в его структуре нет двойных связей, а есть ароматическая связь – делокализованное электронное облако. Типичные реакции непредельных углеводородов – электрофильное присоединение и окисление – для бензола не характерны. Так, он не обесцвечивает бромную воду, не даёт реакции Вагнера (окисление раствором перманганата калия при комнатной температуре). Для бензола характерны реакции, не приводящие к нарушению замкнутой сопряжённой системы, – реакции замещения. Чтобы выяснить, какой тип замещения (радикальное, электрофильное, нуклеофильное) характерен для бензола, вспомните его электронное строение: σ-скелет молекулы плоский, а над и под плоскостью расположено ароматическое облако. Чтобы провзаимодействовать с этим ароматическим облаком, реагент должен быть электрофильным. Итак, для бензола (и ароматических соединений вообще) характерны реакции электрофильного замещения. Примерами реакций SE являются:
Рассмотрим общий механизм реакций электрофильного замещения в бензоле.
На первой стадии электрофил подходит к молекуле бензола и взаимодействует со всем ароматическим облаком (они притягиваются друг к другу). Образуется π-комплекс. Для образования новой ковалентной связи углерод-электрофил необходима пара электронов. Электрофил вырывает её из ароматического облака, образуется σ-комплекс. Он не является замкнутой сопряжённой системой, т.к. атом углерода, образовавший новую σ-связь, перешёл в sp3-гибридизацию (он вышел из плоскости и больше не имеет негибридной pz-орбитали). Остальные пять атомов углерода продолжают участвовать в сопряжении, образуя общее электронное облако, в котором делокализовано четыре электрона (6-2=4), поэтому положительный заряд в σ-комплексе обозначается не на конкретном атоме углерода, а в центре разомкнутого кольца. Итак, σ-комплекс не является ароматической структурой. Для того чтобы вернуть ароматичность, ему необходимо отщепить протон водорода (H+). Его забирает оставшийся в реакционной среде нуклеофил (Nu-). Два электрона связи C-H возвращаются в ароматическое облако, атом углерода вновь становится Лимитирующей стадией реакции электрофильного замещения является стадия образования σ-комплекса, т.к. при этом происходит потеря ароматичности, что требует затрат энергии. Различные реакции электрофильного замещения в бензоле протекают по общему механизму и отличаются только стадией образования электрофильной частицы. Реакция нитрования бензола протекает под действием смеси концентрированных азотной и серной кислот (схему реакции см. выше). Рассмотрим её механизм.
На первой стадии реакции азотная кислота взаимодействует с серной. В данном случае азотная кислота выполняет роль основания, принимая протон от молекулы серной кислоты (по теории Бренстеда, кислота – это молекула или ион, отдающие протон, а основание – молекула или ион, принимающие протон водорода). Образуется протонированная азотная кислота, которая, отщепляя молекулу воды, превращается в катион нитрония, или нитроний-катион. Это и есть электрофильная частица. Таким образом, серная кислота выполняет роль катализатора, принимая участие в образовании электрофильного реагента. Вторая роль серной кислоты – это роль водоотнимающего средства. Воду необходимо отводить из сферы реакции, чтобы сместить её равновесие вправо. После образования электрофила – катиона нитрония - реакция протекает по общему механизму, через образование π- и
Обратите внимание: на стадии превращения σ-комплекса в нитробензол (стадии возвращения ароматичности) протон водорода отщепляется под действием аниона серной кислоты, при этом вновь образуется серная кислота, что доказывает, что она являлась катализатором данной реакции.
Далее молекула бензола взаимодействует с образовавшимся комлексом как с электрофилом:
На стадии образования π-комплекса происходит дальнейшая поляризация связи Cl-Cl, и она разрывается гетеролитически, причём Cl+ сразу участвует в образовании σ-комплекса.
Связь C-Cl в метилхлориде недостаточно полярна, чтобы разорваться гетеролитически. Под действием кислоты Льюиса увеличивается частичный положительный заряд на атоме углерода, и комплекс реагента с катализатором является более сильным электрофилом, чем исходный метилхлорид. Реакция сульфирования бензола протекает под действием олеума (раствор серного ангидрида SO3 в концентрированной серной кислоте).
При образовании π-комплекса связь S=O (в первую очередь π-связь) поляризуется и разрывается по гетеролитическому типу, поэтому при образовании σ-комплекса на атоме кислорода возникает полный отрицательный заряд. Для восстановления ароматичности протон водорода отщепляется от атома углерода кольца и переходит к отрицательно заряженному кислороду. Образуется бензолсульфокислота. Когда мы рассматриваем реакции электрофильного замещения в бензоле, перед нами не стоит вопрос, в каком положении протекает реакция, т.к. все атомы углерода абсолютно равноценны. Другое дело, если в бензольном кольце уже есть заместитель. В этом случае в результате электрофильного замещения принципиально возможно образование трёх изомеров:
Чтобы ответить на вопрос, какой из этих возможных продуктов является преобладающим, необходимо рассматривать электронные эффекты заместителя. Отвлечёмся от реакций электрофильного замещения в бензоле и его производных и рассмотрим электронные эффекты в целом.
|


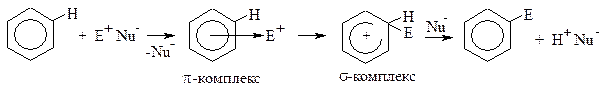


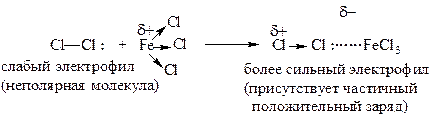 Катализатором реакции галогенирования являются так называемые кислоты Льюиса (по теории Льюиса, кислоты – это нейтральные молекулы или ионы, способные принимать пару электронов): FeCl3, FeBr3, AlCl3, AlBr3 и т.п. Катализатор необходим, чтобы поляризовать молекулу галогена. Кислота Льюиса смещает на себя неподелённую электронную пару хлора, образуя комплекс, в котором на одном из атомов хлора сосредоточивается частичный положительный заряд:
Катализатором реакции галогенирования являются так называемые кислоты Льюиса (по теории Льюиса, кислоты – это нейтральные молекулы или ионы, способные принимать пару электронов): FeCl3, FeBr3, AlCl3, AlBr3 и т.п. Катализатор необходим, чтобы поляризовать молекулу галогена. Кислота Льюиса смещает на себя неподелённую электронную пару хлора, образуя комплекс, в котором на одном из атомов хлора сосредоточивается частичный положительный заряд:
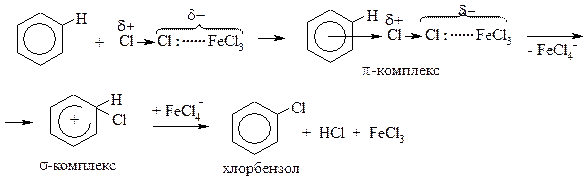
 Аналогично протекают реакции алкилирования (реакция Фриделя-Крафтса).
Аналогично протекают реакции алкилирования (реакция Фриделя-Крафтса).
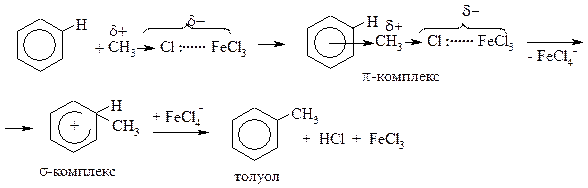
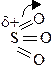 Молекула серного ангидрида является электрофилом из-за большого по величине частичного положительного заряда на атоме серы.
Молекула серного ангидрида является электрофилом из-за большого по величине частичного положительного заряда на атоме серы.