Гибкость полимерных молекул.
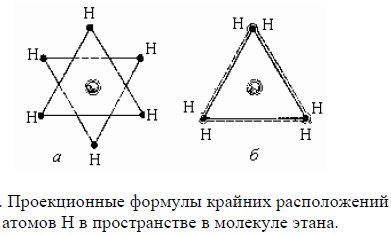
Гибкость является одной из важнейших характеристик полимеров, определяющей высокоэластические, релаксационные и термомеханические свойства полимеров, а также особенности свойств их растворов. Гибкость характеризует способность макромолекул изменять свою форму под влиянием теплового движения звеньев или внешних механических воздействий. Гибкость обусловлена внутренним вращением звеньев или частей макромолекул относительно друг друга. Рассмотрим явление внутреннего вращения в молекулах на примере простейшего органического соединения - молекулы этана. В молекуле этана (СН3-СН3) атомы углерода связаны с атомами водорода и друг с другом ковалентными (σ-связями), причём угол между направлениями σ-связей (валентный угол) составляет 1090 28'. Это вызывает тетраэдрическое расположение заместителей (атомов водорода) в пространстве в молекуле этана. Вследствие теплового движения в молекуле этана происходит вращение одной группы CH3 относительно другой вокруг оси С-С. При этом непрерывно меняется пространственное расположение атомов и потенциальная энергия молекулы. Графически различные крайние расположения атомов в молекуле можно представить в виде проекций молекулы на горизонтальную плоскость (рис.1).
Допустим, что в положении а потенциальная энергия молекулы равна U1, а в положении б - U2 при этом U1 = U2, т.е. положения молекулы энергетически неравноценны. Положение б при котором атомы Н расположены друг под другом является энергетически невыгодным, так как между атомами Н проявляются силы отталкивания, которые стремятся перевести атомы в энергетически выгодное положение а. Если принять U1=0, то U2=max.
Молекулы с меньшей симметрией (например, молекула дихлорэтана) имеют более сложную зависимость U=f(φ). Потенциальным (Uo) или активационным барьером вращения называется энергия, необходимая для перехода молекулы из положения минимума в положение максимума потенциальной энергии. Для этана U0 малая величина (Uo=11.7 кДж/моль) и при обычной температуре происходит вращение групп СН3 вокруг связи С-С с большой скоростью (1010 об/сек). У полимеров вследствие внутри- и межмолекулярных взаимодействий зависимость U=f(φ) имеет сложную форму. Если одно положение звена цепи характеризуется потенциальной энергией U1, а другое - U2, то энергия перехода из одного положения в другое равна разности
|


 U= U1 - U2. Разность энергий перехода
U= U1 - U2. Разность энергий перехода  U из одного равновесного положения звена макромолекулы в другое характеризует термодинамическую гибкость. Она определяет способность цепи изгибаться под влиянием теплового движения.
U из одного равновесного положения звена макромолекулы в другое характеризует термодинамическую гибкость. Она определяет способность цепи изгибаться под влиянием теплового движения. 


