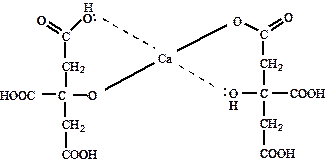I. БИОХИМИЯ ТКАНЕЙ ЗУБА
В составе зуба выделяют минерализованные и неминерализованные ткани. К первым относятся эмаль, дентин и цемент. Вообще в организме человека в норме имеется четыре вида минерализованных тканей: эмаль, дентин, цемент и кость, которые отличаются по химическому составу и происхождению. Последние три происходят из стволовых клеток мезодермы, тогда как эмаль является производным эктодермы. В их химическом составе преобладают неорганические компоненты, а также присутствуют органические соединения и вода (табл.1). Мягкая (неминерализованная) ткань в составе зуба одна, она называется пульпой и находится в полости коронки и корня зуба. Таблица 1 Химический состав эмали, дентина и кости (в % от массы)
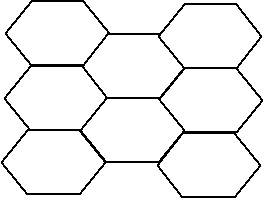
1.1. ЭМАЛЬ Эмаль, покрывающая коронку зуба, - самая твердая ткань в организме (сравнимая с алмазом), что объясняется высокой концентрацией в ней неорганических веществ (до 97%), главным образом, кристаллов апатитов: гидроксиапатита (до 75%), карбонатапатита, фторапатита, хлорапатита и др. Здоровая эмаль содержит 0,8-1,0% свободной воды и 1,2% органических соединений, представленных белками, липидами и углеводами. Углеводы эмали в основном представлены глюкозой, маннозой и галактозой. Вода занимает свободное пространство в кристаллической решетке апатитов и органической основе, а также располагается между кристаллами. Неорганический компонент эмали. Мельчайшими структурными единицами эмали являются кристаллы апатитоподобного вещества, формирующие эмалевые призмы. Минеральную основу составляют кристаллы апатитов и восьмикальциевый фосфат - Са8Н2(РО4)6*5Н2О; формула основного гидроксиапатита - Са10(РО4)6(ОН)2, в этом случае молярное соотношение Са/Р равно около 1,67. Однако, как это установлено в настоящее время, соотношение этих компонентов может изменяться как в сторону уменьшения(1,33), так и в сторону увеличения (2,0). При соотношении Са/Р 1,67 разрушение кристаллов происходит при выходе 2 ионов Са2+, при соотношении 2,0 гидроксиапатит способен противостоять разрушению до замещения 4 ионов Са, тогда как при соотношении 1,33 его структура разрушается. По современным представлениям данный параметр можно использовать для оценки состояния эмали зуба. Гидроксиапатит имеет гексагональную форму (рис. 1). Длинная ось кристаллов-призм расположена по основному направлению давления на кость или зуб. Каждый кристалл покрыт гидратной оболочкой около 1 нм. Связанная вода, образующая эту оболочку, составляет примерно 3,0-3,3% массы эмали. Кроме связанной воды (гидратная оболочка) в эмали имеется свободная вода, располагающаяся в микропространствах. Общий объем воды в эмали составляет 3,8%. Первое упоминание о жидкости, находящейся в твердых тканях зуба, относится к 1928 году. В дальнейшем стали дифференцировать зубную жидкость, которая находится в дентине от эмалевой жидкости, заполняющей микропространства, объем которых составляет 0,1-0,2% от объема эмали. В исследованиях на удаленных зубах человека с использованием специальной методики подогрева показано, что через 2-3 часа после начала опыта на поверхности эмали образуются капельки «эмалевой жидкости». Движение жидкости обусловлено капиллярным механизмом, а по жидкости диффундируют молекулы и ионы. Эмалевая жидкость играет важную биологическую роль не только в период развития эмали, но и в сформированном зубе, обеспечивая ионный обмен.
Рис. 1. Строение молекулы гидроксиапатита
Состояние эмали зуба во многом определяется соотношением Са/Р как элементов, составляющих основу эмали зуба. Это соотношение непостоянно и может изменяться под воздействием ряда факторов. Здоровая эмаль молодых людей имеет более низкий коэффициент Са/Р, чем эмаль зубов взрослых; этот показатель уменьшается также при деминерализации эмали. Более того, возможны существенные различия соотношения Са/Р в пределах одного зуба, что послужило основанием для утверждения о неоднородности структуры эмали зуба, и, следовательно, о неодинаковой подверженности различных участков эмали поражению кариесом. В кристаллической решетке гидроксиапатита имеются вакантные места, поэтому даже в уже сформированном кристалле при химических и физических воздействиях возможны изоморфные замещения. При этом любое проникновение веществ на поверхность или внутрь кристалла связано с преодолением гидратной оболочки. Результатом подобных явлений и образования вакансий является варьирование свойств кристаллов, что выражается в изменении проницаемости эмали, ее резистентности к растворению, адсорбционных свойств. Однако, только некоторые ионы могут включаться в структуру апатитов. Если общую формулу апатита представить как А10В6Х2, то по положению А могут включаться ионы Са2+, Mg2+, Ва2+, Cr2+, Sr2+ и другие, по положению В - РО43- и другие, по положению Х - НО-, F-, Cl- и другие. Примером реакции изоморфного замещения является следующая: Са10(РО4)6(ОН)2 + Mg2+ à Са9 Mg(РО4)6(ОН)2 + Са2+ Известно, что приведенное выше взаимодействие является неблагоприятным, так как снижает резистентность эмали к действию кариесогенных факторов. Замещение в гидроксиапатитах ионов Са на Sr сопровождается формированием стронциевых апатитов - Ca9Sr(РО4)6(ОН)2. При этом стронций, поступая в избыточном количестве, хотя и вытесняет из кристаллической решетки кальций, но сам в ней не удерживается, что приводит к порозности костей. Этот эффект усугубляется недостатком кальция. В результате проводимых как в нашей стране, так и за рубежом, исследований установлено, что микроэлементы в эмали располагаются неравномерно. В наружном слое отмечается большое содержание фтора, свинца, цинка, железа при меньшем содержании в этом слое натрия, магния, карбонатов. Равномерно по слоям распределяются, как правило, стронций, медь, алюминий, калий. Такие изменения характерны для болезни Кашина-Бека (“уровская болезнь”), которая поражает людей, преимущественно в раннем детстве, живущих в долине реки Уров Читинской и Амурской областей. Страдание начинается с болей в суставах, затем возникает поражение костной ткани, размягчение эпифизов, нарушаются процессы окостенения. В эндемичных районах в почве и воде содержится в 2 раза меньше кальция и в 1,5-2 раза больше стронция, чем в норме. В настоящее время существует и другая теория патогенеза “уровской болезни”, согласно которой патология развивается в результате дисбаланса фосфатов в окружающей среде. Изоморфное замещение в гидроксиапатите на фтор приводит к образованию гидроксифторапатитов и фторапатитов - Са10(РО4)6F(ОН) и Са10(РО4)6F2: Са10(РО4)6(ОН)2 + F- à Са10(РО4)6F(ОН) + (ОН)- Фторапатиты, которых в норме в эмали около 0,66%, обладают значительно большей резистентностью к растворению в кислой среде, чем гидроксиапатиты. Было установлено, что при замещении фтором даже одной из 50 гидроксильных групп растворимость эмали резко понижалась. Именно с этим связано профилактическое действие небольших концентраций фтора. Однако при высоком его содержании образуется фторид кальция - СаF2 - практически нерастворимое соединение, которое быстро исчезает с поверхности зубов в результате выщелачивания: Са10(РО4)6(ОН)2 + 2F- à 10СаF2 + 6(РО4)3- + 2(ОН)- В связи с этим не следует применять высокие концентрации фторидов, особенно в кислых растворах. В эмали зуба также содержатся хлорапатит - Са10(РО4)6Cl2 (4,4%) и карбонатапатиты - Са10(РО4)5СО3(ОН)2. Они составляют 19% и их количество увеличивается при употреблении пищи, богатой углеводами. Рост концентрации карбонатапатитов грозит снижением резистентности эмали и способствует развитию кариозного процесса. Большая часть кристаллов гидроксиапатита в эмали ориентирована и упорядочена в виде сложных образований - эмалевых призм. Элементарная ячейка гидроксиапатита (структура 1 порядка) имеет молекулярную массу около 1000, в составе кристалла гидроксиапатита (структура 2 порядка) находится около 2500 таких ячеек (М=2 500 000). Эмалевая призма (структура 3 порядка) в свою очередь составлена из тысяч и миллионов кристаллов. Эмалевые призмы начинаются у эмалево-дентинной границы и идут к поверхности эмали, многократно изгибаясь в виде спирали, которые собраны в пучки (структура 4 порядка). Органические соединения эмали. В процентах сухой массы они составляют: белки – 0,25-0,45%, липиды – 0,6%, цитраты – 0,1%. Наибольшее количество протеинов содержится в области эмалево-дентинного соединения. Белки эмали нельзя причислить к группе коллагеновых, так как в протеинах эмали нет гидроксипролина, а количество пролина составляет 166-187 аминокислотных остатков на 1000. В эмали имеются белки, участвующие в амелогенезе - амелогенины и не являющиеся амелогенинами (энамелины). Амелогенин (первая группа белков эмали) представлен 5 соединениями с молекулярной массой 25; 15; 9,5; 7,5 и 6 кДа. Энамелины (вторая группа белков эмали) также являются гетерогенной фракцией и состоят из 5 классов с молекулярной массой, равной 72, 56, 42, 30, 21 кДа. Белки этого семейства способны агрегироваться и дезагрегироваться. Оба класса протеинов относятся к сложным – гликофосфопротеидам, причем амелогенины содержат до 75% органического фосфата, а энамелины – 25%. Основой формирования и функционального построения эмали служит ее белковая матрица, элементарной функциональной единицей которой является кальций-связывающий белок эмали (КСБЭ). Последний способен к олиго- и полимеризации посредством кальциевых мостиков с образованием трехмерной белковой сетки, нерастворимой в нейтральной среде. Эта структура в дальнейшем выступает в роли центров кристаллизации, обеспечивая упорядоченность и регулярность минерализации, на этапах которой мы подробно остановимся ниже. По мере созревания меняется белковый профиль эмали. На начальном этапе формирования этой ткани соотношение амелогенинов и энамелинов составляет 9:1, а среди аминокислот превалируют такие как пролин и гистидин; в зрелой наряду с уменьшением количества белка оно становится 1:1 и в аминокислотном составе начинают преобладать аспартат, серин, глицин и аланин. Изменение белкового состава эмали связано с различием функций, осуществляемых протеинами на разных стадиях формирования зуба: вначале с транспортом и депонированием минеральных компонентов, а затем с инициацией минерализации. Еще в эмали обнаружен уникальный гидроксипролинсодержащий гликофосфопептид с Мr=3 кДа, он прочно связан с гидроксиапатитом и возникает в результате деградации коллагеноподобного белка зуба или попадает в процессе выделения его из дентина. Третья группа белков эмали – это растворимые белки с Мr 20 кДа. Однако они не обладают сродством к минеральной фазе, не способны к образованию комплексов с кальцием и имеют менее регулярную структуру. Роль этих белков в эмали и в процессе минерализации неясна. Вполне вероятно, что они являются остаточными белками “эмалевого органа”. Процессы минерализации. До восьмого месяца развития плода происходит формирование зачатка зуба, а к моменту рождения ребенка образуется зрелая эмаль. Начало минерализации совпадает с разрушением полипептидов эмалевого матрикса. I этап – протеолиз высокомолекулярных белков до низкомолекулярных с помощью катепсинов (тканевых протеаз) и плазмина. II этап – обогащение матрикса ионами кальция и неорганическим фосфатом. Источником первого является преимущественно цитрат (см. ниже), а второй поступает за счет активации щелочной фосфатазы, которая гидролизует органические эфиры фосфорной кислоты. III этап – фосфорилирование остатков серина в низкомолекулярных белках в результате действия протеинкиназы (рис. 2). IV этап – с фосфорилированными остатками серина реагируют ионы кальция и неорганического фосфата (рис. 2). В конечном итоге формируется первичная ячейка гидроксиапатита (первичный кристалл).
Рис. 2. Схема некоторых этапов минерализации.
Дальнейшее формирование решетки протекает по типу эпитаксии, представляющей собой рост последующих кристаллов на базе предыдущего. При этом вновь образующиеся кристаллы ориентированы по первичному и не связаны с белком. Наличие большого количества глутамата и аспартата в эмалевых белках и других протеинах минерализованных тканей позволяет присоединять кальций непосредственно к карбоксильной группе этих аминокислот. Кроме того, лизин коллагена способен также взаимодействовать с неорганическим фосфатом путем образования фосфамидной связи (рис.3). В костной ткани преципитация кальция и фосфата возможна не только на белках, но и на углеводах и липидах. Амелогенез во многом определяется белковой матрицей. Ингибирование протеолиза, согласно гипотезы Robinson и Kirkham (1984), способствует сохранению белка и нарушает амелогенез, что может быть причиной гипоплазии эмали и флюороза. После прорезывания зубов процесс созревания эмали продолжается и он тесно связан с поступлением минеральных компонентов через приобретенную пелликулу зуба из смешанной слюны.
Рис. 3. Возможные варианты формирования первичного кристалла.
С возрастом происходит накопление Са2+ в поверхностном слое эмали, при этом меняется соотношение Са/Р с 1,51 до 1,86. Это процесс динамичный и зависит от анатомической принадлежности зуба, места его расположения, топографии участка зуба и других факторов. Так, наиболее быстро созревает эмаль в области режущих краев и бугров (в течение 4-6 месяцев после прорезывания). От степени созревания эмали в определенной мере зависит кариесрезистентность зубов. Регуляция процессов минерализации. Для минерализации костей, твердых тканей зуба необходимо поддержание определенных концентраций ионов кальция и неорганического фосфата в плазме крови, слюне и надкостнице. В организме взрослого человека содержится в среднем 1000 г кальция. Основным его депо в организме (99%) являются кости. В костях около 99% кальция присутствует в виде малорастворимой формы кристаллов гидроксиапатита. Другой фонд кальция – это кальций плазмы крови. В плазму крови кальций поступает из кишечника (с водой и пищей) и из костной ткани (в прцессе резорбции). Нормальное протекание процессов минерализации обеспечивается тем, что концентрация Са2+ в крови варьирует в очень узких пределах (2,12-2,60 ммоль/л – у взрослых; 2,74-3,24 ммоль/л – у детей), более широкие колебания характерны для цифр неорганического фосфата (0,64-1,29 ммоль/л – у взрослых; 1,29-2,26 ммоль/л – у детей). В механизм регуляции гомеостаза этих ионов включены три гормона – паратироидный (паратгормон), кальцитонин и кальцитриолы (1,25(ОН)2D3 и 24,25(ОН)2D3). Паратироидный гормон (ПТГ) продуцируется околощитовидными железами и по механизму действия является антагонистом тирокальцитонина. Паратгормон – это полипептид, состоящий из 84 аминокислотных остатков, синтезируется в виде препрогормона (115 аминокислот). От последнего в результате частичного гидролиза в эндоплазматической сети отщепляется 25 аминокислотных остатков и образуется прогормон; далее в комплексе Гольджи от него отщепляется гексапептид и образуется активный гормон. Паратгормон упаковывается и хранится в секреторных гранулах (везикулах). В крови он транспортируется в связанном с белком состоянии. Основной стимул секреции данного гормона – низкий уровень Са2+ во внеклеточной жидкости (менее 2,0 ммоль/л). Вид рецепции данного гормона трансмембранный, через ц-3`,5`-АМФ. Органы-мишени: костная ткань, почки и кишечник. В клетках почек и костной ткани локализованы специфические рецепторы, которые взаимодействуют с паратгормоном, в результате чего инициируется каскад событий, приводящий к активации аденилатциклазы. Внутри клеток органов мишеней возрастает концентрация молекул цАМФ, действие которых стимулирует мобилизацию ионов кальция из внутриклеточных запасов. Ионы кальция активируют киназы, которые фосфорилируют особые белки, индуцирующие транскрипцию специфических генов. Биологические эффекты. В костной ткани рецепторы ПТГ локализованы на остеобластах и остеоцитах, но не обнаружены на остеокластах. При связывании паратгормона с рецепторами клеток-мишеней остеобласты начинают усиленно секретировать инсулиноподобный фактор роста 1 и цитокины. Эти вещества стимулируют метаболическую активность остеокластов. В частности, ускоряется образование ферментов, таких как щелочная фосфатаза и коллагеназа, которые воздействуют на компоненты костного матрикса, вызывают его распад, в результате чего происходит мобилизация Са и фосфатов из кости во внеклеточную жидкость. В почках ПТГ стимулирует реабсорбцию кальция в дистальных извитых канальцах и тем самым снижает экскрецию кальция с мочой, уменьшает реабсорбцию фосфатов. Кроме того, паратгормон способствует гидроксилированию 25-гидроксихолекаль-циферола в кальцитриол (1,25 (ОН)2D3). Последний усиливает всасывание Са в кишечнике. Таким образом, паратгормон восстанавливает нормальный уровень ионов Са во внеклеточной жидкости как путем прямого воздействия на кости и почки, так и действуя опосредованно (через стимуляцию синтеза кальцитриола) на слизистую оболочку кишечника, увеличивая в этом случае эффективность всасывания Са. Снижая реабсорбцию фосфатов из почек, паратгормон способствует уменьшению концентрации фосфатов во внеклеточной жидкости. Кальцитриолы (1,25(ОН)2D3 и 24,25(ОН)2D3) оказывают воздействие на тонкий кишечник, кости и почки. Подобно другим стероидным гормонам, витамин D связывается с внутриклеточным рецептором клетки-мишени. Образуется комплекс гормон-рецептор, который взаимодействует с хроматином и индуцирует транскрипцию структурных генов, в результате чего синтезируются белки, опосредующие действие кальцитриола. Так, в клетках кишечника кальцитриол индуцирует синтез Са-переносящих белков, которые обеспечивают всасывание ионов кальция и фосфатов из полости кишечника в эпителиальные клетки кишечника и далее транспорт из клетки в кровь, благодаря чему концентрация ионов кальция во внеклеточной жидкости поддерживается на уровне, необходимом для минерализации органического матрикса костной ткани. В почках кальцитриол стимулирует реабсорбцию ионов кальция и фосфатов. При недостатке витамина D нарушается образование аморфного фосфата кальция и кристаллов гидроксиапатитов в органическом матриксе костной ткани, что приводит к развитию рахита и остеомаляции. Обнаружено также, что при низкой концентрации ионов Са кальцитриол способствует мобилизации кальция из костной ткани. Кальцитриол способен также усиливать действие паратгормона на реабсорбцию кальция в почках. Кальцитонин - полипептид, состоящий из 32 аминокислотных остатков с одной дисульфидной связью. Гормон секретируется парафолликулярными К-клетками щитовидной железы или С-клетками паращитовидных желез в виде высокомолекулярного белка-предшественника. Секреция кальцитонина возрастает при увеличении концентрации Са и уменьшается при снижении концентрации Са в крови. Кальцитонин – функциональный антагонист паратгормона. Он ингибирует (через ц-3,5-АМФ) высвобождение Са из кости, снижая активность остеокластов. Кроме того, кальцитонин подавляет канальцевую реабсорбцию ионов кальция в почках, тем самым стимулируя их экскрецию почками с мочой. Скорость секреции кальцитонина у женщин сильно зависит от уровня эстрогенов. При недостатке эстрогенов секреция кальцитонина снижается. Это вызывает ускорение мобилизации кальция из костной ткани, что приводит к развитию остеопороза. Паротин – гормон белковой природы с молекулярной массой 100 кДа, вырабатывается в околоушных слюнных железах. Впервые выделен из бычьих околоушных желез. Белки, сходные с паротином, выделены также из подчелюстных слюнных желез (S-паротин), слюны (паротин А, В и С), крови, мочи. Все эти соединения способствуют развитию и росту мезенхимальных тканей, усиливают пролиферацию и кальцинацию дентина зуба. Паротин снижает содержание кальция в крови за счет стимуляции его поступления в ткани зуба, наряду с фосфатом и натрием. В регуляции роста кости то или иное участие принимают почти все другие гормоны, медиаторы и модуляторы. Простагландины, особенно ПГЕ1, снижают фосфатуритическую реакцию клеток почечных канальцев на паратгормон. Глюкокортикоиды необходимы для роста костей. В физиологических концентрациях они стимулируют обмен веществ в костной ткани, повышая чувствительность клеток к паратгормону и кальцитриолам. Инсулин активирует остеобласты и всасывание кальция в кишечнике. Поэтому при сахарном диабете I типа нарушается рост скелета и минерализация костей. Йодтиронины (Т3 и Т4) также необходимы для нормального роста костей. При их избытке активируются остеокласты и возникает гиперкальцемия. Эстрогены и андрогены принимают участие в механизмах бурного роста в пубертатном периоде. В детстве и в период полового созревания они обеспечивают преобладание процессов костеобразования над резорбцией. Процессы минерализации находятся также под контролем некоторых витаминов. Витамин С способствует созреванию коллагена через образование гидроксипролина. Зрелый протеин способен связывать ионы кальция и фосфатов, формируя кристаллы гидроксиапатита. Витамин А влияет на скорость биосинтеза гликозаминогликанов – одного из органических компонентов дентина и цемента. Из холестерола в коже под воздействием ультрафиолетовых лучей синтезируется провитамин D (кальцитриол). Функции эмали зуба. Эмаль – это бессосудистая и самая твердая ткань организма. Кроме того, эмаль остается относительно неизменной в течение всей жизни человека. Указанные свойства объясняются функцией, которую она выполняет – защищает дентин и пульпу от внешних механических, химических и температурных раздражителей. Только благодаря этому зубы выполняют свое назначение – откусывают и измельчают пищу. Структурные особенности эмали приобретены в процессе филогенеза. Явление проницаемости эмали зуба осуществляется благодаря омыванию эмали снаружи ротовой жидкостью, а со стороны пульпы – тканевой и наличию пространств в эмали, заполненных жидкостью. Возможность проникновения в эмаль воды и некоторых ионов известна с конца прошлого и начала нынешнего столетия. Так, C.F.Bedecker (1996) утверждал, что зубная лимфа может проходить через эмаль, нейтрализуя молочную кислоту и постепенно увеличивая плотность за счет содержащихся в ней минеральных солей. В настоящее время проницаемость эмали изучена довольно подробно, что позволило пересмотреть ряд ранее существовавших представлений. Если считалось, что вещества в эмаль поступают по пути: пульпа – дентин – эмаль, то в настоящее время не только установлена возможность поступления веществ в эмаль из слюны, но и доказано, что этот путь является основным. Эмаль проницаема в обоих направлениях: от поверхности эмали к дентину и пульпе и от пульпы к дентину и поверхности эмали. На этом основании эмаль зуба считают полупроницаемой мембраной. Некоторые авторы считают, что проницаемость – это главный фактор созревания эмали зубов после прорезывания.
ДЕНТИН Дентин составляет основную массу зуба. Его коронковая часть покрыта эмалью, корневая – цементом. Дентин, как ткань, относится к группе специализированных костных тканей. Поэтому в его формировании выделяют две стадии: 1. Образование межклеточного вещества – или органической фазы, которая называется предентином. 2. Минерализация предентина и превращение его в дентин. На первой стадии процесс начинается с синтеза сложных углеводов – гликозамингликанов, которые связываются с водой за пределами клеток между отростками Томса и образуют основное гомогенное вещество – обязательную часть межклеточного вещества. После этого одонтобласты начинают синтезировать молекулы коллагена I типа, которые также выходят вне клеток между отростками Томса. Таким образом, межклеточное вещество, которое выделили одонтобласты, содержит только соединения органической природы, является по консистенции мягким, податливым и называется предентином. Вторая стадия (минерализации) начинается с того момента, когда предентин достигает толщины 20-30 мкм, а затем эти стадии идут попеременно до тех пор, пока не образуется необходимая толщина дентина. Процесс минерализации регулируют сами клетки одонтобласты, которые активно захватывают из кровеносных сосудов зубного сосочка многие ионы (Са2+, Mg2+, Na+, F-, PO43- и др.). Последние транспортируются по отросткам одонтобластов в предентин, где включаются в структуру апатитов. Параллельно с этим клетки начинают выделять матриксные пузырьки, которые содержат ферменты – щелочную фосфатазу и пирофосфатазу, гидролизующие органические эфиры фосфорной кислоты и таким образом пополняющие пул неорганического фосфата в участках минерализации. Образование дентина происходит в течение всего периода функционирования зуба при наличии жизнеспособной пульпы. Дентин, образующийся после прорезывания зубов, называют вторичным. Он характеризуется меньшей степенью минерализации и большим содержанием коллагеновых фибрилл. В дентине содержится до 72% неорганических веществ и около 28% органических и воды. Неорганические соединения представлены, наряду с гидроксиапатитами и карбонатапатитами, фосфатом, карбонатом и фторидом кальция, органические - коллагеном и другими белками. Дентин построен из основного вещества и проходящих в нем канальцев, в которых расположены отростки одонтобластов и окончания нервных волокон, проникающих из пульпы. Основное вещество содержит коллагеновые фибриллы, собранные в пучки, и аморфное склеивающее вещество, химический состав которого изучен недостаточно, известно лишь, что оно включает большое количество минеральных солей. Органическая основа дентина. В отличие от эмали дентин содержит большее количество органических веществ. В основном это белки:
нерастворимые (90%) растворимые (10%) – коллаген – собственно белки дентина – структурные гликопротеины – сывороточные белки Нерастворимые протеины в основном представлены коллагеном. Последний имеет особое строение, он не набухает в воде, устойчив к воздействию коллагеназы, содержит до 12% гидроксипролина, 2,0-3,5% лизина и гидроксилизина. В его составе также присутствует большое количество глутаминовой и аспарагиновой кислот, аргинина, лейцина, изолейцина и валина, мало циклических аминокислот, отсутствует триптофан. Растворимые – это белки крови, проникающие через кровеносные сосуды. Они представлены сывороточными альбуминами, b и g-глобулинами, ферментами гликолиза, цикла трикарбоновых кислот, фосфатазами и трансаминазами. Из собственных белков дентина следует упомянуть Са-связывающие белки с молекулярной массой 11 кДа. Физиологическая роль протеинов дентина заключается в инициации минерализации, ее упорядоченности и регулируемости. Возможность влияния одонтобластов на минерализацию обусловлена тем, что проксимальный отросток этих клеток содержит митохондрии, эндоплазматический ретикулум, рибосомоподобные гранулы, т.е. элементы, характеризующие метаболическую активность. Уровень проницаемости дентина корня для большинства минеральных компонентов значительно ниже, чем дентина коронки. Данное явление можно объяснить с учетом структуры этой ткани. Известно, что дентинных канальцев в области бугров зубов человека значительно больше, чем в дентине, прилежащим к фиссурам. Ранее существовало мнение, что жидкость из пульпы поступает в дентин по отросткам одонтобластов и, выделяясь через них в пространство между отростком и стенкой трубочки, возвращается обратно. В настоящее время считают, что анатомической основы для подтверждения дентинной циркуляции нет. Состав дентинной жидкости близок к интерстициальной и включает ионы хлора, калия, натрия. В дентине также содержится около 1% лимонной кислоты, роль которой заключается в способности образовывать хелатные комплексы с кальцием для передачи его во внутрь гидроксиапатита (рис. 4).
Рис. 4. Хелатный комплекс цитрата с ионами кальция.
ЦЕМЕНТ Цемент зуба рассматривают как вариант грубоволокнистой костной ткани. В его состав входят около 70 % неорганических, 20% органических веществ и 10% приходится на воду. Из неорганических соединений преобладают гидроксиапатиты, а также соли фосфата и карбоната кальция, органические вещества представлены главным образом коллагеном, а также гликозамингликанами, липидами. В костной ткани содержится большое количество цитрата, его уровень превышает таковой в печени более, чем в двести раз. Различают клеточный цемент, расположенный в верхушечной части корня и в области его бифуркации, и бесклеточный, покрывающий остальную часть корня. Клеточный цемент содержит цементоциты, в которых выявляются достаточно большое количество РНК, гликогена и ферментов. Это свидетельствует об интенсивных обменных процессах по сравнению с другими минерализованными тканями зуба. Бесклеточный цемент не имеет цементоцитов и состоит из коллагеновых волокон и аморфного склеивающего вещества. Цемент тесно связан с дентином. В течение жизни постоянно происходит отложение цемента. При некоторых заболеваниях, например, пародонтите и периодонтите, а также при повышении нагрузки на зуб происходит интенсивное отложение цемента, при этом формируется гиперцементоз (анкилоз зуба).
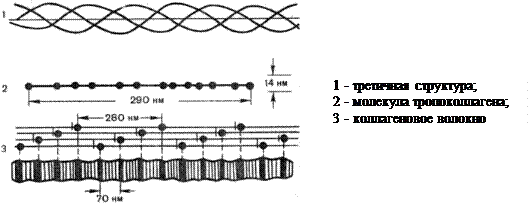
Поскольку наиболее часто нами упоминается коллаген, белок, имеющий довольно оригинальную структуру мы считаем уместным более подробно остановиться на его строении. Из всех белков, обнаруженных у высших позвоночных, коллаген наиболее распространенный: количество его в организме составляет около одной трети всего уровня белков. Сухожилия построены из параллельных пучков молекул коллагена. В отличие от a-кератинов коллаген растягивается с трудом. В настоящее время известны 19 типов коллагена, различающиеся по первичной структуре пептидных цепей, функциям и локализации в организме. Наиболее распространен 1 тип (кожа, кости, сухожилия, связки, роговица, дентин, пульпа, периодонт); 2-ой тип этого белка находится в хряще, стекловидном теле, передней части роговицы; 3-ий тип - в почках, печени, лимфатических узлах, аорте и других сосудах; 4-ый - локализуется в базальных мембранах. Отличие костного коллагена от других его видов в соединительной ткани заключается в том, что в первом имеются остатки фосфорной кислоты и дикарбоновых кислот. Характерной чертой коллагена является также то, что одну треть всех его аминокислотных остатков составляет глицин, а одну четвертую часть и более - пролин, гидроксипролин и гидроксилизин. Исключительно высокое содержание в коллагене таких аминокислот, которые нарушают a-спиральную структуру, дает основание предполагать, что коллаген не образует классическую альфа-спираль. В коллагене каждые три полипептидных цепи скручены и образуют тройную спираль (Рис. 4), при этом под влиянием регулярно располагающихся остатков пролина и оксипролина цепь принимает форму как бы ломаной спирали; это обусловливается жесткостью R-групп пролина, а также тем обстоятельством, что пептидные связи, в образовании которых участвуют пролин и оксипролин, не могут образовать водородных связей. NH-группы пептидных связей, в образовании которых участвуют остатки глицина, образуют межцепочечные водородные связи, которые также способствуют сохранению прочности структуры коллагена и делают ее устойчивой к растягиванию. Каждая полипептидная цепь коллагена имеет молекулярную массу 120000 и содержит около 1000 аминокислотных остатков. Полная трехспиральная единица называется тропоколлагеном. Тропоколлагеновые единицы уложены в волокнах коллагена в сухожилиях ступенчатым образом, чем и объясняется характерное для фибрилл коллагена расстояние между повторяющимися единицами (в зависимости от степени гидратации 600-700 А).
Рис. 4. Схема строения молекулы коллагена. Прочность коллагеновых волокон (нить сечением около 1 мм выдержавает нагрузку более 10 кг) во многом достигается за счет дополнительных ковалентных «сшивок» между молекулами тропоколллагена. Установлено, что в образовании «сшивок» участвуют главным образом, остатки лизина и гидроксилизина. Биосинтез данного протеина, осуществляемый в остео-, хондро- и фибробластах, протекает весьма сложно. Сначала его цепи синтезируются на полисомах в виде предшественников, образуя проколлаген. Затем пептидные цепочки посттрансляционно гидроксилируются и гликозилируются. Гидроксилирование проколлагена осуществляется с участием фермента протоколлаген-гидроксилазы, который в качестве кофермента использует витамин С (аскорбиновую кислоту). Негидроксилированный белок плохо секретируется из клеток, а если секретируется, то сразу же атакуется коллагеназой. Следовательно при гиповитаминозах С и Р содержание коллагена в тканях уменьшается, что в конечном итоге приводит к остепорозу. Выделяют два пути распада коллагена - специфический и неспецифический. В первом случае коллаген разрушается коллагеназой на два фрагмента, которые в дальнейшем гидролизуются лизосомальными протеазами. Во втором - протеин денатурируется продуктами свободнорадикального окисления липидов, а затем подвергается действию протеаз. Продукты специфического распада коллагена стимулируют образование новых остео-, хондро-, фибробластов, то есть обусловливают регенерацию на клеточном уровне.
В костной ткани, разновидностью которой является цемент, содержится до 1% белков, регулирующих остеогенез. К ним относятся морфогены, митогены, факторы хемотаксиса и хемоаттракции. Морфогены – это гликопротеиды, выделяющиеся из разрушающейся костной ткани и действующие на полипотентные клетки, вызывая в нужном направлении их дифференцировку. Важнейший из них – морфогенетический белок кости, состоящий из четырех субъединиц с общей молекулярной массой 75,5 кДа. Остеогенез под влиянием этого белка протекает по энхондальному типу, т.е. сначала образуется хрящ, а из него затем кость. Следует отметить, что этот протеин получен в чистом виде (США, 1983) и применяется при плохой регенерации кости. Выделен, но мало изучен фактор Тильманна (Мr=500-1000 Да), который быстро вызывает интрамембранозный остеогенез (без образования хряща), но в малом объеме. Так развивается кость нижней челюсти. Из дентина также получен морфогенетический фактор (белок), стимулирующий рост дентина. В эмали морфогенов не обнаружено. Митогены – чаще всего гликофосфопротеиды – действуют на преддифференцированные клетки, сохранившие способность к делению, увеличивают их митотическую активность. В основе биохимического механизма действия лежит инициация репликации ДНК.
|

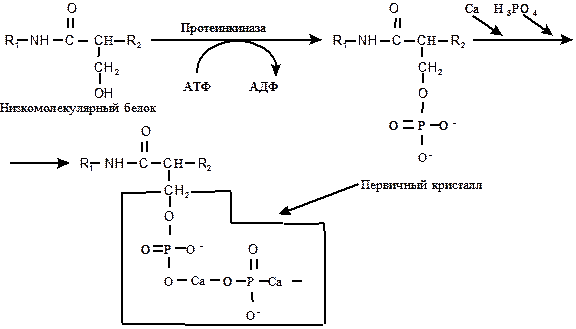
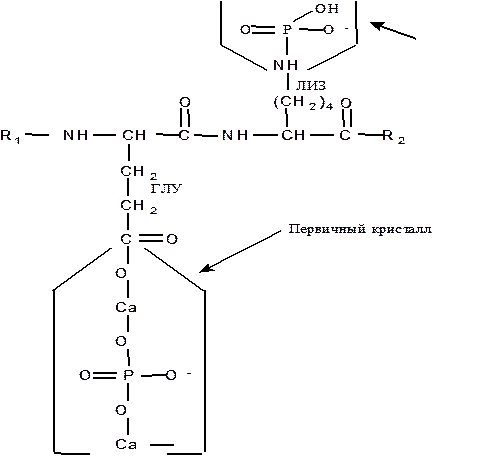

 БЕЛКИ ДЕНТИНА
БЕЛКИ ДЕНТИНА