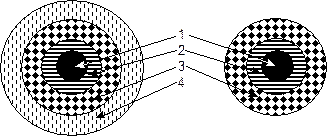II. БИОХИМИЯ ЖИДКОСТЕЙ ПОЛОСТИ РТА И ЗУБНОГО НАЛЕТА
СЛЮНА В последнее десятилетие возросло внимание исследователей к изучению свойств слюнного секрета у человека. Это связано не только с бурным развитием аналитическрй техники, но и с растущим интересом к уникальным свойствам слюны и диагностическим возможностям, связанным с ней. Особенности настоящего времени (социально-демографические причины, рост случаев инфицирования через кровь СПИДом и другими опасными заболеваниями, распространение наркомании и т.п.) делают остро необходимым поиск новых, неинвазивных и безопасных методов диагностики и контроля состояния пациентов. В этом отношении анализ слюны представляет собой одну из наиболее значимых альтернатив анализу крови, в ряде случаев не только дополняя его, но, даже, заменяя. Медиков вообще, и стоматологов, в частности, привлекают также простота взятия и анализа проб слюнной жидкости, возможность частого взятия проб, и полная безопасность при этом для здоровья пациента. Основное же внимание исследователей привлекают возможности диагностирования патологических состояний разнообразных систем организма. Слюна является одной из шести биологических жидкостей организма и играет жизненно важную роль в сохранении интеграции тканей полости рта, а именно: в отборе, проглатывании и подготовке пищи к перевариванию; в нашей способности общаться друг с другом. Функции слюны в поддержании целостности тканей полости рта обеспечиваются, прежде всего, нестимулированной (в состоянии покоя) ее секрецией, которая происходит в отсутствии внешней стимуляции (например, жевания или вкусовых раздражителей). Скорость ее выделения может быть подвержена довольно значительным суточным и сезонным колебаниям. Пик нестимулированной секреции приходится на середину дня, а в ночное время выделение слюны резко снижается. Пищеварительные функции обеспечиваются стимулированным током слюны в ходе самого приема пищи или при жевании. Стимулированная слюна отличается от нестимулированной как по скорости секреции, так и по составу. Первая характеризуется заметным преимуществом по сравнению с нестимулированной по нейтрализующей способности, минерализующему потенциалу, содержанию факторов местного иммунитета. Слюна осуществляет много функций в защите и поддержании целостности слизистой оболочки полости рта, а именно: n принимает участие в очищении полости рта от остатков пищи, налета и бактерий; n благодаря буферным свойствам, она нейтрализует отрицательное действие сильных кислот и щелочей в пределах емкости буфера; n обеспечивает поступление ионов, необходимых для реминерализации зубов; n со слюной выделяются низкомолекулярные азотсодержащие соединения (мочевина и др.), катионы, анионы, метаболиты гормонов, лекарственных препаратов и другие; n обладает противобактериальными, противогрибковыми и противовирусными свойствами. В дополнение к этому, некоторые компоненты слюны усиливают моторные функции жевания, проглатывания и произнесения звуков, а также сенсорные и хемосенсорные функции в полости рта (табл. 2). Таблица 2 Основные функции слюны в организме (Inter.Dental.J., 1992, v. 42, P. 291)
Как заметил Клод Бернар, мы распознаем функции органа, выявляя последствия его отсутствия. Важность слюны наилучшим образом демонстрируется у тех пациентов, у которых фактически слюнной секрет не поступает в полость рта. Такую отягощенную ситуацию мы находим у больных с поздними стадиями синдрома Сьегрена, который является аутоиммунным заболеванием, а также у страдающих раком, получивших в качестве лечения большие дозы облучения. У таких людей отмечается резко выраженная сухость полости рта и горла. Им очень трудно принимать пищу, они должны постоянно “потягивать” воду при жевании, у них много проблем с проглатыванием. Они жалуются на жжение в полости рта, необычные вкусовые ощущения, трудности в разговоре, на языке образуются щели и дольки. Постоянными проблемами становятся кариес и эрозия. Кариес начинает поражать нетипичные для этого заболевания поверхности зубов. Скорость секреции слюны у таких больных минимальна и иногда невозможно получить сколько-нибудь заметное количество слюны из Стенонова и Вартонова протоков. Эти изменения характерны для заключительной стадии прогрессивной гипофункции слюнных желез. Жизнь таких пациентов продолжается без секреции слюны, и становится значительно менее приятной, а для некоторых больных она становится просто непереносимой. В настоящее время стоматологи выделяют новое заболевание – «жвачную болезнь», при котором наблюдается атрофия слюнных желез вследствие неправильного использования жевательных резинок. Слюна является комплексным секретом. Ротовую жидкость обычно называют «смешанной слюной». Она первично состоит из секретов больших и малых слюнных желез. В дополнение к этому смешанная слюна содержит ряд компонентов неслюнного происхождения. К ним относятся: жидкость зубодесневой бороздки, сывороточные составляющие и клетки крови, бактерии и продукты их жизнедеятельности, слущенный эпителий и клеточные элементы, вирусы и грибки, остатки пищи и выделения из бронхов. И даже чистые секреты из больших желез, при сборе непосредственно из отверстий основных протоков околоушных, подчелюстных и подъязычных желез, содержат не только синтезированную слюну, но также и некоторые вещества, разносимые током крови, например, лекарственные препараты, гормоны и вирусы. Они достигают слюны и могут быть обнаружены в ней. Целый ряд физиологических факторов влияет на состав смешанной слюны. Важными среди них являются источник, метод сбора и степень стимулирования. Большие слюнные железы построены из разных железистых или секреторных клеток, которые запрограммированы на синтез совершенно различных секретов. Околоушные железы имеют серозные (белковые) секреторные клетки и образуют белковосодержащий водянистый секрет; слюна из подъязычных желез – мукозная (слизеподобная) и поэтому более вязкая. Подчелюстные железы имеют оба типа секреторных клеток (серозные и слизистые) и образуют слюну с более низким содержанием белка и более высокой вязкостью, чем секрет околоушных желез. Малые слюнные железы разбросаны по всей полости рта и являются чисто слизистыми железами. Они вырабатывают особенно вязкую слюну с высоким содержанием секреторного иммуноглобулина А. В ответ на стимулирование, количество выделяемой слюны может увеличиться многократно, но при этом происходит существенное изменение ее консистенции и концентрации многих компонентов. Объем и состав слюны, выделяющейся за сутки, зависит от многих факторов, в частности, от особенностей пищи. В среднем у взрослого человека суточное количество слюны составляет около 1500 мл. Однако, скорость секреции меняется в зависимости от ряда факторов: возраста (после 55-60 лет слюноотделение замедляется), нервного возбуждения («сухость во рту»), пищевого раздражителя. Во время сна слюны выделяется в 8-10 раз меньше – от 0,5 до 0,05 мл/мин, чем в период бодрствования, а при стимуляции 2,0-2,5 мл/мин. С уменьшением слюноотделения увеличивается степень поражения зубов кариесом. В практической деятельности стоматолог имеет дело только с ротовой жидкостью, так как она является средой, в которой постоянно находятся органы и ткани полости рта. Состав слюны, общая характеристика. На 99% слюна состоит из воды. Оставшийся 1% сухого остатка приходится на белки, липиды, глюкозу, мочевину и электролиты, в основном, катионы натрия, кальция, анионы хлоридов и фосфатов. Большую часть молекул органических соединений продуцируют железистые клетки, меньшую – синтезируют клетки протоков, некоторые из них транспортируются в слюну из крови. Составные вещества слюны представлены в таблице 3. Неорганические компоненты слюны. Неорганические соединения в смешанной слюне составляют 0,22% и представлены макро- и микроэлементами: Na, K, Ca, Mo, Cu, Fe, P, F, S и др. Минеральные вещества могут находиться как в ионизированной форме в виде простых ионов, так и в составе органических и неорганических соединений – солей, хелатов, белков. Важно то, что качественный и количественный состав электролитов в слюне определяет рН и буферную емкость. В то же время содержание электролитов в слюне меняется во времени и имеет циркадные ритмы. Существует тесная взаимосвязь между количеством электролитов, скоростью слюноотделения, временными колебаниями рН и температурой полости рта. Смешанная слюна имеет рН, близкий к нейтральному (6,8-7,4), что зависит от соотношения NaHPO4-/NaH2PO4, аммонийных групп (NH4+), CO2 и белка. рН слюны покоя отличается от рН стимулированной слюны. Так, нестимулированный секрет из паротидной и подчелюстной слюнных желез имеет умеренно кислый рН (5,8), который увеличивается до 7,4 при последующей стимуляции. Интересно, что этот сдвиг совпадает с увеличением в слюне ионов НСО3- и уменьшением NaH2PO4. В смешанную слюну ионы натрия и калия поступают с секретом околоушных и подчелюстных слюнных желез. Слюна из подчелюстных слюнных желез содержит 8-14 ммоль/л калия и 6-13 ммоль/л натрия. Паротидная слюна содержит больше калия - около 25-49 ммоль/л и значительно меньше натрия, всего 2-8 ммоль/л, то есть по соотношению электролитов секреты желез больше напоминают тканевую жидкость, а не сыворотку крови. Таблица 3 Компоненты слюны (Inter.Dental.J., 1992, v. 42, P. 292)
Слюна перенасыщена ионами кальция и фосфора. В ней фосфат содержится в двух формах: свободный неорганический и связанный с белками и другими соединениями. Уровень общего фосфата в слюне достигает до 7,9 ммоль/л, из них 70% приходится на долю неорганического фосфата (5,0-5,6 ммоль/л). В свою очередь неорганический фосфат представлен в виде НРО42- и Н2РО4-, которые образуют фосфатную буферную систему. Содержание ионов кальция в слюне близко к его концентрации в плазме – 2,1-2,3 ммоль/л. Этот щелочноземельный металл, как и фосфаты находится в ионизированной форме (около 50%), а остальная часть в соединении с белками, фосфатами, цитратом, карбонатом и другими анионами. Существует коэффициент отношения Са2+/Са общий, который равен 0,54. Такая концентрация кальция и фосфатов необходима для поддержания постоянства состава тканей зуба. Данный механизм поддерживается тремя основными процессами: регуляция рН, препятствие растворению зуба и внедрение ионов в минерализованные ткани. Кальций и фосфаты не выпадают в осадок, потому что основу слюны составляют мицеллы, связывающие большое количество воды, в результате чего все водное пространство оказывается связанным и поделенным между ними (Рис. 8).
А Б
Рис. 8. Строение мицеллы фосфата кальция в физиологических условиях (А) и при патологии полости рта (Б). 1 – ядро; 2 – потенциалопределяющие ионы; 3 – противоионы; 4 – диффузный слой (Леонтьев В.К. и соавт., 1991).
Молекулы фосфата кальция – [Са3(РО4)2]n - образуют нерастворимое ядро. На поверхности ядра сорбируются находящиеся в слюне в избытке молекулы гидрофосфата – НРО42-. В адсорбционном и диффузном слоях мицеллы будут находиться ионы Са2+, являющиеся противоионами. Белки, связывающие огромное количество воды (в частности муцин), способствуют распределению всего объема слюны между мицеллами, в результате чего она структурируется, приобретает высокую вязкость, становится малоподвижной. Таким образом, состав мицелл можно представить в следующем виде: {[n(Ca3PO4)2]mHPO42- (m-x)Ca2+}2х- Са2+ В кислой среде заряд мицеллы может уменьшиться вдвое и снизится устойчивость мицеллы, а ионы дигидрофосфата такой мицеллы не участвуют в процессе реминерализации. При понижении рН до 6,2 слюна становится недонасыщенной кальцием и неорганическим фосфатом и превращается в деминерализующую. Появляются ионы Н2РО4- вместо НРО42-. Подщелачивание сопровождается увеличением ионов РО43-, которые участвуют в образовании труднорастворимого соединения Са3(РО4)2, осаждающегося в виде зубного камня. Микрокристаллизация слюны. Еще в 1977г. П.А. Леус показал, что на предметном стекле после высушивания капли ротовой жидкости остается осадок, имеющий различное микроскопическое строение. Микрокристаллизация слюны имеет индивидуальные особенности и это может быть связано с общим состоянием организма, полости рта, нагрузкой питательными веществами. Образование микрокристаллов может характеризовать реминерализующую способность слюны, а интенсивность кариеса связана с типом микрокристаллизации. Различают три вида: I тип – четкий рисунок удлиненных кристаллопризматических структур, сросшихся между собой и занимающих всю поверхность капли. Этот тип присущ для компенсированной формы течения кариеса. II тип – в центре капли видны отдельные дендритные кристаллопризматические структуры меньших размеров, чем при I типе. Характерен для субкомпенсированной формы течения кариеса. III тип – по всей капле просматривается большое количество изометрически расположенных кристаллических структур неправильной формы. Этот тип микрокристаллизации характерен для декомпенсированной формы кариеса. Вместе с тем, микрокристаллизация слюны отражает состояние организма в целом, поэтому данный параметр можно использовать для экспресс-диагностики некоторых соматических заболеваний. Органические компоненты слюны, характеристика. Как видно из таблицы 2 смешанная слюна содержит белки, полипептиды, липиды, витамины, гормоны, органические кислоты. Количество их зависит от состояния организма, ротовой полости и различается по количественным оценкам в осадке слюны и надосадочной жидкости. В слюне определяется от 1,5 до 4,0 г/л белка. Методом двумерного электрофореза определено около 500 пятен, характеризующих различные протеины, но только 120-150 являются продуктом слюнных желез, а остальные имеют бактериальное и клеточное (чаще лейкоцитарное) происхождение. Большая часть белков слюнных желез вырабатывается секреторными клетками и делится на несколько классов. Каждый класс имеет определенное число отличающихся, но близко связанных членов (генетический полиморфизм). Они включают: богатые пролином белки; гистатины; пептиды богатые тирозином; муцины – низко- и высокомолекулярные; амилазы (альфа и гамма); а также несколько пероксидаз слюны. Содержание общего белка в слюне практически здоровых людей составляет в среднем 187,71 + 10,9 мг/дл, тогда как у больных язвенной болезнью желудочно-кишечного тракта до лечения этот показатель достоверно повышается. Другие протеины слюны существуют в гомогенной форме. Некоторые белки продуцируются секреторными клетками, остальные – клетками протоков. К железистым белкам относятся фактор роста эпителия, секреторный компонент и лактоферрин. Лизоцим продуцируется клетками протоков. Вместе с тем точное место происхождения многих компонентов до сих пор неизвестно. К компонентам, транспортируемым прямо из кровотока в слюну, относится альбумин, иммуноглобулины G, А и М, витамины, лекарственные препараты, гормоны, электролиты и вода. Отмечена хорошая корреляция по уровням ряда гормонов и лекарств между плазмой крови и слюной. Это обстоятельство явилось основой предложений использовать анализы слюны как неинвазивный метод динамического контроля уровня гормонов, терапевтических средств и запрещенных к употреблению препаратов. Многие белки и другие компоненты слюны защищают мягкие и твердые ткани полости рта. Муцины слюны покрывают и смазывают поверхности слизистой оболочки. Их крупные молекулы предотвращают прилипание бактерий и колонизацию, защищают ткани от физического повреждения и позволяют им устоять перед тепловыми перепадами. Некоторые из протеинов, такие как лизоцим, обладают способностью разрушать стенку бактериальных клеток; другие, как гистатин, лактоферрин и лактопероксидаза угнетают рост микробов; третьи – антитела слюны, например, секреторный иммуноглобулин А и липаза слюны, могут защищать зубы от кариеса. Ниже мы остановимся на характеристике наиболее значимых соединений. Гликопротеины слюны. Большинство белков слюны относится к данному классу, причем углеводная компонента довольна вариабельна как в количественном (от 4 до 40%), так и в качественном отношении. Синтез протекает в две стадии: вначале образуется белковое ядро, к которому присоединяется углеводная цепь. Последних может быть несколько. В условиях стимуляции могут синтезироваться неполноценные гликопротеины и слюна становится менее вязкой. Наиболее изучены из данных макромолекул муцин, иммуноглобулины и группоспецифические вещества. Муцин. С ним прямо связана вязкость слюны. Муцины входят также в состав секретов бронхов и кишечника, семенной жидкости и выделений шейки матки. Все они играют роль смазки и защищают подлежащие ткани от повреждений как механических, так и химических. В полипептидной цепи муцина из подчелюстной слюнной железы содержится большое количество треонина и пролина. К радикалам треонина через образование О-гликозидной связи присоединяются молекулы N-ацетилнейраминовой кислоты, N-ацетилгалактозамина, фукозы и галактозы. Сам белок напоминает по своему строению гребенку (так называемые щеточные структуры): короткие углеводные цепи, как зубья торчат из жесткой, богатой пролином полипептидной цепи, которые соединяются между собой дисульфидными мостиками и образуются большие молекулы с особыми вязкими свойствами. Муцин способен адсорбироваться на поверхности зуба, образуя нерастворимую пленку, имеющую слабый отрицательный заряд. Муцин легко преципитируется на зубах, особенно при низком значении рН. Кроме того, он может образовывать комплексы с липидами и при взаимодействии с мембранами эпителиальных клеток участвовать в построении пелликулы. Последняя выполняет роль селективного фильтра и барьера, обеспечивающего защиту подлежащих клеток, предотвращающего высушивание и контролирующего проницаемость слизистой оболочки. Защитные качества пелликулы зависят от размера мукоидного геля. Однако муцин также легко адсорбирует на своей поверхности и микроорганизмы, метаболиты которых, в конечном итоге, могут привести к деминерализации эмали. Содержание муцина в слюне здоровых людей составляет 75,4 + 8,8мг/дл. Иммуноглобулины слюны. В ней присутствуют все 5 классов: IgA, IgG, IgD, IgM, IgE, которые различаются по молекулярной массе, конфигурации и углеводной компоненте, но вторичная структура у всех этих соединений одинакова: 2 легких (L) и 2 тяжелых (Н) цепи, аминокислоты в которых упакованы в домены. Иммуноглобулины как правило поступают из сыворотки и с секретом слюнных желез. Исключение составляет IgA2 (IgAs), который синтезируется в околоушных (90%) и подчелюстных (10%) слюнных железах. Его концентрация в слюне в 100 раз выше по сравнению с IgG и IgM. Он отличается от других более высокой молекулярной массой, что связано с появлением дополнительных пептидов. Два четырехцепочечных мономера Н и L цепей образуют димер, в состав которого также входят секреторный гликопротеид (SP) и добавочный полипетид (J-цепь) (рис. 9). Показано, что H, L и J цепи синтезируются в плазменных клетках интерстициальной ткани слюнных желез. При поступлении белка в ацинарные клетки он соединяется с гликопротеидом SP, который синтезируется серозными эпителиальными клетками. Такая структура предохраняет молекулу иммуноглобулина от разрушающего действия многочисленных ферментов, находящихся в секретах слизистых оболочек. Механизм действия IgAs заключается в том, что он активирует альтернативным путем комплемент, что в свою очередь приводит к лизису микроорганизмов. IgAs препятствует адгезии бактерий к эпителиальным клеткам, затрудняя тем самым колонизацию их на слизистой.
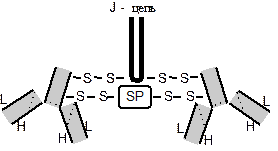
Рис. 9. Схема строения секреторного иммуноглобулина А: Н – тяжелая цепь; L – легкая цепь; SP – секреторный компонент.
Группоспецифические вещества слюны в отличие от эритроцитарных содержат 85% углеводов и 15% белка. Антигенная специфичность веществ определяется конформацией некоторых остатков сахаров, расположенных на концах углеводных цепей. Концентрация группоспецифических веществ в слюне равна 10-130 мг/л. Они в основном поступают с секретом слюнных желез и точно соответствуют группе крови. Исследование группоспецифических веществ в слюне используется в судебной медицине для установления группы крови в тех случаях, когда это невозможно сделать иначе. Кроме того, в слюне обнаружено несколько специфических белков, характеризующихся преобладанием одной или нескольких аминокислот. К ним относятся белки, богатые пролином (PRP), пептиды, богатые тирозином – стайзерины, белки, богатые гистидином – гистатины и цистатины – белки, богатые цистеином. Белки, богатые пролином (PRP), были открыты Оппенгеймером в 1971 году в паротидной слюне и составляют до 70% от общего количества всех белков в этом секрете. Молекулярная масса их колеблется от 6 до 12 кДа, 75% от всего числа аминокислот в данных соединениях приходится на пролин, глицин, глутаминовую и аспарагиновую аминокислоты. В полости рта PRP выполняют несколько функций. Они легко адсорбируются на поверхности эмали и являются компонентами приобретенной пелликулы зуба, задерживая его деминерализацию и ингибируя излишнее осаждение минералов. Таким образом поддерживают постоянство кальция и фосфора в эмали зуба. Они могут связывать определенные микроорганизмы и участвуют тем самым в формировании микробных колоний бляшки. PRP необходимы для смачивания пищевого комка. Гистатины – основные олигопептиды, включающие 12 подклассов. Полностью установлена их первичная структура и показано, что они состоят из 7-38 аминокислотных остатков. Сравнение последовательности аминокислот в различных гистатинах выявило большую степень сходства между ними и только гистатины подклассов 1 и 2 значительно отличаются от других членов этого семейства белков. Считается, что гистатин 2 является фрагментом гистатина 1, а гистатины 4-12 образуются при гидролизе гистатина 3. Этот ограниченный протеолиз протекает при участии слюнного калликреина и некоторых других протеиназ. Это образование происходит либо в секреторных везикулах, либо при прохождении белков через железистые протоки. Гистатин 1 участвует в образовании приобретенной пелликулы зуба. Он также является мощным ингибитором роста кристаллов гидроксиапатита, что необходимо для стабилизации растворенных минералов в жидкостях полости рта. Смесь частично очищенных гистатинов вызывала усиление гликолитической активности части выделенных бактерий полости рта и подавляла рост некоторых видов Str. mutans. Гистатин 5 вовлечен в процесс подавления слюной вируса иммунодефицита и грибков (Candida albicans). Одним из механизмов такого антимикробного и антивирусного действия является взаимодействие гистатина 5 с различными протеиназами, выделенными из микроорганизмов ротовой полости. Стайзерины – группа пептидов, богатых тирозином. Эти соединения представляют собой фосфопептиды, состоящие из 40-43 аминокислот. Они (от англ. sthaiser - прилипать) вместе с другими секреторными протеинами ингибируют спонтанную преципитацию фосфорнокальциевых солей на поверхности зуба, в ротовой полости и в слюнных железах. Цистатины были открыты в 1984 году. Они синтезируются в серозных клетках околоушных и подчелюстных слюнных желез. Всего обнаружено 8 типов, из них 6 белков охарактеризовано – это цистатин S, удлиненные его формы – S-HSP-12, SA, SN, SAI, SAIII. Цистатины – это кислые белки с молекулярной массой 9,5-13 кДа. Они ингибируют активность цистеиновых протеиназ, к которым относятся катепсины В, Н, L и другие протеиназы, у которых в активном центре присутствует остаток цистеина. Помимо ингибирующей активности цистатин SAIII содержит 4 остатка фосфосерина и предполагается, что они вовлекаются в связывание фосфорнокальциевых соединений с эмалью зуба. Часть этих белков находится в приобретенной пелликуле зуба. Высокая адгезивная способность цистатинов SАI и SAIII связана с тем, что они имеют сходство в аминокислотной последовательности с фибронектином и ламинином. Через ингибирование активности цистеиновых протеиназ слюнные цистатины выполняют свою антимикробную и антивирусную функцию. Кроме того, они защищают белки слюны от энзиматического расщепления ферментами микроорганизмов. Альбумин. В смешанной слюне этот белок определяется в небольшом количестве, его происхождение пока остается неясным. Из слюнных желез в слюну поступают биологически активные соединения, к ним относятся фактор роста эпидермиса, фактор роста нервов, фактор роста мезодермы, эритропоэтин, ренин и некоторые другие. Ферменты слюны. В смешанной слюне представлены пять оcновных групп ферментов: карбоангидразы, эстеразы, протеолитические, переноса и смешанная группа. Всего определяется активность более 100 ферментов. По происхождению ферменты делятся на три группы: секретируемые паренхимой слюнной железы, образующиеся в процессе ферментативной деятельности бактерий и образующиеся в процессе распада лейкоцитов в полости рта. В связи с обнаружением в слюне и ротовой жидкости человека секретируемых из крови ферментов (пепсиноген, трипсиноген) было обнаружено, что слюна и кровь содержат несколько изоформ амилазы, доказано их происхождение из разных желез-продуцентов и существенные изменения при многих гастроэнтерологических заболеваниях. Полученные результаты свидетельствуют о гетерогенности a -амилазы ротовой жидкости и слюны и о повышении саливадиагностической информативности определения в них не только общей амилолитической активности, но и s- и p- a -амилазы с применением высокоселективного ингибитора s- a -амилазы человека. Гликозидазы: a-амилаза и лизоцим. Слюнная a-амилаза расщепляет 1-4 гликозидные связи в крахмале и гликогене. По своим иммунохимическим свойствам и аминокислотному составу слюнная альфа-амилаза очень сходна с панкреатической. У обеих определяется 94% сходства в аминокислотной последовательности, но кодируются они различными генами (АМУ1 и АМУ2). Амилаза является сложным белком с четвертичной структурой. Ее изоферменты из 11 белков можно объединить в 2 семейства. Белки семейства А имеют молекулярную массу 62 кДа и содержат остатки углеводов, а изоэнзимы В лишены углеводного компонента и имеют М.м. 56 кДа. В смешанной слюне идентифицирован фермент, который путем дегликозилирования изоамилаз А превращает их в семейство В. Амилаза выделяется с секретом паротидной железы, где концентрация ее составляет 648-803 мкг/мл и не зависит от возраста, но меняется в течение суток и в зависимости от чистки зубов и приема пищи. Лизоцим гидролизует гликозидную связь между С-1 N-ацетилмурамовой кислоты и С-4 N-ацетилглюкозамина, которые формируют полисахарид клеточной стенки бактерий. Фермент представляет собой одну полипептидную цепь из 129 аминокислотных остатков и массой 14,6 кДа. Стабильность фермента обеспечивают четыре поперечных дисульфидных мостика. Лизоцим определяется также в десневой жидкости, слезах, курином белке, что обеспечивает формы неспецифической антибактериальной защиты. Активность этого фермента в ротовой полости может уменьшаться при тяжелых формах пародонтита. Другие гликозидазы. В смешанной слюне определяется активность нескольких гликозидаз – это a-L-фукозидаза, a- и b-гликозидаза, a- и b-галактозидаза, a-D-маннозидаза, b-глюкуронидаза, b-гиалуронидаза, нейраминидаза, b-N-ацетилгексозаминидазы. Все они имеют различное происхождение и свойства. a-L-фукозидаза выделяется с секретом околоушной железы и расщепляет a-1,2 связи в коротких олигосахаридных цепях. b-N-ацетилгексозаминидаза содержится в секретах больших слюнных желез, а также образуется смешанной культурой микрофлоры полости рта. Остальные имеют бактериальное происхождение и наиболее активны в кислой среде. Пероксидазы. В цельной смешанной слюне определяются две разных группы слюнной пероксидазы. Ферменты с изоэлектрической точкой в щелочной среде образуются в околоушной и подчелюстной слюнных железах, и представлены множественными формами с молекулярной массой 78, 80 и 28 кДа. Это гемопротеиды, однако в своем составе содержат и углеводы (4,6%). Энзимы находятся в комплексе с одним из белков, богатых пролином. Бактерии зубной бляшки, мелкие слюнные железы и эпителиальная выстилка слизистой оболочки полости рта вообще лишены этого фермента. Данная пероксидаза катализирует окисление роданидов (тиоцинатов, -SCN) в присутствии Н2О2 с образованием НOSCN и гипотиоцината (-OSСN). Антибактериальная активность последнего в 10 раз выше, чем у Н2О2. Из гипотиоцианта в дальнейшем спонтанно генерируются активные формы кислорода, которые разрушают липиды клеточных мембран микроорганизмов. Наибольшее окисление роданидов протекает при рН=5-6. При этом создается опасность деминерализации твердых тканей зуба. Миелопероксидазапоступает в слюну преимущественно из азурофильных гранул полиморфноядерных лейкоцитов. Этот фермент, образуя энзим-субстратный комплекс с пероксидом водорода, окисляет анионы галогена (Cl-, Br-, I-) и образует ионы гипохлорита (-OCl), хлоридиума (Cl+) и молекулы хлора. При взаимодействии гипохлорита с Н2О2 образуется активная форма кислорода – синглентный (1О2), обладающая антибактериальным и антивирусным эффектами. Повышение уровня миелопероксидазы в слюне отражает, в основном, процесс развития лейкоцитарно-эндотелиального дисбаланса в его крайнем выражении, прорыве гисто-гематического барьера и имбибиции тканей пародонта активированными лейкоцитами, активно высвобождающими миелопероксидазу в окружающую среду. Значение изменений активности миелопероксидазы для диагностики тяжести поражения пародонта подтверждается и наличием зависимости ее содержания в слюне от степени тяжести пародонтита. При этом регистрируется отчетливая зависимость между тяжестью пародонтита и профилем активности фермента в слюне. Отражая степень лейкоцитарной инфильтрации в ткань и степень поражающего эффекта на тканевые структуры, активность миелопероксидазы в слюне может считаться одним из критериев, позволяющих оценить прогрессирование деструктивных процессов в тканях пародонта. Щелочная и кислая фосфатазы отщепляют неорганический фосфат от органических соединений. Кислая фосфатаза в смешанную слюну попадает с секретом больших слюнных желез, а также бактерий, лейкоцитов и эпителиальных клеток. В слюне определяется до 4 изоферментов кислой фосфатазы. Щелочная фосфатаза, оптимум рН которой 9,1-10,5, также определяется в смешанной слюне. Активность фермента очень низка в секретах слюнных желез и ее происхождение в слюне связывают с клеточными элементами. Активность обоих энзимов в слюне, как правило, увеличивается при пародонтите, гингивите. Противоречивые данные об изменении скорости гидролиза фосфорных эфиров получены при кариесе. Вместе с тем выявлено, что повышенная растворимость эмали при использовании реминерализующей терапии совпадает с высокой активностью щелочной фосфатазы. В слюне определяется невысокая активность протеиназ и их ингибиторов, оптимум рН которых находится и в кислой и в слабощелочной среде. К ним относятся калликреин и другие трипсиноподобные протеиназы, катепсины D, В, а также a1-ингибитор протеиназ, a2-макроглобулин и другие. Основная их функция – регулируемый ограниченный протеолиз белков с образованием активных форм белка или активных олигопептидов. Нуклеазы ротовой жидкости (ДНК-аза, РНК-аза) участвуют в расщеплении нуклеиновых кислот. Биологическая роль данных ферментов заключается в деградации полинуклеотидов бактерий и вирусов, что играет существенную роль в защите организма от проникновения инфекционного фактора через полость рта. В слюне также содержатся ферменты, участвующие в свертывании крови и фибринолизе: плазмин, активаторы плазминогена, ингибиторы фибринолиза, факторы обладающие тромбопластической активностью. Полагают, что все эти энзимы играют роль в образовании фибрина и регенерации ран слизистой полости рта. Липиды. Их общее содержание невелико. Оно колеблется и считается, что большая их часть поступает с секретом околоушной и подчелюстной желез и только 2% из плазмы и клеток. Количество общих липидов в нестимулированном секрете околоушной железы не превышает 60-70 мг/л. Часть липидов представлена свободными насыщенными и ненасыщенными высшими жирными кислотами – пальмитиновой, стеариновой, олеиновой, эйкозапентаеновой. Кроме того, в слюне присутствует свободный холестерин и его эфиры (около 28% от общего количества), триацилглицеролы (примерно 50%) и, в очень небольшом количестве, глицерофосфолипиды. Углеводы в слюне находятся в комплексе с белками. Уровень глюкозы в слюне в норме составляет 0,06-0,17 ммоль/л. Слюна содержит также мочевину (1,7-6,7 ммоль/л), лактат, пируват, тиоцинаты (роданиды), нитраты, нитриты. Последние два поступают в слюну с пищей, водой, табачным дымом, где при участии нитратредуктазы бактерий нитраты превращаются в нитриты, которые в свою очередь могут вступить в реакцию со вторичными аминами (аминокислоты, нуклеотиды, лекарственные препараты) с образованием канцерогенных нитрозосоединений. Эта реакция протекает в кислой среде, а ускоряют ее тиоцианаты. Показано, что при лейкоплакии слизистой полости рта у курильщиков и лиц, занятых в табачном, производстве в слюне растет количество нитритов и активность нитратредуктазы. Кроме того, содержание роданидов в слюне у курильщиков в 2-10 раз превышает таковое у некурящих людей (в норме – 0,5-1,2 ммоль/л), их уровень также может увеличиваться при воспалении пародонта. В слюне определяется подавляющее большинство стероидных гормонов – эстрогены, андрогены, прогестерон, глюко- и минералокортикоиды. Уровень половых гормонов у женщин меняется в зависимости от фазы менструального цикла. Исследование стероидных гормонов в слюне используется для оценки влияния контрацептивов на эндокринную систему женщины. По гормональному профилю слюны можно судить о приеме стероидных анаболиков. Одним из защитных механизмов полости рта, обеспеченных компонентами ротовой жидкости, наряду с указанными выше (иммуноглобулины, пероксидазы, протеазы, нуклеазы, факторы гемостаза и фибринолиза и другие), служит образование приобретенной пелликулы зуба, которая лежит под слоем зубного налета. Это очень тонкая органическая пленка, являющаяся структурным элементом поверхностного слоя эмали. Она не исчезает в процессе жевания и может быть удалена лишь при воздействии сильных абразивных агентов. Пелликула появляется после прорезывания зубов и в ее образовании участвуют главным образом белки ротовой жидкости. Муцины, имея кислый характер и высокое сродство к гидроксиапатиту эмали, притягиваются к поверхности зуба, также как и кислые белки, богатые пролином, - эти протеины составляют основную структурную часть пелликулы. Она, выступая в роли ионообменника, регулирующего поступление ионов кальция и фосфата, препятствует избыточному их осаждению из перенасыщенной солями слюны. Жевание и наличие микроорганизмов в полости рта создают основу для прикрепления бактерий к белкам пелликулы и инициирует рост зубного налета. Ограничение роста последнего и повреждающего действия микроорганизмов на твердые ткани зуба связано с присутствием белков слюны, таких как гистатины и цистатины, которые обладают антибактериальным и антивиру
|