Зависимость давления насыщенных паров от температуры
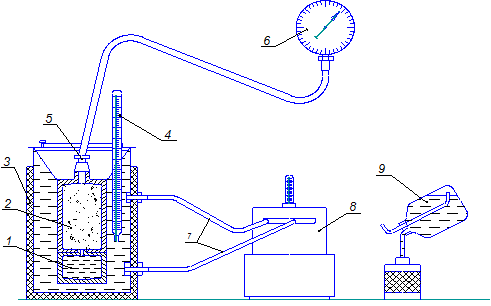
Прибор для определения давления насыщенных паров топлива (рис. 1.3) состоит из топливной 1 и воздушной 2 металлических камер цилиндрической формы, соединенных между собой резьбой. Воздушная камера, предназначенная для паровой фазы, соединена при помощи резиновой трубки и пружинного зажима (крана) 5 с манометром-вакуумметром 6. При проведении опытов прибор помещается в водяную баню 5, соединенную двумя шлангами 7 с термостатом 8. Заданная температура воды поддерживается термостатом и контролируется по ртутному термометру 4, погруженному в баню до отметки 38 °С, с пределами измерений от 0 до 50 °С и ценой деления шкалы 0,1 градуса [22]. На позиции 9 показана схема заполнения топливной камеры. Так как давление насыщенных паров зависит от температуры и состояния жидкой и паровой фаз, ГОСТ 1756–52 предусматривает определение этой величины при температуре 38 °С и соотношение фаз 1:4 (жидкость – газ). Перед началом опыта сосуд рассоединяют, шланг должен быть зажат зажимом. В топливную камеру заливают бензин и охлаждают его до температуры 0 °С. Затем соединяют топливную камеру с воздушной. Собранный сосуд поворачивают и сильно встряхивают несколько раз. Приводят сосуд в нормальное положение, опускают его в баню с температурой t = 38 °С. После погружения сосуда в баню открывают зажим и через 5 мин. определяют давление или разрежение по показанию манометра-вакуумметра. Указанные выше операции повторяют до тех пор, пока значение давления по манометру не стабилизируется. При стабилизации давления достигается термодинамическое равновесие, когда жидкость (бензин) уже не испаряется, а газ (пар) не конденсируется. Стабилизированное давление и есть давление насыщенных паро в. При снижении давления жидкие углеводородные топлива могут переходить в газообразное состояние.
Рис. 1.3. Схема прибора для определения давления насыщенных паров: 1 – топливная камера; 2 – воздушная камера; 3 – водяная баня; 4 – термостат; 5 – пружинный зажим; 6 – манометр; 7 – шланги; 8 – термостат; 9 – схема заполнения топливной камеры Следует помнить, что если манометр показывает избыточное давление, например, плюс 0,1∙105 Па, то абсолютное давление будет равно 1,1∙105. Если вакуумметр показывает установившееся разрежение минус 0,2∙10 5 Па, то абсолютное давление равно 0,8∙105 Па или 80 кПа. В соответствии с ГОСТ 1756–2000 (ISO – 3007–99) «Нефтепродукты, определение давления насыщенных паров» давление насыщенных паров определяют с использованием водяной лабораторной бани типа ПЭ–700 и набора бомб ПЭ–7100 с комплектами манометров марки МТИ–1218. На рис. 1.4 показан современный прибор для определения давления насыщенных паров. Прибор состоит из манометра с ручкой, которая служит для поворота и его встряхивания, воздушной и топливных камер. В процессе определения давления насыщенных паров прибор находится в водяной бане, в которой поддерживается постоянная температура. Вязкость – способность жидкости оказывать сопротивление при относительном движении её слоёв. Согласно закону Ньютона сила внутреннего трения между слоями жидкости определяется выражением:
где S – площадь соприкасающихся слоев, м2;
Рис. 1.4. Бомба типа ПЭ-7100 для определения давления насыщенных паров
Анализ формулы 1.7 показывает, что коэффициент динамической вязкости Кинематическая вязкость: ν = С· Δ τ = 10·0,1 = 1 мм2/с или 1 сСт. Определив кинематическую вязкость, м2/с, можно оценить динамическую вязкость, Па∙с. Для этого величину кинематической вязкости, м2/c, умножают на плотность жидкости, кг/м3, (μ = υ ×ρ;). Кинематическая вязкость в м2/с применяется для оценки зависимости вязкости жидкости от температуры при определении режимов движения (ламинарное или турбулентное) и расчете потерь энергии при движении жидкости в местных сопротивлениях и по длине. Для измерения кинематической вязкости в диапазоне 0,3–5000 сСт применяют автоматическое программно-управляемое устройство Динамическая вязкость, Н∙с/м2 (Па∙с), применяется при расчете сил трения, например, между подшипниками скольжения и шейками коленчатого вала двигателя. В холодное время года вязкость моторного масла резко повышается, силы трения достигают величины, при которой затрудняется вращение коленчатого вала и запуск двигателя. При кинематической вязкости моторного масла более 3000 сСт запуск двигателя затруднен. Расход жидкости или газа – это количество жидкости (газа), протекающее за единицу времени через данное живое сечение. Различают расход объёмный (м3/с) и массовый (кг/с).
Сжимаемость жидкости (газа) – её способность уменьшаться в объёме при повышении давления. Оценивается коэффициентом объёмного сжатия (м2/Н):
где V – первоначальный объём системы;
Величина, обратная β;, – модуль упругости: К = 1/ β;. Для воды величина В любой замкнутой системе (насос, цилиндр) создаваемое давление определяется по формуле:
Величину давления Δ Р ограничивают при помощи перепускных или предохранительных клапанов. Оптимальная величина Δ Р выбирается с учётом назначения конструкции исполнительного механизма, например, насоса для перемещения нефтепродукта и создания необходимого давления. Состав и свойства топлив нефтяного происхождения изменяются в зависимости от температуры и давления. Углеводороды, содержащие от 1 до 4 атомов углерода, при нормальных атмосферных условиях являются газами. При повышении давления молекулы газа укрупняются и переходят в жидкое состояние. Бутан (С4Н10) переходит в жидкое состояние при повышении давления до 0,8 МПа. При понижении давления до величины атмосферного сжиженный бутан переходит в газообразное состояние. Данное свойство газов используется при создании систем питания двигателей, работающих на сжиженном газе (пропан-бутановая смесь газа). При нормальных атмосферных условиях (Т = 273 К, Р = 760 мм рт. ст.) диаметр молекул газа одинаков и составляет 2∙10-10 м. Массу молекулы малых размеров определить трудно. В 1811 г. итальянский физик Авогадро (1776 – 1856) предположил, что одинаковый объем газа (любого типа) при одинаковом давлении и температуре должен содержать равное количество молекул. Опыты показывают, что 1 грамм атомов Н (водорода) содержит 6∙10 23 атомов. Масса молекул газа, кг, содержащая в объеме 22,4 литра при Р = 760 мм рт. ст. (1∙10 5 Па) и Т = 273 К (t = 0 °С), называется молем. Моль (молекулярная масса) – количество вещества в определенном объеме. Если количество молекул, равное 6∙1023, компактно упаковать, то их объем составит 22,4 литра. Количество молекул, равных 6∙10 26, займут объем, равный 22,4 м3. Плотность воздуха при атмосферных условиях равна 1,29 кг/м3. В объеме, равном 22,4 м3, его масса составит 28,9 кг (1,29 ∙22,4 = 28,9). Один киломоль воздуха равен 28,9 кг. Один моль воздуха составит 0,0289 кг или 28,9 г. Киломоль – количество газа, масса которого в кг численно равна его молекулярной массе. В воздухе по массе содержится 23 % (0,23) кислорода О2 и 77 % (0,77) азота N2.. Молекулярная масса кислорода 32, азота 28. Молекулярная масса воздуха Для полного сгорания 1 кг бензина требуется 14,45 кг воздуха или 0,5 киломолей воздуха. В тепловом расчете двигателя внутреннего сгорания требуемое количество воздуха для сгорания 1кг топлива определяют в кг или в киломолях. При определении потерь нефтепродуктов от испарения и «дыханий» резервуаров необходимо знать плотность испарившихся легких фракций. Для этого определяют молекулярную массу испарившегося нефтепродукта в кг/кмоль. В таблице 1.4 показано изменение молекулярной массы нефтяных фракций в зависимости от температуры начала кипения в оС.
Таблица 1.4
|

 (1.7)
(1.7) – коэффициент динамической вязкости, (Н·с/м2 = Па·с);
– коэффициент динамической вязкости, (Н·с/м2 = Па·с); – градиент скорости, характеризующий относительное изменение скорости между отдельными слоями жидкости, 1/с.
– градиент скорости, характеризующий относительное изменение скорости между отдельными слоями жидкости, 1/с.


 , м2/с. Для воды: 1·10-6, м2/с. Вязкость измеряют в стоксах или сантистоксах (1Ст = 1см2/с; 1сСт = 1 мм2/с). Эталоном кинематической вязкости в 1 cСт является дистиллированная вода при 20 °С. Вязкость любой жидкости можно определить при помощи капиллярного вискозиметра (см. рис. 1.5). Он представляет собой U-образную прозрачную трубку с капилляром, над которым расположены две шарообразных емкости.
, м2/с. Для воды: 1·10-6, м2/с. Вязкость измеряют в стоксах или сантистоксах (1Ст = 1см2/с; 1сСт = 1 мм2/с). Эталоном кинематической вязкости в 1 cСт является дистиллированная вода при 20 °С. Вязкость любой жидкости можно определить при помощи капиллярного вискозиметра (см. рис. 1.5). Он представляет собой U-образную прозрачную трубку с капилляром, над которым расположены две шарообразных емкости.  (1.8)
(1.8) (1.9)
(1.9) V – изменение объёма;
V – изменение объёма; (1.10)
(1.10) кг/ кмоль.
кг/ кмоль.


