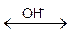Электролитов
Амфотерные электролиты являются слабыми электролитами. Способность амфотерных электролитов практически полностью реагировать как с кислотами, так и со щелочами, образуя и в том, и в другом случае соли, связана с двойственным характером ихдиссоциации. В растворах амфотерных электролитов устанавливается сложное гетерогенное равновесие между осадком и раствором. Например, диссоциацию амфотерного электролита – гидроксида алюминия можно выразить схемой:
Если к раствору гидроксида алюминия добавлять кислоту(увеличивать концентрацию катионов водорода Н+), равновесие будет смещаться в сторону диссоциации по основному типу. Гидроксид алюминия будет вести себя как основание. Этот процесс может быть выражен уравнением Al(OH)3 + 3HCl = AlCl3 + 3H2O. Ионно-молекулярные уравнения: Al(OH)3 + 3H++ 3Cl- = Al3++ 3Cl-+ 3H2O; Al(OH)3 + 3H+ = Al3++ 3H2O. Если к раствору Al(OH)3 добавлять щелочь, то увеличивается концентрация гидроксид-ионов (ОН-) и равновесие диссоциации гидроксида алюминия будет смещаться в сторону диссоциации по кислотному типу. Гидроксид алюминия будет вести себя как кислота: Al(OH)3 + NaOH = NaAlO2 + 2H2O; Al(OH)3 + Na++ OH- = Na++ AlO2-+ 2H2O; Al(OH)3 + OН- = AlO2- + 2H2O. В щелочных растворах алюминий находится в виде иона [Al(OH)4]-, ион AlO2- обнаружен только в растворах с рН>13, поэтому последнюю реакцию можно записать в следующем виде: Al(OH)3 + NaOH = Na[Al(OH)4]; Al(OH)3 + Na++ OH-= Na+ + [Al(OH)4]-; Al(OH)3 + OH-= [Al(OH)4]-. Таким образом, проявление амфотерными электролитами двойственных свойств кислоты и основания объясняется смещением равновесия при введении в раствор одноименных ионов.
|