Тема 3. Строение атома и периодический закон
Пример 1. Хлор имеет изотопы с массовыми числами 35 и 37. Укажите для каждого изотопа порядковый номер, число протонов и нейтронов, заряд ядра. Определите массовую долю в нем изотопа с массовыми числами 35 и 37, приняв атомную массу хлора 35, 453. Решение. Изотопы хлора имеют одинаковый порядковый номер 17, следовательно, и одинаковый заряд ядра — 17 протонов, а так как атом электронейтральный, то 17 электронов. Согласно протонно-нейтронной теории, у изотопа хлора
Следовательно, хлор содержит 77, 4% изотопа Пример 2. Напишите схему распределения электронов в атоме хлора, его электронную и электронно-графическую формулы. Решение. Хлор расположен в третьем периоде, следовательно, у его атома три энергетических уровня. Хлор находится в VII группе главной подгруппы, поэтому число электронов на последнем уровне равно семи. Число электронов на остальных уровнях определяется по формуле N = 2n2, т. е. 2и8. Следовательно, схема строения атома хлора K L M
электронная формула хлора
электронно-графическая формула
Пример 3. Дайте характеристику элемента хлора и его соединений (с кислородом и водородом) на основании его положения в периодической системе элементов. Решение. Хлор расположен в VII группе главной подгруппы. Хлор — неметалл. На последнем энергетическом уровне семь электронов, высшая степень окисления в кислородных соединениях равна семи. Высший оксид имеет формулу
|

 будет 18 нейтронов (35—17), а у изотопа с массовым числом 37 — 20 нейтронов (37—17). Если обозначить массовую долю (в %) изотопа
будет 18 нейтронов (35—17), а у изотопа с массовым числом 37 — 20 нейтронов (37—17). Если обозначить массовую долю (в %) изотопа  — через (100—х), то можно составить уравнение
— через (100—х), то можно составить уравнение , откуда x = 77, 4%
, откуда x = 77, 4% 2 8 7
2 8 7


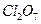 — кислотный, гидроксид его является кислотой
— кислотный, гидроксид его является кислотой  Водородное соединение отвечает формуле НС1. Исходя из электронно-графической формулы (наличия свободных d-орбиталей в третьем слое) может проявлять в возбужденном состоянии степень окисления 3, 5, 7.
Водородное соединение отвечает формуле НС1. Исходя из электронно-графической формулы (наличия свободных d-орбиталей в третьем слое) может проявлять в возбужденном состоянии степень окисления 3, 5, 7.


