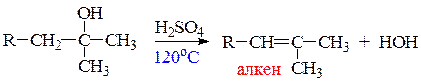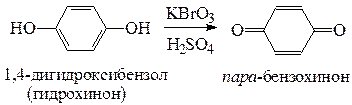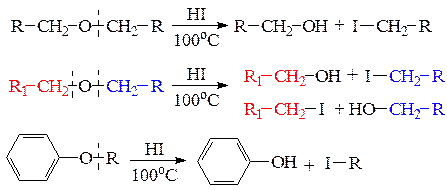И простых эфиров
1. Реакции замещения: а) реакции замещения ОН-группы спиртов на галоген. Гидроксильную группу в спиртах можно заместить на галоген действием концентрированных бромо- или иодоводородных кислот, реагента Лукаса (НCl + ZnCl2), галогенидов фосфора и тионилхлорида:
Фенолы (за исключением нитрофенолов) не вступают в реакции замещения ОН-группы. б) реакции с неорганическими кислородсодержащими кислотами являются общим способом получения сложных эфиров неорганических кислот. Многоосновные кислоты дают как кислые, так и средние эфиры:
Фенолы, в отличие от спиртов, не образуют сложные эфиры минеральных кислот. В этих условиях в фенолах протекают реакции замещения Н-атома в бензольном кольце (см. ниже реакции подпункта «е») в) реакции дегидратации спиртов протекают под действием сильных минеральных кислот (H2SO4; H3PO4) или Al2O3 при нагревании. В зависимости от температуры и строения спирта возможны два направления реакции: межмолекулярная дегидратация (с образованием простого эфира) и внутримолекулярная дегидратация (с образованием алкена). Чем выше температура реакции, тем больше вклад реакции элиминирования (отщепления). Третичные спирты отщепляют воду с образованием алкенов в присутствии менее концентрированных кислот при более низких температурах. Такие спирты практически не образуют простые эфиры.
Фенолы, в отличие от спиртов, не вступают в реакции дегидратации. г) реакции О-алкилирования - замещение подвижного Н-атома или металла на алкильный (или арильный) заместитель. Спирты и фенолы алкилируются в виде солей активных металлов (алкоголятов и фенолятов) с образованием простых эфиров - реакция Вильямсона.
д) реакции О-ацилирования - замещение подвижного Н-атома или металла на ацильный заместитель. В качестве ацилирующих средств используются карбоновые кислоты, их ангидриды и галогенангидриды. В результате реакций ацилирования образуются сложные эфиры. Спирты ацилируются всеми перечисленными ацилирующими средствами. Фенолы ацилируются только в виде фенолятов и только сильными ацилирующими средствами: ангидридами и галогенангидридами кислот.
е) реакции фенолов по бензольному кольцу протекают легко, чаще всего не требуют катализаторов. Реакция фенола с бромной водой является качественной - происходит обесцвечивание бромной воды и выпадает светлый осадок 2, 4, 6-трибромфенола.
2. Реакции окисления: а) жесткое окисление спиртов приводит к образованию альдегидов, кетонов и карбоновых кислот. Первичные спирты окисляются в соответствующие альдегиды, а затем в кислоты. Вторичные спирты при окислении образуют кетоны. Третичные спирты довольно устойчивы к действию окислителей, однако в кислотных растворах окислителей может происходить разрыв С-С связей возле гидроксильной группы с образованием смеси кислот и кетонов с меньшим числом С-атомов.
Под действием высоких температур в присутствии катализаторов - тонкодисперсной меди, серебра или оксида цинка - спирты дегидрируются до соответствующих альдегидов (первичные спирты) или кетонов (вторичные спирты).
б) окисление простых алифатических эфиров происходит на свету под действием кислорода воздуха. Окислению подвергается α -углеродный атом, образуются взрывоопасные неустойчивые гидропероксиды и пероксиды.
в) окисление фенолов жесткими окислителями сопровождается разрушением бензольного кольца с образованием трудноразделимой смеси индивидуальных соединений. При окислении броматами можно получить определенные продукты:
3. Реакции расщепления простой эфирной связи: а) расщепление простых эфиров концентрированной иодоводороной кислотой происходит при нагревании и приводит к образованию спирта и иодалкана. Если эфир несимметричный, то могут образовываться два различных спирта и два иодалкана. При расщеплении алкилариловых эфиров всегда образуется фенол и иодалкан:
б) расщепление простой эфирной связи металлическим натрием или литием происходит при нагревании с образованием алкоголятов или фенолятов и металлорганических соединений.
|