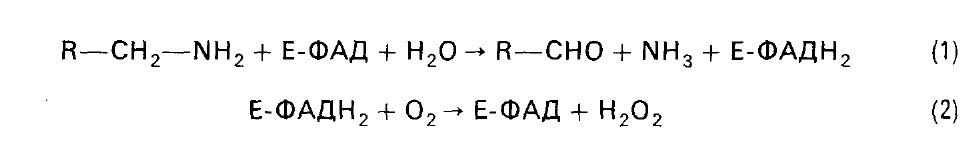Реакции по карбоксильной группе
1. Декарбоксилирование аминокислот. Простетической группой декарбоксилаз L-аминокислот служит пиридоксальфосфат (активная форма витамина В1). Продуктами декарбоксилирования аминокислот являются амины. Так как они образуются в качестве продуктов жизнедеятельности и обладают высокой физиологической активностью, их называют биогенными аминами. Открыты 4 типа декарбоксилирования аминокислот. Для тканей животных характерно α -декарбоксилирование.
При декарбоксилировании гистидина возникает гистамин. Он вызывает расширение сосудов в очаге воспаления, участвует в секреции соляной кислоты в желудке, что используется в клинике при изучении секреторной деятельности желудка (гистаминовая проба). При повышенной чувствительности к гистамину используют антигистаминные препараты.
При декарбоксилировании глутаминовой кислоты образуется у-аминомасляная кислота: НООСCH(NH2)CH2CH2COOH глутаминовая кислота g-аминомасляная кислота Она накапливается в мозговой ткани и представляет собой нейрогуморальный ингибитор. ГАМК используется в клинике как лекарственное средство при некоторых заболеваниях ЦНС. Декарбоксилаза ароматических аминокислот катализирует декарбоксилирование 3, 4-диоксифенилаланина (ДОФА), образуется дофамин. Он является предшественником норадреналина и адреналина. Накопление биогенных аминов может вызывать нарушения ряда функций в организме. Существуют специальные механизмы обезвреживания биогенных аминов. Происходит их окислительное дезаминирование с образованием альдегидов и освобождением аммиака. Ферменты - моноамино-и диаминоксидазы. Процесс является необратимым и протекает в две стадии:
Пероксид водорода далее распадается на воду и кислород. Моноаминоксидаза (МАО), ФАД-содержащий фермент, преимущественно локализуется в митохондриях.
|

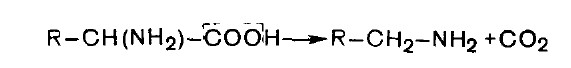

 NH2CH2CH2CH2COOH + СО2
NH2CH2CH2CH2COOH + СО2