Количественные характеристики вещества
Массы атомов химических элементов очень малы. Например, абсолютная масса атома кислорода составляет 2,667 · 10-26 кг. Пользоваться такими значениями в расчетах очень неудобно, поэтому на практике вместо абсолютных масс атомов используют относительные атомные массы. В 1961 г. была принята единая шкала относительных атомных масс, в основе которой лежит атомная единица массы (а.е.м.). А.е.м. – величина, равная 1/12 абсолютной массы атома углерода – 12С: 1 а.е.м. = Относительная атомная масса (Ar) – безразмерная величина, равная отношению средней массы атома элемента (естественного изотопа) к атомной единице массы. Относительная молекулярная масса (Мr) вещества – безразмерная величина, равная отношению массы его молекулы к атомной единице массы. Мr равна сумме относительных атомных масс всех элементов (Э) с учётом индексов:
Количество вещества (n) – величина, прямо пропорциональная числу структурных единиц (атомов, молекул, ионов и др.) в системе. Единицей измерения количества вещества является моль. Моль – количество вещества, содержащее столько молекул, атомов, ионов или других структурных единиц, сколько атомов содержится в 12 граммах изотопа углерода 12С. Количество частиц (атомов, ионов, молекул), содержащееся в 1 моле вещества равно 6,02∙1023 моль-1 и называется постоянной Авогадро (N a). Молярная масса (М) – это масса 1 моля вещества. Молярная масса вещества и количество вещества связаны соотношением:
Единицей измерения молярной массы является г/моль и кг/моль. Молярная масса любого вещества М численно равна его относительной молекулярной массе Мr, а для атома простого вещества – его относительной атомной массе Аr.
|

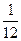 · mа (12С) =
· mа (12С) =  , откуда
, откуда 



