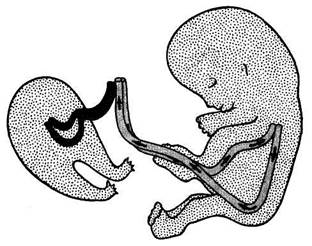
В — пигопаги; г — неполное расхождение близнецов.
Развитие близнецов, родившихся в срок, в большинстве случаев бывает нормальным. Однако масса их тела обычно меньше (на 10% и более), чем при одноплодной беременности. При двойнях масса детей при рождении менее 2500 г наблюдается в 40—60%. Низкая масса близнецов в этом случае чаще всего обусловлена недостаточностью маточно-плацентарного комплекса, который не способен в достаточной степени обеспечить адекватные условия для оптимального роста и развития близнецов. Следствием этого является ЗВУР плода, которая при многоплодной беременности распространена. Масса близнецов соответственно уменьшается пропорционально их количеству (тройня, четверня и т. д.). Разница в массе тела близнецов может достигать 200—300 г, а иногда и больше. Неравномерное (диссоциированное) развитие близнецов связано с неодинаковым поступлением питательных веществ из единого плацентарного круга кровообращения. При многоплодной беременности пороки развития плода в 2 раза (до 18,8%) превышают их частоту у женщин с одноплодной беременностью и наиболее характерны для монозиготных плодов. Сросшиеся близнецы являются наиболее типичным примером пороков, наблюдаемых только при моноамниотическом типе многоплодной беременности. В 75% сросшиеся близнецы — девочки. Среди различных типов срастания близнецов выделяют следующие (рис. 12.4): • торакопаги (сращение в области грудной клетки) - 18-74%; • омфалопаги и ксифопаги (сращение в области пупка и хрящом мечевидного отростка) — 0,5— 10%; • торакомфалопаги — 28%; • краниопаги (сращение гомологичными частями черепа) — 1—6%; • неполное расхождение: раздвоение только в одной части или области тела — 10%; • пигопаги и ишиопаги (соединение боковых и нижних отделов копчика и крестца) соответственно 18—20 и 5—6%. В 1/3 случаев сросшиеся близнецы рождаются мертвыми или умирают в 1-й день жизни. Выживание детей зависит от типа сращения и сочетанных аномалий. У сросшихся близнецов всегда выявляются анатомические аномалии развития, которые вероятнее всего обусловлены нарушением эмбрионального деления. У торакопагов в 100% имеется общая печень, в 50% общий желудочно-кишечный тракт, в 75% отмечаются врожденные пороки сердца, из которых в 90% — разной степени слияние перикарда. Нередко бывает слияние сердца с формированием двух желудочков и разного числа предсердий. Дефект межжелудочковой перегородки встречается практически у всех близнецов этой группы. Прогноз определяется степенью сращения. При общем сердце близнецы умирают в течение 3 мес. Омфалопаги и ксифопаги. При этом типе печень срастается в 80% случаев, грудинный хрящ—в 26%, диафрагма — в 17%, мочеполовые пути — в 3%. В 1/3 наблюдений встречаются омфалоцеле (эмбриональная грыжа) и общий дистальный отдел подвздошной кишки. Пороки сердца (дефект межжелудочковой перегородки и тетрада Фалло) наблюдаются с частотой до 25%. Краниопаги. При частичном типе краниопагов, когда головной мозг разделен костями черепа или твердой мозговой оболочкой, каждый плод имеет отдельную мягкую мозговую оболочку. При полном типе головной мозг соединен. Церебральная связь встречается в 43% случаев и чаще формируется при височно-теменном варианте сращения. Пигопаги, соединенные в области ягодиц и нижних отделов позвоночника, имеют общую часть канала крестцового отдела позвоночника, общие прямую кишку и задний проход, общий мочевой пузырь и мочеиспускательный канал, слитные наружные половые органы. Прогноз довольно благоприятный, так как в патологический процесс не вовлечены жизненно важные органы. Ишиопаги, соединенные в области нижней части крестца и копчика, имеют общий тазовый пояс. Ишиопаги имеют 3 или 4 ноги. У них общая нижняя часть желудочно-кишечного тракта. Может быть общий мочевой пузырь и мочеиспускательный канал. Синдром фето-фетальной гемотрансфузии (СФФГ) возникает в 5—25% наблюдений при монозиготной двойне с монохориальным биамниотическим типом плацентации. Перинатальная смертность при данной патологии составляет от 60 до 100%. При монохориальной двойне в плаценте нередко образуются анастомозы между сосудистыми системами обоих плодов (артерио-артериальные, артериовенозные или вено-венозные). Если в сосудистой системе плаценты кровяное давление симметрично, оба близнеца развиваются в одинаковых условиях. Имеющиеся при монохориальном типе артерио-артериальные анастомозы компенсируют гемодинамический дисбаланс, который может быть вызван артериовенозными шунтами. Однако это равновесие может быть нарушено вследствие асимметричного плацентарного кровообращения. Предпосылки для развития СФФГ закладываются при монохориальной двойне уже в процессе развития сосудистой сети плаценты, когда формируются условия для совместного использования близнецами определенных сосудистых зон (котиледонов). При этом с одной и той же группой котиледонов связаны оба близнеца одновременно. Образующиеся артериовенозные анастомозы, которые проходят через капиллярное ложе котиледона, способствует оттоку крови от одного близнеца (донора) к другому (реципиенту). Выраженность СФФГ (легкая, средняя, тяжелая) зависит от степени перераспределения крови через эти анастомозы, которые варьируют в размерах, числе и направлении. Нарушение состояния плода-донора обусловлено гиповолемией из-за недостаточного поступления крови и гипоксии вследствие плацентарной недостаточности. У него формируются задержка развития, маловодие, артериальная гипотония и часто анемия (концентрация гемоглобина может быть 80 г/л и меньше). У плода-реципиента имеют место гиперволемия и гиперосмолярность, приводящие к сердечной недостаточности, полиурии, многоводию и водянке (общий отек, асцит, перикардиальный или плевральный выпот). Кроме того, имеют место артериальная гипертония, гипертрофия сердца, гиперволемия, отмечается высокое гематокритное число и склонность к тромбозам. Различия в размерах и массе между обоими плодами (диссоциация развития) могут появиться в различные сроки беременности. Степень диссоциации их может варьировать. Нередко ситуация приобретает угрожающий характер между 20-й и 30-й неделями беременности, когда наиболее вероятно преждевременное ее прерывание. В связи с возникающими нарушениями может наступить смерть одного из плодов. Если плод умирает в первые 2 нед беременности (до начала оссификации), то возможна его полная резорбция. Если плод умирает позже и не подвергся резорбции, то он сначала мацерируется, затем дегидратируется, уменьшается в размерах, уплощается и вдавливается в хориальную пластинку своей плаценты либо в амнион вне плаценты. Такой мумифицированный плод носит название «бумажный плод». Обнаруживается он, как правило, после рождения оставшегося в живых близнеца при осмотре последа. После смерти одного из близнецов из монохриальной двойни оставшийся в живых может быть быстро обескровлен путем массивного сброса крови в сосудистое русло мертвого близнеца, что вызывает острую гипотонию и ишемические повреждения мозга. Происходящие гемодинамические нарушения могут привести к смерти и второго близнеца. Одним из признаков СФФГявляется увеличение воротникового пространства у одного или обоих плодов в сроки беременности 10—44 нед, что может быть обусловлено сердечной недостаточностью в связи с гиперволемией. В ряде случаев можно обнаружить артериовенозные анастомозы с помощью цветного допплеровского картирования. К признакам, которые могут указывать на наличие СФФГ, относят различия в массе новорожденных на 20% и более, формирование многоводия с 16—24-й неделе беременности. Патогномоничными эхографическими признаками тяжелого СФФГявляются наличие большого мочевого пузыря у плода-реципиента на фоне выраженного многоводия и отсутствие наполнения мочевого пузыря у плода-донора в связи с анурией. Для последнего характерно также снижение двигательной активности на фоне выраженного маловодия. Дополнительным эхографическим критерием является наличие гипертрофичного, расширенного сердца у плода-реципиента. У плода-донора сердце может быть также расширено, что наряду с гиперэхогенным кишечником служит проявлением гипоксии. При исследовании кровотока в артериях пуповины у пациенток с СФФГ отмечаются изменения допплерометрических показателей у обоих плодов. У плода-донора это обусловлено указанной патологией развития плаценты, у плода-реципиента нарушение кровотока связывают с компрессией пуповины в результате многоводия. При выявлении выраженного маловодия у одного плода и многоводия у другого при монохориальной двойне частота внутриутробной смерти обоих плодов составляет 90%, что диктует необходимость более ранней диагностики этой патологии. Для лечения СФФГ удаляют лишнее количество амниотической жидкости путем амниоцентеза под контролем ультразвукового сканирования. Этот метод лечения в первую очередь предотвращает риск самопроизвольного аборта или преждевременных родов. Эффективность этого метода лечения составляет 30—83%, что зависит от степени тяжести СФФГ. В качестве альтернативного метода лечения при тяжелой степени СФФГ может быть использована эндоскопическая лазерная коагуляция анастомозирующих сосудов плаценты под постоянным эхографическим контролем. Эффективность данного метода составляет 70%. В процессе выполнения данной лечебной процедуры трансабдоминально вводят фетоскоп в амниотическую полость плода-реципиента. Визуально и с помощью эхографии изучают состояние хорионической пластинки вдоль всей межплодовой перегородки, выявляют и производят коагуляцию пересекающих ее сосудов. На завершающем этапе проводят дренирование околоплодных вод для нормализации их количества. С помощью эндоскопической лазерной коагуляции возможно пролонгирование беременности в среднем на 14 нед, что способствует значительному снижению перинатальной смертности Одним из проявлений трансфузионного синдрома является обратная артериальная перфузия у близнецов (синдром акардии, акардиальный монстр, ацефальная акардия, голокардия, псевдокардиальная аномалия). Частота этой аномалии составляет 1:35 000 новорожденных. Обратная артериальная перфузия возникает только у монозиготных близнецов со сросшимся плацентами.
Во всех случаях при ОАП обнаруживают пуповинные анастомозы, которые на ранних этапах эмбриогенеза могут приводить к обратной циркуляции крови в пуповине. Это в свою очередь обусловливает нарушение развития органов и систем у одного из плодов вследствие недостатка кислорода и питательных веществ. Таким образом, при ОАП формируется близнец-реципиент и близнец-донор (рис. 12.5). Такое нарушение гемодинамики обусловлено тем, что у одного из близнецов сосуды пуповины формируются раньше и охватывают большую часть хориона. У второго плода этот процесс запаздывает, и ему достается меньшая часть хориона, не соответствующая его потребностям. Сосуды пуповины второго плода при этом в большей степени тяготеют к сосудам первого плода, а не к плаценте. Близнец-донор, как правило, морфологически здоров, хромосомный набор у него в пределах нормы. Однако у этого плода имеются признаки перегрузки сердца, характеризующиеся водянкой, ЗВУР, гипертрофией правого желудочка и гепатоспленомегалией.
Рис. 12.5. Характер фетоплацентарного кровотока при синдроме обратной артериальной перфузии.
У близнеца-реципиента, кроме сердца, может отсутствовать любой другой орган, а внешний вид плода принимает различные формы. Наиболее распространенными являются следующие формы поражений (рис. 12.6): • acardia anceps: пораженный плод имеет наиболее сохранный вид, голова сформирована полностью или частично с остатками костей свода черепа и мозговой ткани, лицевой череп с расщелинами, различаются конечности и отдельные части туловища; • acardia acephalus: отсутствует голова, верхняя часть туловища с органами грудной клетки, верхние конечности; определяются рудиментарная диафрагма, зачатки органов брюшной полости, тазовые кости и нижние конечности; • acardia acormus: отсутствует туловище, голова или структура, подобная голове, прикрепляется к плаценте напрямую или через короткую пуповину; • acardia amorphus: наиболее выраженное поражение плода, который представляет собой аморфную массу. Смертность близнецов-реципиентов составляет практически 100%. Смертность плодов-доноров - 50%. Выявить перечисленные нарушения состояния плодов при многоплодной беременности с наибольшей достоверностью позволяет УЗИ. Заболеваемость и смертность при многоводной беременности. В сравнении с одноплодной беременностью заболеваемость близнецов в 5 раз выше. Даже у доношенных близнецов, особенно тройней, нередко наблюдаются признаки морфо-функциональной незрелости. Эти дети требуют в дальнейшем специального ухода и вскармливания. Признаки морфофункциональной незрелости особенно резко выражены у недоношенных близнецов. По имеющимся данным, 16% от всех детей, родившихся незрелыми, приходится на близнецов.
Рис. 12.6. Формы поражений у плода-реципиента при синдроме обратной артериальной перфузии.
При многоплодии обычно прослеживается прямая зависимость между массой плаценты и массой плодов. Масса каждой отдельной плаценты или суммарная масса плацент, разделенная на количество плодов (при монохориальном типе плацентации или слившихся плацентах), как правило, ниже массы плацент при одноплодной беременности того же срока. Закономерно, что и оценка по шкале Апгар при многоплодной беременности также чаще бывает ниже, чем при одноплодной. У монозиготных близнецов чаще отмечаются тенденция к отставанию в физическом и нервно-психическом развитии новорожденных, повышение числа случаев родовых травм. Неонатальный период у плода-реципиента в результате трансфузионного синдрома может быть осложнен опасной перегрузкой сердца и сердечной недостаточностью. Повышенная частота осложнений при многоплодной беременности как со стороны матери, так и плода, ведет к значительному увеличению перинатальной смертности.
Перинатальная смертность при многоплодной беременности в 6—10 раз выше, чем при одноплодной, и находится в прямой зависимости от массы тела детей. В развитых странах перинатальная смертность двойни составляет 47—120%о, а для тройни — между 93 и 203%о. Такая высокая смертность близнецов сохраняется в течение 1-го года жизни, и только ко 2-му году частота смертности среди дизиготных близнецов равняется таковой после одноплодной беременности. Заболеваемость и смертность монозиготных близнецов в 2—3 раза выше, чем у дизиготных. Принимая во внимание, что среди монозиготных близнецов приблизительно в 1% встречается монохориальный и моноамниотический тип, смертность этих близнецов может достигать 50%. Высокая заболеваемость среди монозиготных близнецов чаще всего обусловлена трансфузионным синдромом, сращением близнецов и патологией пуповины. При этом перинатальная смертность вторых плодов при двойнях является более высокой, чем первых. Основные причины заболеваемости и смертности близнецов сопряжены с преждевременными родами. При этом в структуре осложнений преждевременных родов ведущее место занимают: • респираторный дистресс-синдром; • асфиксия; • внутрижелудочковые кровоизлияния; • некротический энтероколит. Другую группу причин заболеваемости близнецов составляют: • задержка развития плода (ЗВУР); • интранатальные осложнения; • трансфузионный синдром; • патология пуповины; • аномалии развития.
|