Метиландростендиол
Methylandrostendiolum. Methandriolum. Метиландростендиол. 17-α-метил-Δ5-андростен-3β-17β-диол. С20Н32О2. М = 304,48.
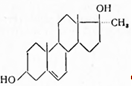
Синонимы: Androdiol, Metandiol, Notandron, Testodiol и др. Является промежуточным продуктом при синтезе 17-метилтестостерона. 17-Метиландростендиол — белый кристаллический порошок. Не растворим в воде и мало в спирте, растворяется в хлороформе, пиридине и кипящем метиловом спирте, т. пл. 202—206°. Раствор препарата в 80%-ной уксусной кислоте в присутствии концентрированной серной кислоты дает на границе слоев оранжевую полосу и затем зеленовато-желтую флуоресценцию. При ацетилировании уксусным ангидридом, в присутствии пиридина, образуется ацетильное производное, т. пл. 133—136°. Чистоту препарата определяют по отсутствию кетостероидов (0,002 г препарата растворяют в 1 мл 95%-ногоспирта и прибавляют 1 мл 95%-ного раствора м-динитробензола и 1 мл 15%-ного раствора едкого натра — спустя 1 ч раствор не должен быть темнее смеси 1 мл 95%-ного спирта с теми же реактивами). Хранят с предосторожностью (список Б), в сухом месте, защищенном от действия света. Применяют сублингвально для усиления белкового анаболизма у реконвалесцентов после тяжелых травм, операций, инфекционных и других заболеваний по 0,025—0,05 г на прием в виде таблеток. Обладая значительно меньшей андрогенной активностью, нежели метилтестостерон, препарат может применяться и в женской практике с целью повышения анаболизма, а также для уменьшения активности фолликулярного гормона в климактерическом периоде (и при раке молочной железы). При длительном применении иногда наблюдается усиленный рост волос на лице и туловище и увеличение сальности кожи. Кувада и Мнгасака (1938) синтезировали различные эфиры 17-метилтестостерона, но не получили интересных для медицины препаратов. Недеятельным оказался 17-аллилтестостерон, синтезированный Бутенандтом и Петерсом (1938 г.). При окислении Δ4-двойной связи тестостерона перекисью водорода получено соединение строения:
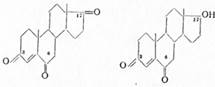
не обладающее андрогенной активностью. Аналогичны и другие полиоксисоединения, как андростантриол-3,5,6-он-17, андростантрион-3,16,17-ол-5, Δ5-андростентрион-3,4,17 и андростантриол-3,14,17 — оказались неактивными. Напротив, андростентрион-3,6,17 и 6-оксотестостерон в опытах на кастрированных крысах (самках) вызывали течку, т. е. проявляли активность женского гормона. 3-Галогенопроизводные дегидроэпиандростерона неактивны, но 17-хлор-Δ5-андростенол-3-ацетат достаточно активен (Вестфаль); слабой биологической активностью обладают 17-аминопроизводные андростана.
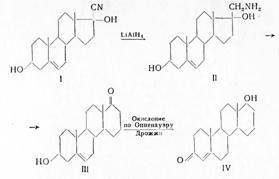
Замена пятичленного кольца D на шестичленное приводит к незначительному уменьшению активнрсти D-гомотестостерона (20—30γ). Он получен из циангидрина дегидроэпиандростерона (I), который при восстановлении дает оксиамин (II), а при действии на него азотистой кислоты перегруппировывается по Демьянову с расширением кольца вD -гомоаналог дегИдроэпиандростерона (III) и по методу Мамоли переводится в D-гомо- тестостерон (IV):
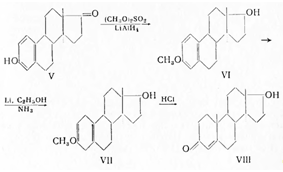
Полученный из Зα-окси-D-гомоандростерона 4,5-гомодигидротестостерон действует в опытах на крысах аналогично дигидротестостерону. Для проявления андрогенной активности необязательно присутствие С19-метильной группы; 19-нортестостерон также обладает андрогенной активностью. Он получается из эстрона (V) через метиловый эфир эстрадиола, с последующим восстановлением ароматического кольца литием и спиртом в жидком аммиаке в метоксикарбинол (VI); последний при кислотном гидролизе переходит в 19-нортестостерон (VII):
|