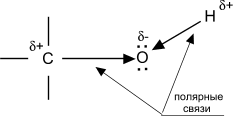
Химические свойства. Свойства спиртов ROH определяются наличием полярных связей Od-–Hd+ и Cd+–Od-, и неподеленных электронных пар на атоме кислорода.
Свойства спиртов ROH определяются наличием полярных связей Od-–Hd+ и Cd+–Od-, и неподеленных электронных пар на атоме кислорода.
При реакции спиртов возможно разрушение одной из двух связей: C–OH (с отщеплением гидроксильной группы) или O–H (с отщеплением водорода). Это могут быть реакции замещения, в которых происходит замена OH или H, или элиминирование (отщепление), когда образуется двойная связь. На реакционную способность спиртов большое влияние оказывает строение радикалов, связанных с гидроксильной группой.
I. Реакции с разрывом связи RO–H
1. Спирты реагируют с щелочными и щелочноземельными металлами, образуя солеобразные соединения – алкоголяты. Со щелочами спирты не взаимодействуют.
2СH3CH2CH2OH + 2Na ® 2СH3CH2CH2ONa + H2 2СH3CH2OH + Сa ® (СH3CH2O)2Ca + H2
В присутствии воды алкоголяты гидролизуются:
(СH3)3С–OK + H2O ® (СH3)3C–OH + KOH
Это означает, что спирты – более слабые кислоты, чем вода. 2. Взаимодействие с органическими кислотами (реакция этерификации) приводит к образованию сложных эфиров.
В общем виде:
II. Реакции с разрывом связи R–OH.
1. С галогеноводородами:
R–OH + HBr «R–Br + H2O
2. С концентрированной серной кислотой:
III. Реакции окисления
1. Спирты горят: 2С3H7ОH + 9O2 ® 6СO2 + 8H2O
2. При действии окислителей: a) первичные спирты превращаются в альдегиды (или в карбоновые кислоты)
b) вторичные спирты окисляются до кетонов
c) третичные спирты устойчивы к действию окислителей.
IV. Дегидратация
Протекает при нагревании с водоотнимающими реагентами. 1. Внутримолекулярная дегидратация приводит к образованию алкенов
CH3–CH2–OH ––t°>140°C,H2SO4® CH2=CH2 + H2O
При отщеплении воды от молекул вторичных и третичных спиртов атом водорода отрывается от соседнего наименее гидрогенизированного атома углерода; образующийся алкен содержит наибольшее число заместителей при двойной связи (правило Зайцева).
2. Межмолекулярная дегидратация даёт простые эфиры
Обе реакции конкурируют между собой. Увеличение температуры и разбавление инертным растворителем благоприятствуют внутримолекулярному процессу.
Многоатомные спирты
Получение
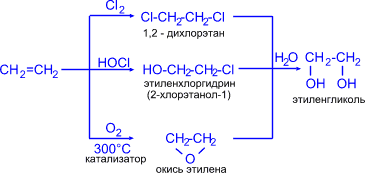
1. Этиленгликоль (этандиол-1,2) синтезируют из этилена различными способами:
3CH2=CH2 + 2KMnO4 + 4H2O ® 3HO–CH2–CH2–OH + 2MnO2 + 2KOH
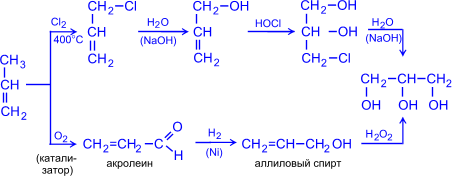
2. Глицерин (пропантриол -1,2,3) получают гидролизом жиров (см. "Жиры") или из пропилена по схемам:
|