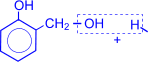Химические свойства. Альдегиды характеризуются высокой реакционной способностью
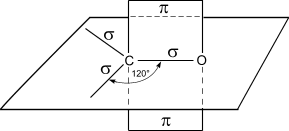
Альдегиды характеризуются высокой реакционной способностью. Большая часть их реакций обусловлена наличием карбонильной группы. Атом углерода в карбонильной группе находится в состоянии sp2 -гибридизации и образует три s- связи (одна из них – связь С–О), которые расположены в одной плоскости под углом 120° друг к другу.
Схема строения карбонильной группы
Двойная связь карбонильной группы по физической природе сходна с двойной связью между углеродными атомами, т. е. это сочетание s- и p- связей, последняя из которых образована р- электронами атомов углерода и кислорода. Ввиду большей электроотрицательности атома кислорода по сравнению с атомом углерода, связьС=О сильно поляризована за счет смещения электронной плотности p- связи к атому кислорода, в результате чего на атоме кислорода возникает частичный отрицательный (d-), а на атоме углерода – частичный положительный (d+) заряды: Благодаря поляризации атом углерода карбонильной группы обладает электрофильными свойствами и способен реагировать с нуклеофильными реагентами. Важнейшими реакциями альдегидов являются реакции нуклеофильного присоединения по двойной связи карбонильной группы.
1. Одной из типичных реакций нуклеофильного присоединения альдегидов является присоединение синильной (циановодородной) кислоты, приводящее к образованиюa- оксинитрилов.
Эта реакция используется для удлинения углеродной цепи и получения a- оксикислот.
2. Присоединение гидросульфита натрия дает кристаллические вещества, обычно называемые гидросульфитными производными альдегидов.
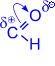
3. Присоединение спиртов к альдегидам приводит к образованию полуацеталей – соединений, в которых атом углерода связан и с гидроксильной (–ОН), и с алкоксильной (–ОR) группами.
4. Присоединение водорода к альдегидам осуществляется в присутствии катализаторов (Ni, Co, Pd и др.) и приводит к образованию первичных спиртов.
5. Окисление. Альдегиды легко окисляются, образуя соответствующие карбоновые кислоты.
a) аммиачный раствор оксида серебра [Ag(NH3)2]OH при нагревании с альдегидами окисляет альдегид до кислоты (в виде ее аммониевой соли) с образованием свободного металлического серебра. Восстановленное серебро ложится тонким слоем на стенки химического сосуда, в котором осуществляется реакция, и получается серебряное зеркало. Эта реакция, получившая поэтому название "серебряного зеркала", служит качественной реакцией на альдегиды.
b) еще одной характерной реакцией является окисление альдегидов гидроксидом меди (II).
Сухой газообразный формальдегид в присутствии катализаторов образует высокомолекулярный полиформальдегид. Полимеризация формальдегида напоминает полимеризацию алкенов.
В водных растворах формальдегид образует полимер, называемый параформом.
n CH2 = O + H2O ® HOCH2
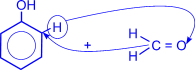
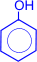
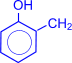
Особое практическое значение имеет реакция поликонденсации формальдегида с фенолом с образованием фенолформальдегидных смол. При действии щелочных или кислых катализаторов на смесь фенола и формальдегида конденсация идет в орто- и пара- положениях.
Рост молекулы за счет конденсации фенола с формальдегидом осуществляется при нормальной температуре в линейном направлении.
и т. д.
Фенолформальдегидные смолы – первенцы промышленных синтетических смол, их производство под названием "бакелит" впервые начато в 1909 году. Фенолформальдегидные смолы используются в производстве различных пластмасс. В сочетании с различными наполнителями такие пластмассы называются фенопластами. Кроме того, фенолформальдегидные смолы применяются при изготовлении различных клеев и лаков, термоизоляционных материалов, древесных пластиков, литейных форм и др.
|

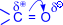 .
.

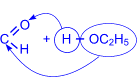
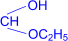 полуацеталь
полуацеталь
 ацеталь
ацеталь

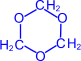 (триоксиметилен)
(триоксиметилен)
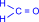 –––––®
–––––®