Процесс без теплообмена с внешней средой
(адиабатный процесс) При адиабатном процессе энергообмен рабочего тела с окружающей средой происходит только в форме работы. Рабочее тело предполагается теплоизолированным от окружающей среды, т.е. передача тепла между ним и окружающей средой отсутствует, т.е. q=0, а следовательно dq=0 Тогда, уравнение первого закона термодинамики примет вид
Таким образом изменение внутренней энергии и работа в адиабатном процессе эквивалентны по величине и противоположны по знаку. Следовательно, работа адиабатного процесса расширения совершается вследствие уменьшения внутренней энергии газа и, следовательно, температура газа уменьшатся. Работа адиабатного сжатия полностью идет на увеличение внутренней энергии, т.е. на повышение его температуры. Получим уравнение адиабаты для идеального газа. Из первого закона термодинамики
при dq=0 получим (du=CVdT)
Теплоемкость
Дифференцируя уравнение состояния pV=RT получим
Подставляя RdT из (**) в (*)
или
или, разделив на pV,
Интегрируя при k=const, получим
откуда
Последнее уравнение называется уравнением Пуассона и является уравнением адиабаты при Из уравнения Пуассона следует, что
то есть при адиабатном расширении давление падает, а при сжатии возрастает. Изобразим изохорный процесс в pV, pT и VT – диаграммах
Площадь V1 12 V2 под адиабатой 1-2 на pV– диаграмме дает работу l равную изменению внутренней энергии газа
Сравнивая уравнение адиабаты с законом Бойля-Мариотта Получим уравнение адиабаты в pT и VT−;диаграммах. В адиабатном процессе изменяются все три параметра (p,V,T). Получим зависимость между T и V. Уравнения состояния для точек 1 и 2
откуда, разделив второе уравнение на первое
Подставляя отношение давление из уравнения адиабаты Пуассона
или TVk-1=const – уравнение адиабаты в VT- диаграмме. Подставляя в (*) (3) отношение объемов из уравнения адиабаты (Пуассона)
или Работа в адиабатном процессе при CV=const
Учитывая соотношение между температурой T и V
Учитывая соотношение между T и p
Изменение внутренней энергии Располагаемая работа, с учетом того, что
Т.е. располагаемая работа в k раз больше работы адиабатного процесса l. φ и ψ не находим.
|

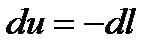
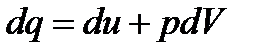
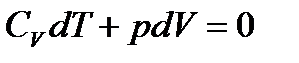
 , откуда
, откуда (*) (1)
(*) (1)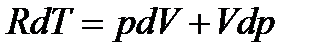 (**) (2)
(**) (2)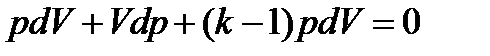
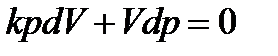 (3)
(3)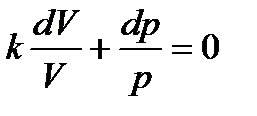
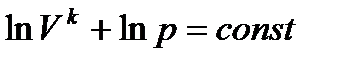
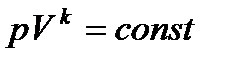
 .
.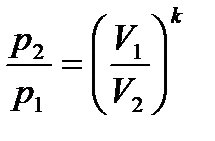 ,
,

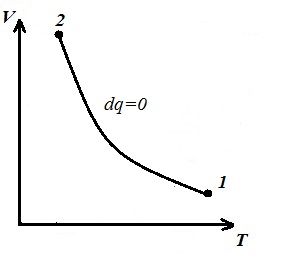
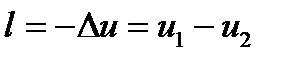
 (T=const) можем сделать вывод, что, поскольку k>1, то при расширении по адиабате давление падает сильнее, чем по изотерме, т.е. в pV– диаграмме адиабата больше изотермы, т.е. адиабата – неравносторонняя гипербола, не пересекающее координатных осей.
(T=const) можем сделать вывод, что, поскольку k>1, то при расширении по адиабате давление падает сильнее, чем по изотерме, т.е. в pV– диаграмме адиабата больше изотермы, т.е. адиабата – неравносторонняя гипербола, не пересекающее координатных осей.
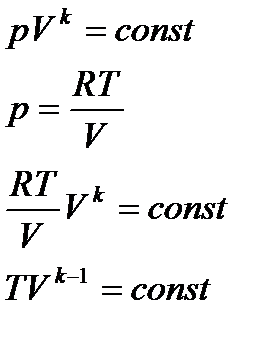
 (*) (3)
(*) (3)
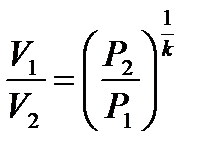

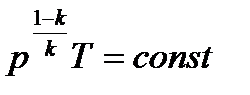
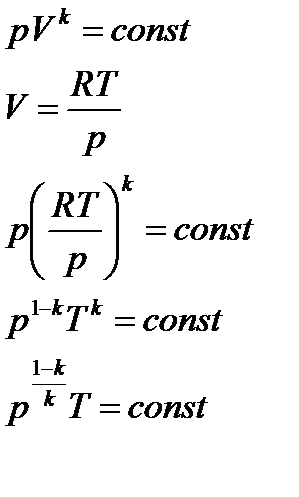
 − уравнение адиабаты в pT- диаграмме. Эти уравнения получены в предположении, что k=const.
− уравнение адиабаты в pT- диаграмме. Эти уравнения получены в предположении, что k=const.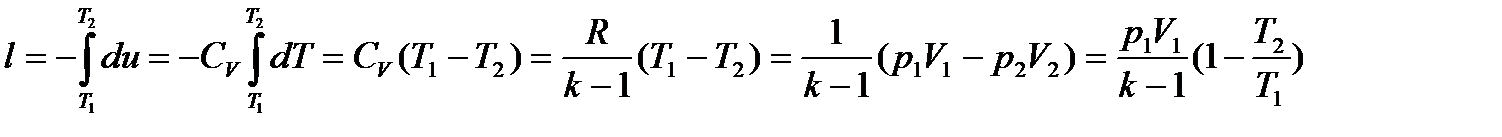
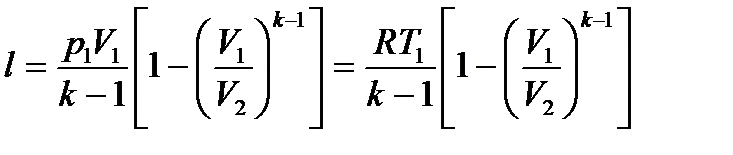

 u=-l.
u=-l.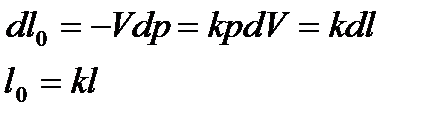 ,
,


