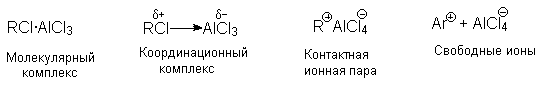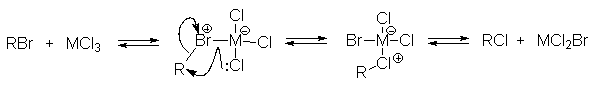Кинетика и механизм
Кинетическое изучение реакции Фриделя-Крафтса провести нелегко, поскольку скорость реакции очень чувствительна к следам влаги, реакционная смесь расслаивается в негомогенные слои, первоначальные продукты реакции легко изомеризуются и, кроме того, кинетика сильно зависит от растворителя. Несмотря на эти трудности, основные закономерности этой реакции в настоящее время достаточно хорошо выяснены. Например, бензилирование хлористым бензилом в нитробензоле в присутствии безводного AlCl3 в качестве катализатора описывается кинетическим уравнением третьего порядка v=k[RHal][ArH][AlCl3]. Поэтому механизм реакции можно представить следующей схемой:
где В: =AlCl4- ; H2O или другое основание. Скорость реакции лимитируется второй стадией Точное строение интермедиата (RCl .AlCl3) неизвестно. В принципе, можно представить целый ряд структур от молекулярного комплекса до диссоциированных карбокатионов.
Участие свободных карбокатионов как алкилирующих агентов маловероятно. Если бы алкилирующими агентами были свободные карбокатионы, то медленной стадией была бы стадия их образования (k1), а реакция с аренами была бы быстрой и третьего порядка не должно было наблюдаться. Крайне маловероятно, что алкилирующим агентом является молекулярный комплекс. При низких температурах иногда удается выделить комплексы алкилгалогенидов с кислотами Льюиса. Для них характерен медленный обмен галогенов по схеме:
Скорость обмена возрастает в ряду перв.R< втор.R<трет.R, что можно объяснить и ион-парным строением, и структурой координационного аддукта. Многие исследователи, работающие в данной области, полагают, что строение комплексов RX. MXn постепенно изменяется от структуры координационного аддукта в случае R=СН3 до структуры ионной пары в случае R=t-Bu, однако экспериментально это пока не подтвердено. Способность атома галогена в RX к комплексообразованию с AlCl3 или другой жесткой кислотой Льюиса резко уменьшается от фтора к иоду, вследствие этого активность алкилгалогенидов в качестве алкилирующих агентов в реакции Фриделя-Крафтса также уменьшается в ряду RF> RCl> RBr> RI. По этой причине алкилиодиды не применяют в качестве алкилирующего агента. Различие в активности алкилфторидов и алкилбромидов настолько велико, что позволяет селективно замещать фтор в присутствии брома в одной и той же молекуле.
|