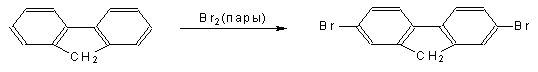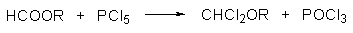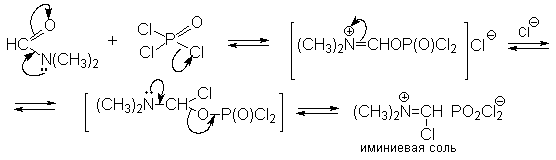Формилирование ароматических соединений
Прямое введение формильной группы в бензольное кольцо впервые удалось осуществить Л.Гаттерману и Г.Коху в 1897 году. Формилирование по Гаттерману-Коху осуществляется под действием оксида углерода (II) и хлористого водорода в присутствии типичного катализатора Фриделя-Крафтса - хлорида алюминия, промотированного хлоридом меди (I).
Роль однохлористой меди в этой реакции неясна: возможно она связывает СО в комплекс, что способствует образованию крайне нестабильного хлористого формила HCOCl из CO и HCl, однако предположение об участии хлористого формила в реакции Гаттерман-Коха никогда не было строго доказано экспериментально. Таким путем удается ввести альдегидную группу в различные алкилбензолы, арилгалогениды, полициклические углеводороды и т.д., причем формильная группа вводится селективно в пара-положение. Высокие выходы альдегидов наблюдаются при использовании высоких давлений порядка 50-200 атм в отсутствии Cu2Cl2 или при обычном давлении в присутствии Cu2Cl2.
В лабораторных условиях необходимую для формилирования аренов смесь CO и HCl удобно получать при действии хлорсульфоновой кислоты на муравьиную кислоту.
В качестве формилирующего агента можно применять относительно стабильный газообразный фтористый формил при катализе трехфтрористым бором. Фтористый формил получается при взаимодействии смешанного ангидрида муравьиной и уксусной кислот с безводным фтористым водородом.
По существу реакцию Гаттермана-Коха можно рассматривать как частный случай ацилирования по Фриделю-Крафтсу, однако с гораздо более ограниченной областью применения. В ароматическое кольцо фенолов, нафтолов, их простых эфиров, аминов и N,N-диалкиланилинов с помощью CO и HCl ввести формильную группу не удается. Поэтому сам Гаттерман предложил другой метод введения альдегидной группы, в котором в качестве формилирующего агента использовалась смесь безводного HCN и газообразного хлористого водорода в присутствии кислоты Льюиса (реакция Гаттермана). Для того, чтобы избежать применения ядовитой синильной кислоты, Р.Адамс модифицировал условия реакции, заменив ее цианидом цинка. Это позволило из цианида цинка и HCl получать непосредственно в реакционной смеси HCN и безводный хлористый цинк, играющий роль слабой кислоты Льюиса. Этот метод дает хорошие результаты при формилировании фенолов и простых эфиров фенолов.
Истинная природа электрофильной частицы, принимающей участие при введении формильной группы с помощью HCN,HCl и кислоты Льюиса, точно не установлена, полагают, что ею может быть интермедиат типа HN=CHN=CHCl, однако каких-либо строгих доказательств этого не имеется. В настоящее время обе реакции Гаттермана в своем классическом варианте введения альдегидной группы в ароматическое кольцо редко применяются и представляют скорее чисто познавательный интерес. Реакция Гаттермана стала очень популярной после того, как было установлено, что вместо цианидов для введения формильной группы можно использовать нетоксичный и легко доступный симметричный 1,3,5-триазин. Этот реагент обеспечивает высокие выходы альдегидов при формилировании алкилбензолов, фенолов, эфиров фенолов, конденсированных углеводородов и гетероциклических соединений.
В синтетической практике для введения формильной группы очень удобно использовать легко доступные
Это очень удобный лабораторный метод формилирования конденсированных углеводородов, бифенилов, фенолов и их простых эфиров. Главный его недостаток состоит в низкой селективности формилирования алкилбензолов для которых, как правило, образуется смесь орто- и пара-изомерных альдегидов примерно в равных количествах. Необходимые
Для введения альдегидной группы в ароматическое кольцо, активированное диалкиламино-, гидрокси- или алкоксигруппой, эффективна реакция, описанная в 1927 г А.Вильсмейером и А.Хааком. Диметилформамид (берется как реагент и растворитель) в присутствии хлорокиси фосфора является превосходным региоселективным формилирующим агентом. С помощью этого реагента альдегидная группа вводится в пара-положение по отношению к имеющимся NR2-; или OR-группам. Эту реакцию можно также рассматривать как ацилирование, где роль катализатора - кислоты Льюиса выполняет хлорокись фосфора (POCl3). Электрофильным агентом в реакции Вильсмейера-Хаака является иминиевая соль, которая образуется при взаимодействии ДМФА и хлорокиси фосфора (в чистом виде ее, как правило, не выделяют).
Иминиевая соль такого типа при необходимости может быть выделена в индивидуальном виде, например, при взаимодействии ДМФА с фосгеном, где после отщепления СО2 образуется соль (CH3N+ =CHCl) Cl-. Реакция Вильсмейера-Хаака чрезвычайно проста в экспериментальном отношении и обеспечивает очень высокие выходы ароматических альдегидов, содержащих NR2-,OR- или OH-группы. Она оказывается практически ценной при формилировании конденсированных ароматических углеводородов - антрацена, азулена, пирена и др., а также разнообразных гетероциклических соединений ряда фурана, тиофена, пиррола, индола. В табл.4 приведены сводные данные по формилированию ароматических соединений с помощью различных реагентов, наглядно отражающие их достоинства и недостатки. В качестве субстратов выбраны алкилбензолы, фенолы, нафтолы, а также конденсированные углеводороды и бифенил. Таблица 4 Формилирование ароматических соединений с помощью
|

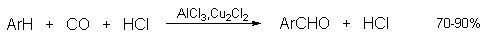
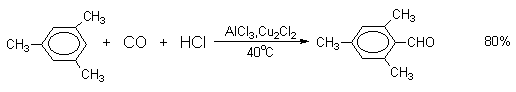
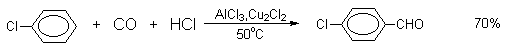
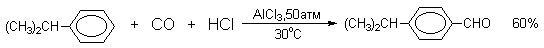
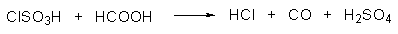
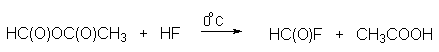
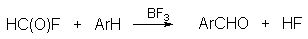
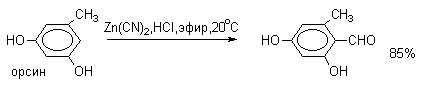
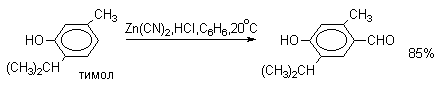
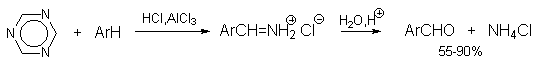
 ,
,