Acidum ascorbinicum
у-Лактон-2,3-дегидро-L-гулоновой кислоты
Получение. В 1933 г. был осуществлен синтез аскорбиновой кислоты, который подтвердил ее строение. В промышленности синтез аскорбиновой кислоты осуществляется из D-глюкозы, которая в больших количествах получается при расщеплении крахмала серной кислотой. Аскорбиновая кислота представляет собой белый кристаллический порошок кислого вкуса. Она легко растворима в воде, растворима в этиловом спирте, нерастворима в эфире, бензоле и хлороформе. Температура плавления 190—193 °С (с разложением). Аскорбиновая кислота ведет себя как одноосновная кислота. Кислотный характер ее обусловлен атомом водорода гидроксильной группы в положении 3, за счет которого она образует соли.
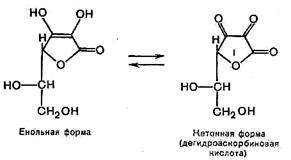
Характерной частью молекулы аскорбиновой кислоты, обусловливающей ее химические свойства и физиологическую активность, является ендиольная группировка.
Благодаря подвижности водородных атомов енольных гидроксильных групп аскорбиновая кислота легко окисляется, причем окисление может идти в 2 стадии. 1-я стадия. Характеризует обратимый процесс окисления, при котором аскорбиновая кислота окисляется до дегидроаскорбиновой кислоты (кетонная форма), способной снова восстанавливаться до аскорбиновой кислоты.
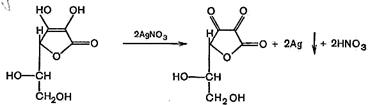
2-я стадия. В водной среде процесс окисления может идти дальше — до разложения дегидроаскорбиновой кислоты. В этом случае продукты разложения не могут снова превратиться в аскорбиновую кислоту, что характеризует необратимый процесс окисления с потерей физиологической активности. Определение подлинности кислоты аскорбиновой проводится за счет ее способности к окислительно-восстановительным реакциям. 1. При действии на аскорбиновую кислоту раствором нитрата серебра происходит восстановление серебра (темный осадок); сама же аскорбиновая кислота окисляется и превращается в кетоформу.
2. При действии на аскорбиновую кислоту раствором 2,6-дихлорфенолиндофенола (окрашенного в синий цвет) последний восстанавливается, превращаясь в бесцветное лейкооснование.
Кроме этих двух реакций, рекомендуемых ГФ, можно привести еще целый ряд реакций, основанных на восстановительных свойствах аскорбиновой кислоты. а) с реактивом Фелинга — СuО восстанавливается до Сu2О красного цвета.
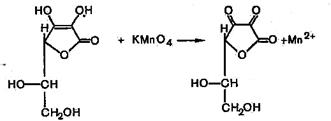
б) с раствором перманганата калия — происходит обесцвечивание раствора вследствие восстановления иона МnО2 до иона Мn2+.
в) с гексацианоферратом (III)калия в присутствии разведенной хлороводородной кислоты, с последующим добавлением раствора хлорида железа (III) — образуется берлинская лазурь, окрашивающая раствор в синий цвет.
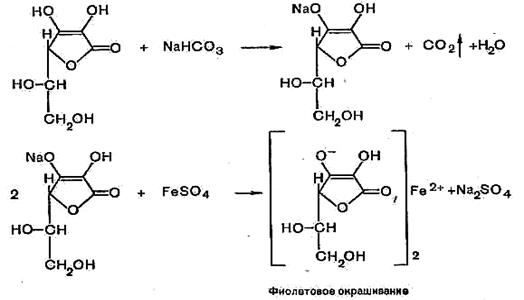
г) с раствором соли сульфата железа (II) — образуется аскорбинат железа, окрашенный в фиолетовый цвет.
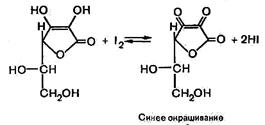
Количественное определение кислоты аскорбиновой также основано на ее химических свойствах. ГФ рекомендует иодатометрический метод. В этом случае титрантом служит раствор иодата калия. Титрование ведут в присутствии иодида калия и хлороводородной кислоты (индикатор крахмал) до стойкого синего окрашивания:
Количественное определение содержания аскорбиновой кислоты в растворах проводят также иодо-метрически, но здесь надо учитывать то обстоятельство, что в растворах аскорбиновой кислоты присутствует стабилизатор — гидросульфит натрия NaHSО3, который как восстановитель может реагировать с иодом. Поэтому предварительно к раствору аскорбиновой кислоты добавляют раствор формальдегида (формалин). Последний связывает гидросульфит натрия, и, таким образом, иод затрачивается только на окисление аскорбиновой кислоты.
Кислота аскорбиновая может определяться количественно и методом нейтрализации как одноосновная кислота.
Изменение структуры молекулы аскорбиновой кислоты приводит либо к уменьшению, либо к потере физиологической активности. Значительно снижает или полностью уничтожает физиологическую активность аскорбиновой кислоты увеличение числа углеродных атомов в молекуле. Применение. Применяют внутрь, внутримышечно и внутривенно. Выпускается в виде порошка, таблеток по 0,05 г и в ампулах по 1, 2 мл 5—10% растворов. Кислоту аскорбиновую часто применяют в комбинации с глюкозой (таблетки аскорбиновой кислоты с глюкозой), рутином (аскорутин). Она входит в состав поливитаминных препаратов. Хранение. Следует хранить в хорошо укупоренной таре, предохраняющей от действия света, в сухом, прохладном месте.
|